Clear Sky Science · zh
在共现的染色质特征上测序DNA甲基化和羟甲基化
解读细胞的化学注记
体内每个细胞携带相同的DNA,但脑细胞、皮肤细胞和干细胞的行为却大相径庭。原因之一是细胞会在DNA及其包裹蛋白上写入化学“注记”,帮助基因打开或关闭。到目前为止,科学家很难在同一段DNA上同时读取多种注记,这留下了关于它们如何协同工作的理解空白。本研究提出了一种新方法,能够同时读取基因序列和关键的化学标记,揭示它们如何结合来控制被称为增强子的关键DNA开关。
为什么DNA需要“铅笔痕迹”
DNA并非孤立运作。它绕在称为组蛋白的蛋白质上形成染色质,DNA和组蛋白都可以被小的化学基团修饰。两种重要的DNA标记是加在字母C(胞嘧啶)上的甲基和羟甲基。这些标记影响DNA的紧密程度以及邻近基因是否活跃。概括来说,甲基标记通常与基因沉默相关,而羟甲基标记往往出现在基因活跃的区域。但这些标记的影响取决于它们的局部环境:它们在基因组中的确切位置以及它们旁边的组蛋白标记类型。
分开绘制地图的问题
现有的测序方法可以在全基因组范围内绘制甲基和羟甲基标记,而其他方法可以绘制标记活跃或沉默区域的组蛋白标记。然而,这些通常在不同实验中完成,然后在计算机上进行比对。那样只能告诉我们哪些特征倾向于位于同一邻域,但无法确认它们是否真正共存在单个细胞的同一片段DNA上。早期尝试将这些测量结合的方法依赖于会损伤DNA的强烈化学处理,而且关键是无法在同一次读取中可靠地区分甲基与羟甲基。因此,研究者缺乏关于标记组合如何协作的清晰分子层面图景。
一种新的多层读取方法
作者开发了一种称为6-base-CUT&Tag的方法,能够读取所有四种DNA碱基以及胞嘧啶的两种化学状态——未修饰、甲基化和羟甲基化——在与所选染色质特征物理相连的DNA片段上。首先,他们使用类似分子钩子的抗体拉出缠绕在携带特定位点的组蛋白上的DNA,例如活性染色质的标记。随后,一种工程化的酶将特殊接头插入,使每个捕获到的DNA片段形成一个小环,从而在会破坏游离片段的清洗步骤中得以保存。经改良的化学与酶促流程接着将不同的胞嘧啶状态转换为可区分的序列信号,现代测序仪可以读取这些信号。这样,单次读取就能报告该片段来源、其携带的组蛋白标记以及其上哪些胞嘧啶是甲基化或羟甲基化的。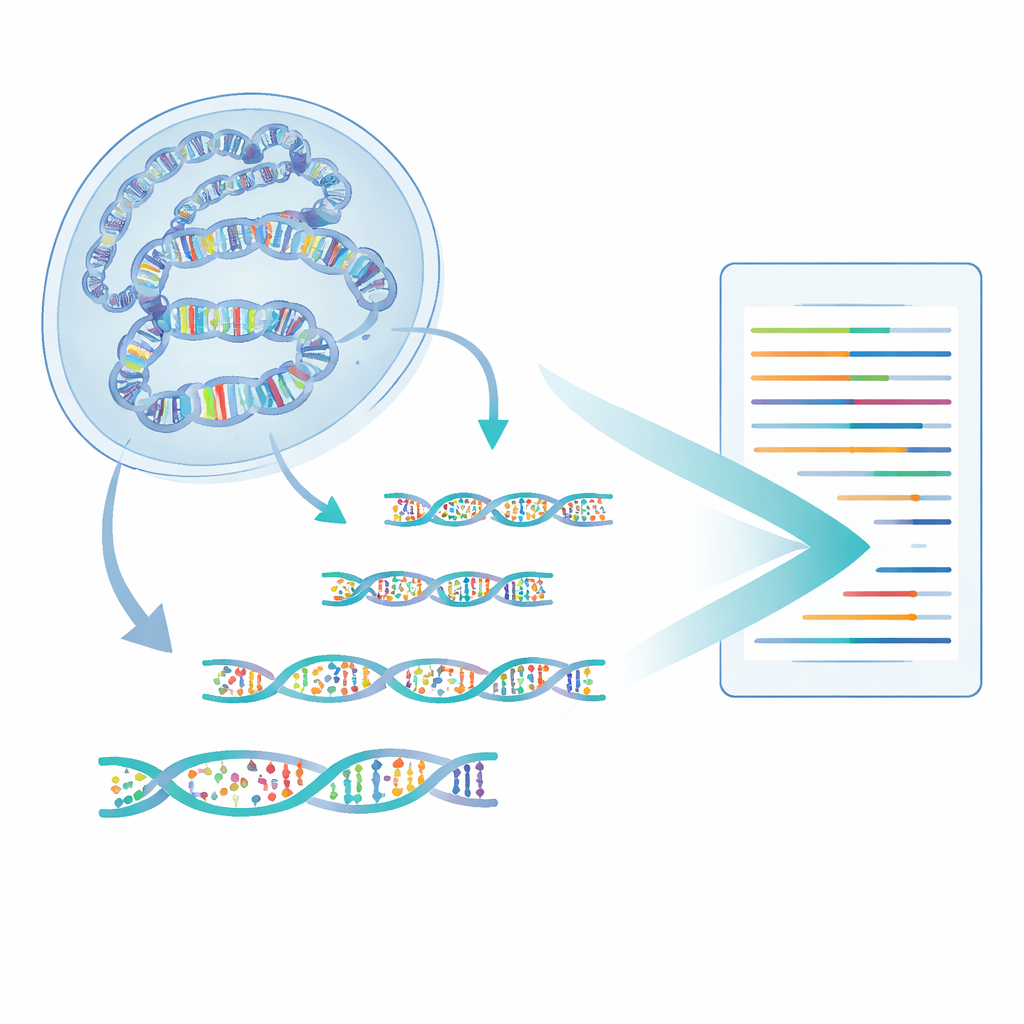
聚焦基因开关
研究团队以小鼠胚胎干细胞为测试对象,将6-base-CUT&Tag应用于若干标记不同类型调控DNA的关键组蛋白标记。他们重点研究增强子——作为开关控制基因何时何地开启的DNA片段。增强子可处于“活跃”、“预备”或“待命”状态,由特定的组蛋白标记区分。研究者发现,仅被一种称为H3K4me1的组蛋白标记(常被视为“预备”)标注的增强子,在DNA上显示出最高水平的甲基和羟甲基标记,尤其是在直接位于H3K4me1结合的核小体上。相比之下,带有强活性或抑制信号的增强子显示出较少的这些DNA标记,或倾向于向羟甲基化转变,这暗示甲基标记正在被擦除。
用更细致的视角解码增强子状态
由于所有增强子类型都共享H3K4me1标记,团队进一步探问仅在H3K4me1标注的DNA上检测到的DNA标记模式,是否足以区分不同的增强子状态。他们使用6-base-CUT&Tag数据训练了一个机器学习模型,单纯基于该组蛋白特征处的甲基和羟甲基含量,将增强子分类为活跃、预备或待命。该模型的表现优于用标准全基因组数据(不限制于任何组蛋白标记)训练的同类模型。换句话说,在标记实际发生的即时环境中读取DNA标记,比在细胞中对所有DNA取平均能提供更清晰的图景。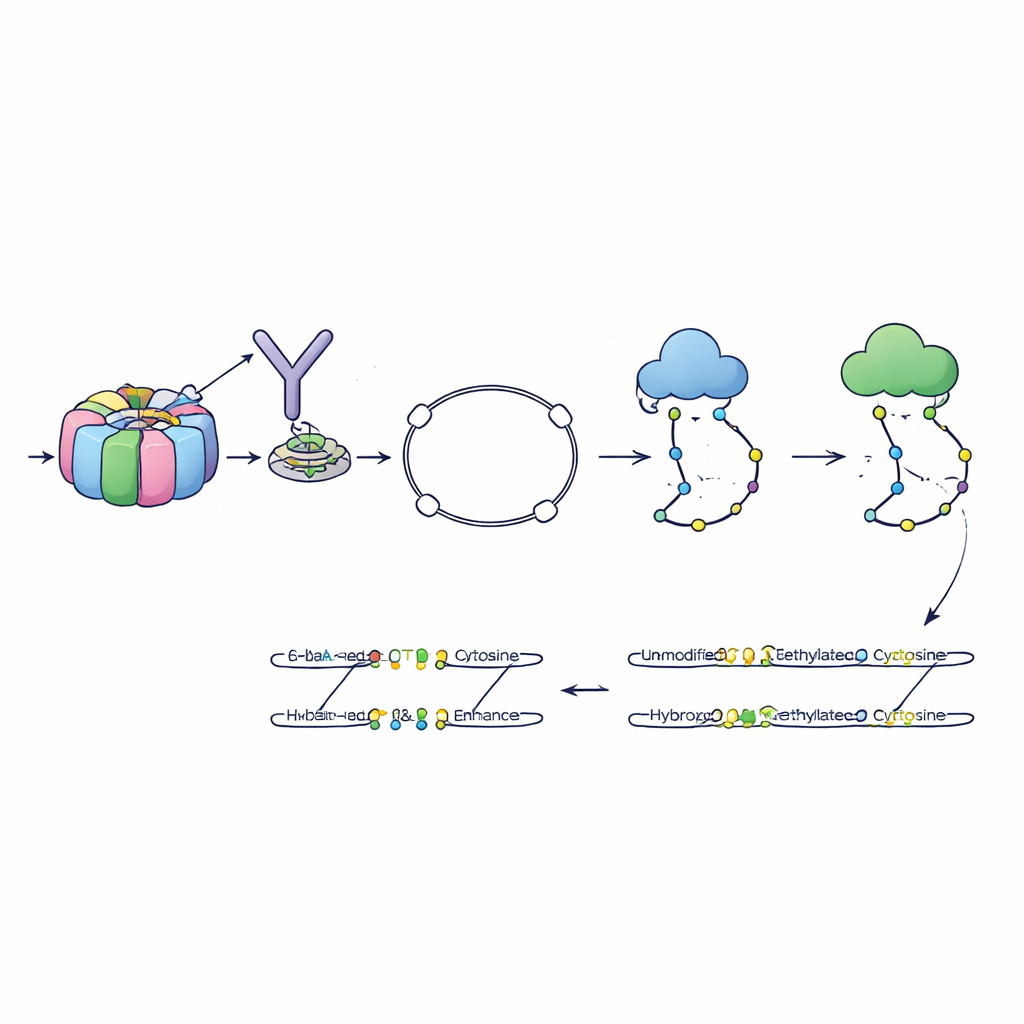
对理解细胞身份的意义
对非专业读者而言,关键信息在于该方法允许科学家在同一分子上读取多层信息——DNA序列、DNA标记和组蛋白标记。这样的细粒度视角揭示了特定化学标签组合如何定义干细胞中基因开关的准备状态。由于6-base-CUT&Tag比早期方法更高效且对DNA损伤更小,它能够发现此前被隐藏的微妙模式。随着时间推移,这种对染色质的多层读取有望帮助解释细胞如何记忆其身份、在发育或疾病过程中如何变化,以及我们如何更精确地在治疗中针对调控密码。
引用: Araujo Tavares, R.d.C., Dhir, S., He, X. et al. Sequencing DNA methylation and hydroxymethylation at co-occurring chromatin features. Nat Commun 17, 2591 (2026). https://doi.org/10.1038/s41467-026-69429-6
关键词: 表观遗传学, DNA甲基化, 染色质, 增强子, 干细胞