Clear Sky Science · zh
人类磷酸核糖酰甲酰甘氨酸胺化酶的别构调控与催化耦合的结构与分子基础
这种酶为何与健康相关
你体内的每个细胞都依赖嘌呤——这些小分子驱动反应、储存能量并承载遗传信息。增殖迅速的癌细胞对嘌呤尤其渴求,且常常重塑其合成途径。本研究聚焦于一种称为FGAMS(磷酸核糖酰甲酰甘氨酸胺化酶)的人源酶,它是从头合成嘌呤过程中的关键环节。通过揭示FGAMS的三维结构以及其各部分如何运动与互相通讯,作者阐明了该酶如何被开启或关闭,并指出了可能用于抑制肿瘤生长的靶点。
生命构件的受控组装
细胞通过被称为从头(de novo)途径的复杂装配线合成嘌呤,该过程耗能并依赖多种酶将一个复杂的环逐步拼接起来。FGAMS在这一序列中执行第四步,并坐落在被称为嘌呤体(purinosome)的更大酶簇中心,帮助高效地传递底物。由于快速生长的癌细胞常常增强这一途径,像FGAMS这样的酶成为有吸引力的药物靶点:抑制它们可以切断肿瘤获取核苷酸的来源,而健康细胞则可以依赖回收途径生存。
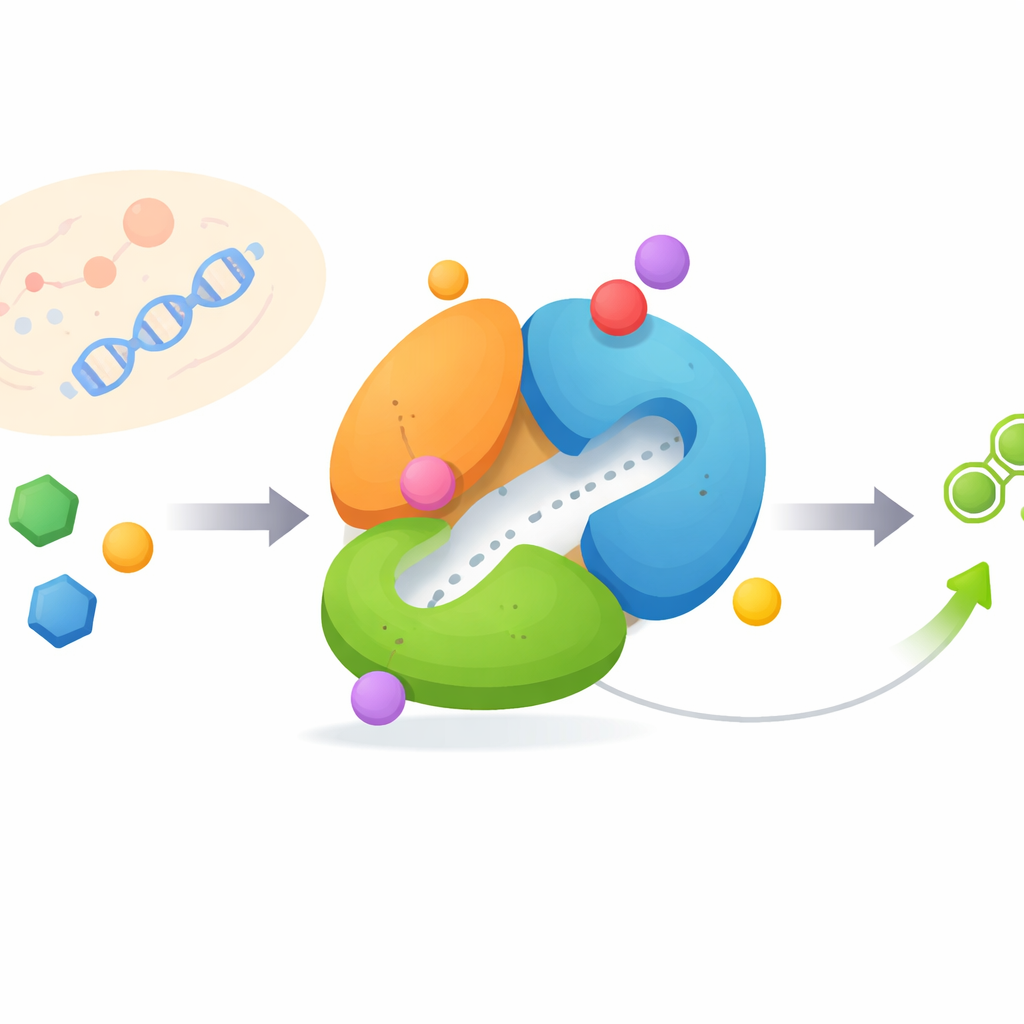
会变形的分子机器
FGAMS由三个连接的结构域组成,每个结构域执行不同任务并必须按精确顺序协同工作。一个结构域从氨基酸谷氨酰胺上切割出氨,另一个使用该氨改造一个小的糖基分子,第三个结构域则充当调控枢纽。研究人员利用高分辨率低温电子显微镜捕捉到了FGAMS的三种不同工作状态:结合能量分子的状态、捕获短寿命反应中间体的状态,以及同时存在多种底物与中间体的状态。比较这些状态显示,灵活的环段和N端的“臂”发生了剧烈位移,随着化学反应的推进重构了酶的构型。
隐匿的通道与分子闸门
一个关键谜题是:在一个结构域释放的氨如何安全传递到远端被使用的位点,而不扩散并造成损伤。新的结构揭示了一条此前未见的内部通道连接两个位点,并由若干特定氨基酸形成一系列“闸门”。当适当的底物结合并形成中间体时,一个中央环段折叠为有序构象,牵动N端结构域并重排催化结构域附近的环段。这一舞蹈式变化打开了两个入口闸门,使谷氨酰胺得以被处理,并短暂重塑了一个稳定高能中间体、便于断键的区域。
通过运动耦合化学反应
随着反应进行,酶并非被动等待;它利用每一步化学变化作为信号。一旦在产生氨的结构域形成了共价硫酯中间体,先前的运动部分被逆转。这放松了中央环段并重新定位闸门以封堵泄漏通路,同时通道两端的另外两个闸门打开。若干“瓶颈”残基的微小位移扩大了内部通道,使一分子氨能够通过通道直接进入第二个活性位点,与被捕获的中间体反应生成最终产物。对这些闸门残基的突变会导致氨泄漏或两段反应解耦,证实该闸门—通道系统对高效催化至关重要。
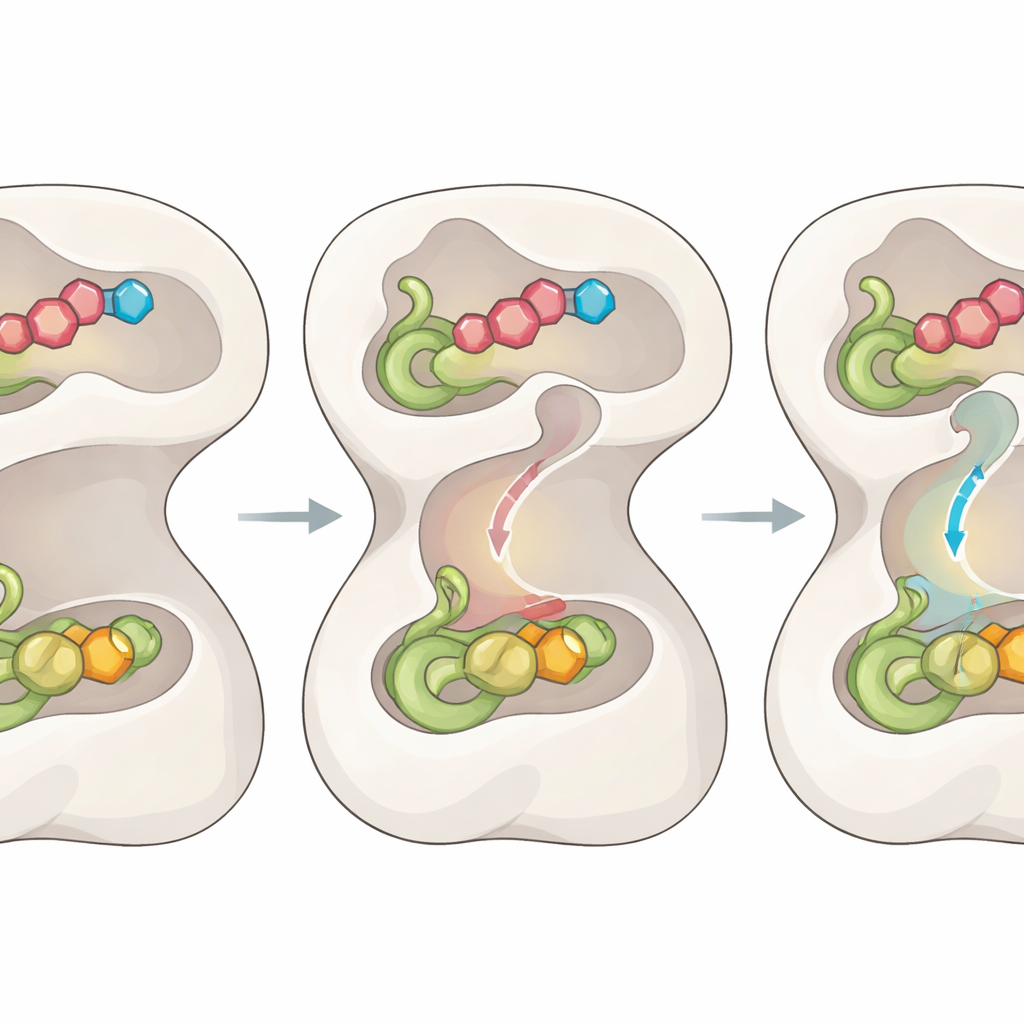
从结构认识到治疗路径
通过追踪FGAMS在催化循环中的历程,本研究勾勒出域运动、灵活环段、内部闸门与瞬时通道如何协同布线以协调化学反应的详细图景。对普通读者而言,结论是该酶像一个微型可编程工厂:只有在所有合适部件就位时才打开大门和内部传送带,从而兼顾速度与安全性。由于FGAMS支持癌细胞的嘌呤生成并与肝肿瘤的不良生存率相关,所得到的结构蓝图和新发现的控制点为设计阻塞通道、冻结闸门或捕获关键中间体的药物提供了多重立足点,可能催生新一类靶向抗癌疗法。
引用: Sharma, N., Zhou, W. & French, J.B. Structural and molecular basis for allosteric regulation and catalytic coupling of human phosphoribosylformylglycinamidine synthase. Nat Commun 17, 2732 (2026). https://doi.org/10.1038/s41467-026-69423-y
关键词: 嘌呤生物合成, 别构调控, 氨通道化, 癌症代谢, 低温电子显微镜结构