Clear Sky Science · zh
由肉芽肿微环境引导的声-免疫疗法用于治疗并预防结核病复发
为何这种新的结核病方法重要
结核病仍然感染了全球四分之一的人口,并且即使在长期抗生素治疗后也可能复发。本研究描述了一种有针对性的“声学+免疫”疗法,旨在不仅杀死藏匿于肺深处的结核分枝杆菌,还重新训练免疫系统,使疾病更不容易复发。该方法结合了来自患者样本的见解与一种可由医用超声激活的智能纳米颗粒药物。
肺结节内的隐秘战场
当结核病菌入侵时,肺部的免疫细胞会将自身围成紧密的组织结节,称为肉芽肿。这些结构旨在囚禁细菌,但也为微生物创造了一个隐蔽的利基,使其能够潜伏并躲避抗生素。通过重新分析来自人类肺组织的单细胞RNA测序数据,研究人员将普通的非结核性肉芽肿与真正的结核性肉芽肿及健康肺组织进行了比较。他们发现,在结核病病变中,关键的“第一应答”细胞——巨噬细胞和树突状细胞——已转入一种抑制状态。那些通常感知细菌并发出警报的分子通路被下调,而抑制免疫活性的基因则被上调。
当免疫系统踩下制动
研究团队随后考察了来自耐药与敏感结核病患者的血样,以及病情复发或保持治愈的患者样本。在这些群体中出现了相同的模式:负向调节免疫的基因和通路在耐药及复发者中更为活跃。本应帮助免疫细胞识别并清除细菌的信号变弱。这表明治疗失败不仅与药物或细菌有关,还与免疫微环境被推入过度受抑、“耐受”状态有关,尤以肉芽肿内部为甚。
设计一种声激活的辅助颗粒
以这种免疫瘫痪的图景为指导,研究人员设计了一种名为 manSNI 的纳米颗粒。它由一种有机半导体聚合物构成,暴露于超声时可产生一阵阵活性氧(ROS);表面包覆甘露糖有助于靶向巨噬细胞;并载有一种小分子免疫激活剂,可刺激这些细胞上的Toll样受体。在体外实验中,manSNI颗粒在受感染的巨噬细胞溶酶体内聚集,在超声作用下产生足以摧毁超过99%结核模型细菌的ROS,即便超声需穿过数厘米组织。活性氧还破坏了细菌膜,释放出可作为抗原的细菌蛋白质。
将“冷”肉芽肿变成“热”免疫枢纽
在患有类结核性肺病的小鼠中,manSNI在肉芽肿中的累积远高于缺乏甘露糖靶向基团的类似颗粒。当肺部短暂暴露于超声时,肺内细菌计数几乎降至零。与此同时,局部免疫景观发生了转变。巨噬细胞向促炎、抗菌状态转变;树突状细胞成熟并将抗原信息带到邻近淋巴结;结核特异性的T细胞和产生抗体的B细胞扩增。对肺组织的基因表达分析显示,先前在人体肉芽肿中被抑制的若干关键感知与防御通路现已被强烈重新激活。
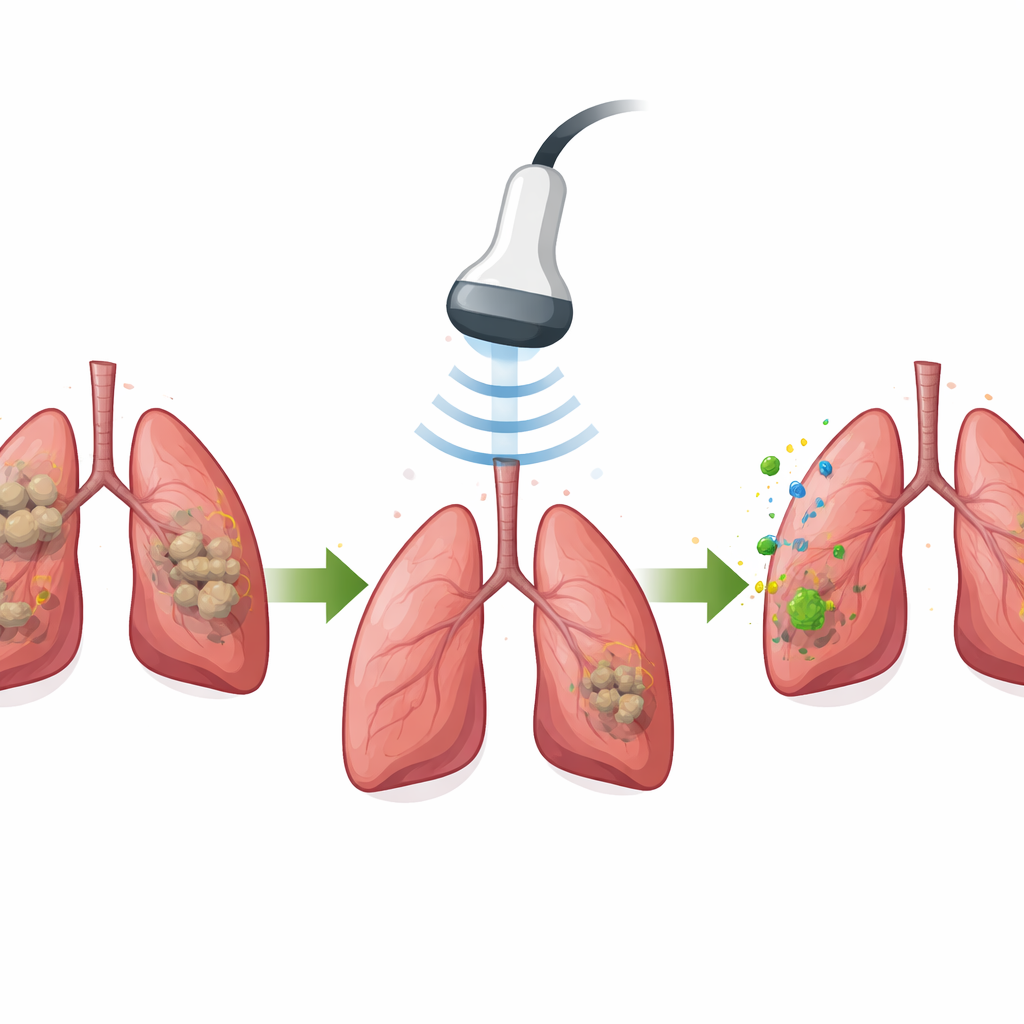
建立对复发和再感染的持久保护
清除首发感染仅是挑战的一部分;许多患者会再次发生结核病,可能是残存细菌或新暴露所致。在长期小鼠研究中,作者将一种标准抗生素(利福平)与 manSNI 加超声进行了比较。两种方案都能在初期清除可检测细菌,但仅用抗生素后复发很常见,而声-免疫疗法后复发则很少。接受 manSNI 的动物在肺中形成了更高水平的组织驻留记忆T细胞,在淋巴器官中具有更多中心和效应记忆T细胞,且血液中存在长期存留的记忆B细胞和抗体。当这些小鼠被故意再次暴露于结核模型细菌时,大多数能够抵抗再感染或仅出现轻微、短暂的病灶。
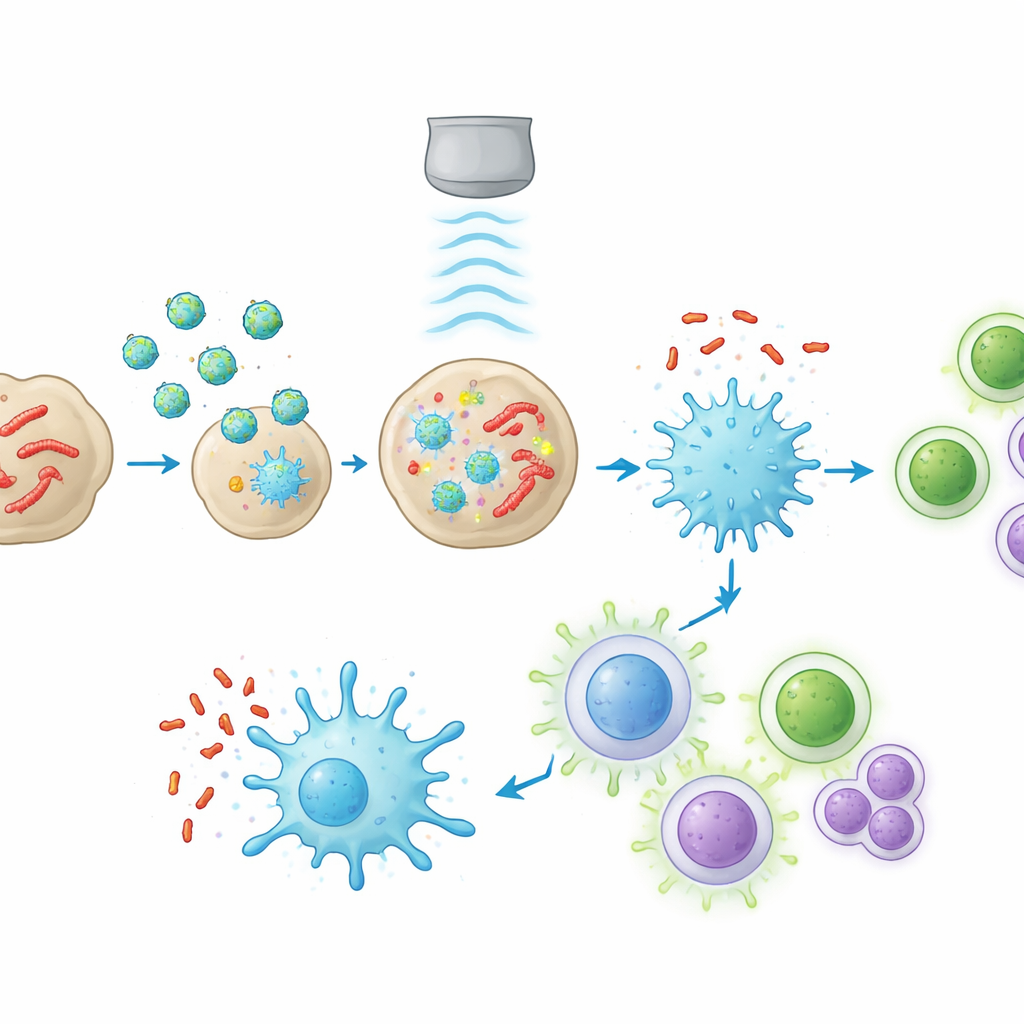
这对未来结核病护理可能意味着什么
对于非专业读者,主要结论是该工作提供了一种双管齐下的策略:直接摧毁藏匿在难以触及的肺结节中的细菌,同时将局部免疫环境从“关闭”重置为“开启”。该方法利用在临床中已常见的超声,非侵入性地激活一种精确靶向的纳米颗粒,既能杀死病原体,又能发挥类似内置疫苗助剂的作用。尽管实验在小鼠和较安全的模型菌株上进行,而非最危险的结核分枝杆菌,但结果提示了一条通向更短、更有效治疗的道路,这类治疗不仅能治愈结核病,还可大幅降低其复发的概率。
引用: Wang, W., Li, F., Mo, W. et al. Granulomas microenvironment-guided sono-immunotherapy to treat and prevent recurrence of tuberculosis. Nat Commun 17, 2595 (2026). https://doi.org/10.1038/s41467-026-69420-1
关键词: 结核病, 声免疫疗法, 纳米颗粒, 肉芽肿, 超声治疗