Clear Sky Science · zh
用于丙型肝炎病毒疫苗设计的原生样可溶 E1E2 糖蛋白异二聚体装配于自组装蛋白纳米颗粒上
为什么需要更好的丙型肝炎疫苗
丙型肝炎是一种隐匿性感染,可能在多年内缓慢地导致肝脏瘢痕形成,症状出现前已进展为肝硬化与肝癌。尽管现有药物能治愈大多数感染,但价格昂贵、不能阻止再次感染,且无法逆转已发生的肝脏损伤。本研究提出一种新型疫苗策略,旨在在病毒入门处阻断感染:将精确设计的病毒表面蛋白固定在微小蛋白颗粒上,训练免疫系统识别并在病毒建立感染前将其中和。
瞄准病毒的分子钥匙
丙型肝炎通过一对称为 E1 和 E2 的表面蛋白进入肝细胞,这对蛋白共同起到分子钥匙的作用。它们是“广谱中和抗体”的主要靶点——这类免疫分子可以阻断多种不同毒株。然而,E1 和 E2 天生柔软、被大量糖基覆盖、且在毒株间高度多样化,这使得构建既外观又行为像天然蛋白的疫苗版本十分困难。早期尝试未能可靠地将这对脆弱的蛋白稳定在能暴露最具保护性的抗体靶位的构象上。
设计稳定的病毒诱饵
受近期高分辨率丙型肝炎表面结构图像的启发,研究者们对 E1E2 进行了重设计,使其成为可溶、适合疫苗使用且仍模仿天然病毒的“诱饵”。他们修剪了通常位于病毒膜附近的柔性尾区,并删除了 E1 中倾向于导致聚集的松散环。随后将 E1 和 E2 融合到一种特制的蛋白支架 SPYΔN 上,该支架像安全别针一样将两者锁定在一起。该设计产生了纯净、稳定的 E1E2 复合物,主要保持目标构象,不易解体,并能强烈结合多种已知能中和多样化丙型肝炎毒株的人源抗体。
用纳米颗粒放大免疫信号 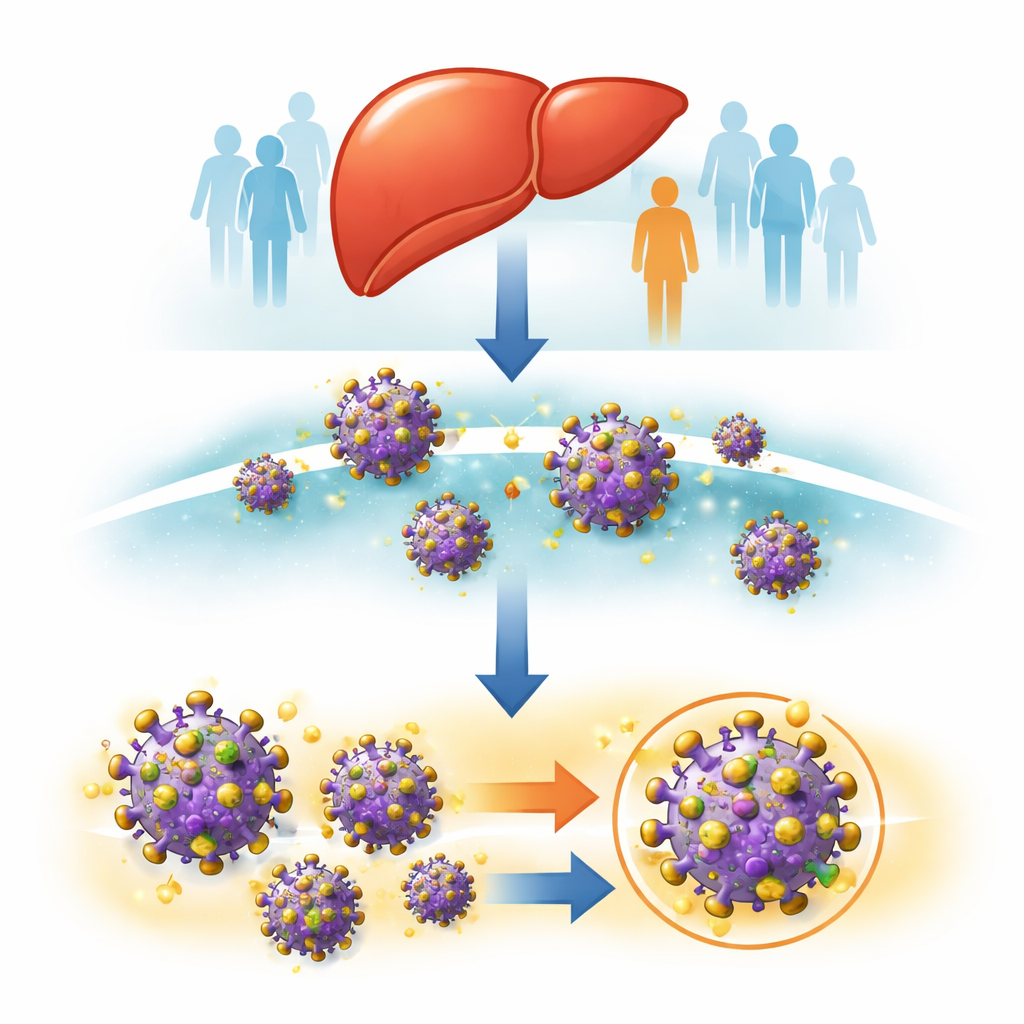
Figure 1.

为增强免疫反应,团队将数十个这种稳定化的 E1E2 复合物连接到自组装蛋白纳米颗粒上,形成带有大量相同棘突的类病毒球体。他们使用两种载体颗粒:较小的 24 亚基铁蛋白空壳和较大、多层的 60 亚基设计。通过化学修饰控制 E1E2 上糖基的分布,使其更接近天然病毒的“糖盾”,因为糖基图谱会影响抗体如何识别和结合表面。实验室测试显示,将 E1E2 安排在纳米颗粒上能显著增强与多种保护性抗体及丙型肝炎用于进入肝细胞的受体 CD81 的结合,表明病毒表面的关键特征被忠实再现。
在小鼠中测试保护效果 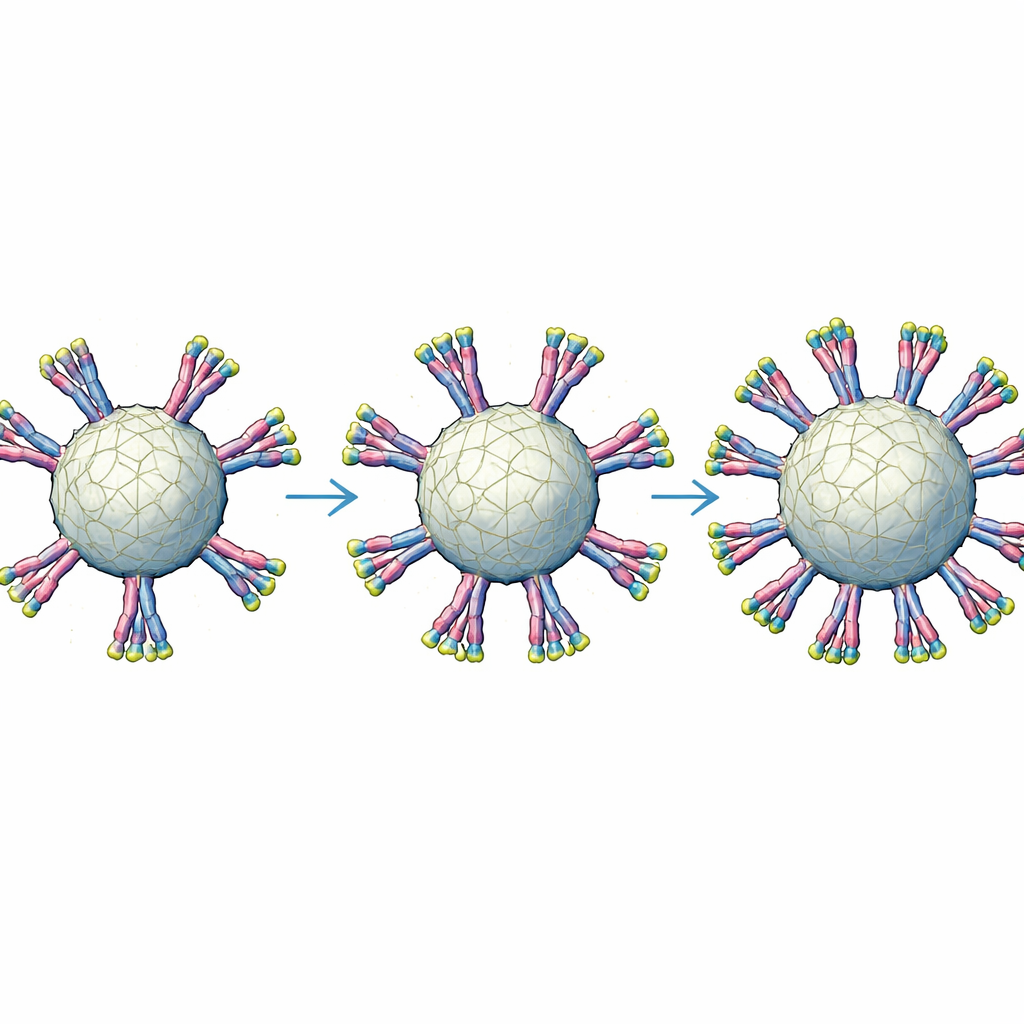
Figure 2.

研究者随后用游离的 E1E2 或不同糖基修饰的纳米颗粒展示型对小鼠免疫注射。来自接种动物的血液被用于针对一组代表多种基因型和抵抗水平的丙型肝炎“假病毒”进行检测。与游离 E1E2 蛋白相比,纳米颗粒疫苗持续产生更强且更迅速的中和抗体反应,而较大的 60 亚基颗粒在诱导跨多种病毒株有效的抗体方面尤为出色。将糖基修改为更简单、更类病毒的形式可带来额外但适度的提升。团队还观察到雌鼠的免疫反应强于雄鼠,以及用于生产蛋白的细胞系类型会微妙地改变保护的广度。
这项工作如何推动疫苗设计向前
本研究提供了一套可行的方法,用于构建“原生样”丙型肝炎表面蛋白并将其有序展示在蛋白纳米颗粒上。通过将 E1E2 锁定为稳定、模拟病毒的形态并在单个颗粒上排列多个拷贝,研究者创造了能引导免疫系统关注病毒最脆弱部位的疫苗候选物。在小鼠中,这些构建体诱导出可中和并阻断若干难缠丙型肝炎毒株的抗体,为下一代有望预防感染并助力实现全球丙型肝炎消除目标的疫苗奠定了基础。
引用: He, L., Lee, YZ., Zhang, YN. et al. Native-like soluble E1E2 glycoprotein heterodimers on self-assembling protein nanoparticles for hepatitis C virus vaccine design. Nat Commun 17, 2633 (2026). https://doi.org/10.1038/s41467-026-69418-9
关键词: 丙型肝炎疫苗, 病毒纳米颗粒, E1E2 糖蛋白, 广谱中和抗体, 基于结构的设计