Clear Sky Science · zh
细胞壁水解促进第二波转肽反应以在巴氏芽孢杆菌隔膜形成后实现细胞分离
细菌如何完成一分为二
细菌分裂速度惊人,同时还能在不破裂的情况下构建并重建其坚固的外壳。本研究揭示了土壤细菌巴氏芽孢杆菌完成细胞分裂的一个隐藏的最后步骤。研究表明,在两个未来子细胞之间的新壁已经形成之后,壁先被切开,然后从内部被细微地重新缝合。理解这一额外步骤有助于解释细菌如何保持形状和强度——也可能为破坏有害微生物提供新的途径。
先建墙,然后放手
当棒状细菌如巴氏芽孢杆菌分裂时,首先构建一个称为隔膜的扁平内壁,将母细胞分成两个隔室。该壁由肽聚糖构成——由短肽连接的糖链网状结构,形成包裹细胞的保护笼。在许多具有两层膜的细菌中,隔膜的构建与切割同时进行。但在拥有单层厚壁的巴氏芽孢杆菌中,这一过程被分为两步:隔膜先完全构建,随后才被打开以让子细胞分离为单独的杆状体。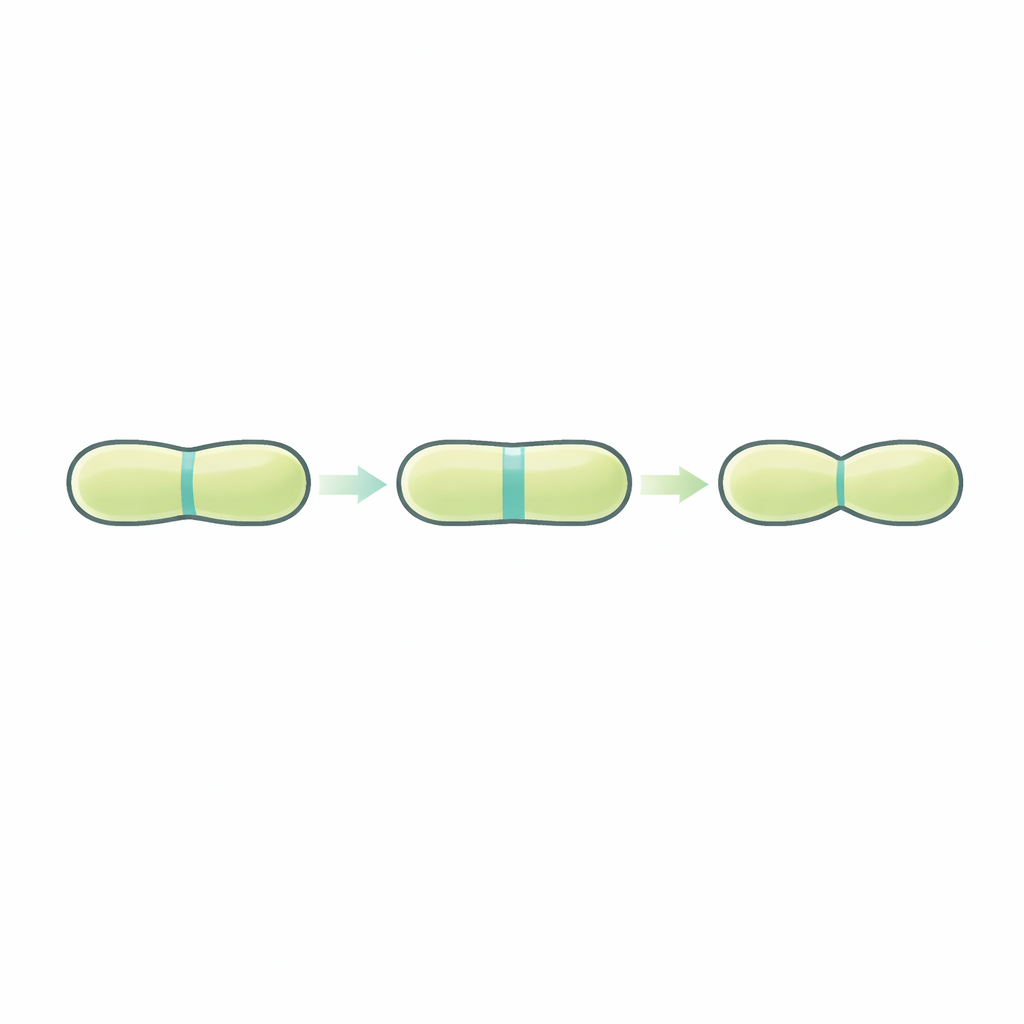
追踪隐藏的建造工作
作者使用了模拟细胞壁天然成分的特殊荧光构件。这些探针在被酶整合进肽聚糖网时会发光,使研究者能够看到连接反应发生的时间和位置。借助高分辨率三维显微镜,他们追踪了成千上万细胞中的这些信号。研究证实,在隔膜从细胞外缘向中心内生长、形成完整扁平板时存在第一波活性。出乎意料的是,他们随后观察到第二波、较晚的交联活性,这波活性从已完成隔膜的边缘开始并在细胞开始分离时向内传播。
在不添加新材料的情况下重塑
一个关键问题是,这种晚期活性是反映新细胞壁材料的插入,还是仅仅对已有结构的重排。为此,团队标记了一种必须在添加新链时使用的可溶性前体。他们仅在隔膜早期构建阶段观察到该前体,而在后期分离阶段未见到。通过结合多种荧光标记,他们表明第二波活性利用的是已有的、先前未交联的肽链作为原料。换言之,一旦隔膜建成,细胞并不进一步增厚它;相反,细胞切割并重新交联同一网状结构,以增强正在形成的子细胞端极的强度。
切割者与缝合者协同工作
研究确定了参与重塑的两个主要分子。酶LytF充当切割者,切断壁中的键以打开隔膜。另一种酶PBPH是转肽酶,负责将肽链缝合在一起。通过缺失不同壁切割酶的突变体,作者表明当LytF的活性被去除或失活时,第二波交联在很大程度上消失,细胞保持连成长链。同样,当PBPH缺失时,细胞在分离上表现出明显缺陷,且在完整隔膜处几乎没有晚期交联。带荧光标记的蛋白成像进一步显示,LytF仅在早期分裂支架离开后才到达隔膜,而PBPH在分离位点的持续存在依赖于LytF的切割作用。这些观察共同支持这样一种模型:LytF按时分解细胞壁,暴露或重新排列出可供PBPH交联的肽链,从而加固新生极点。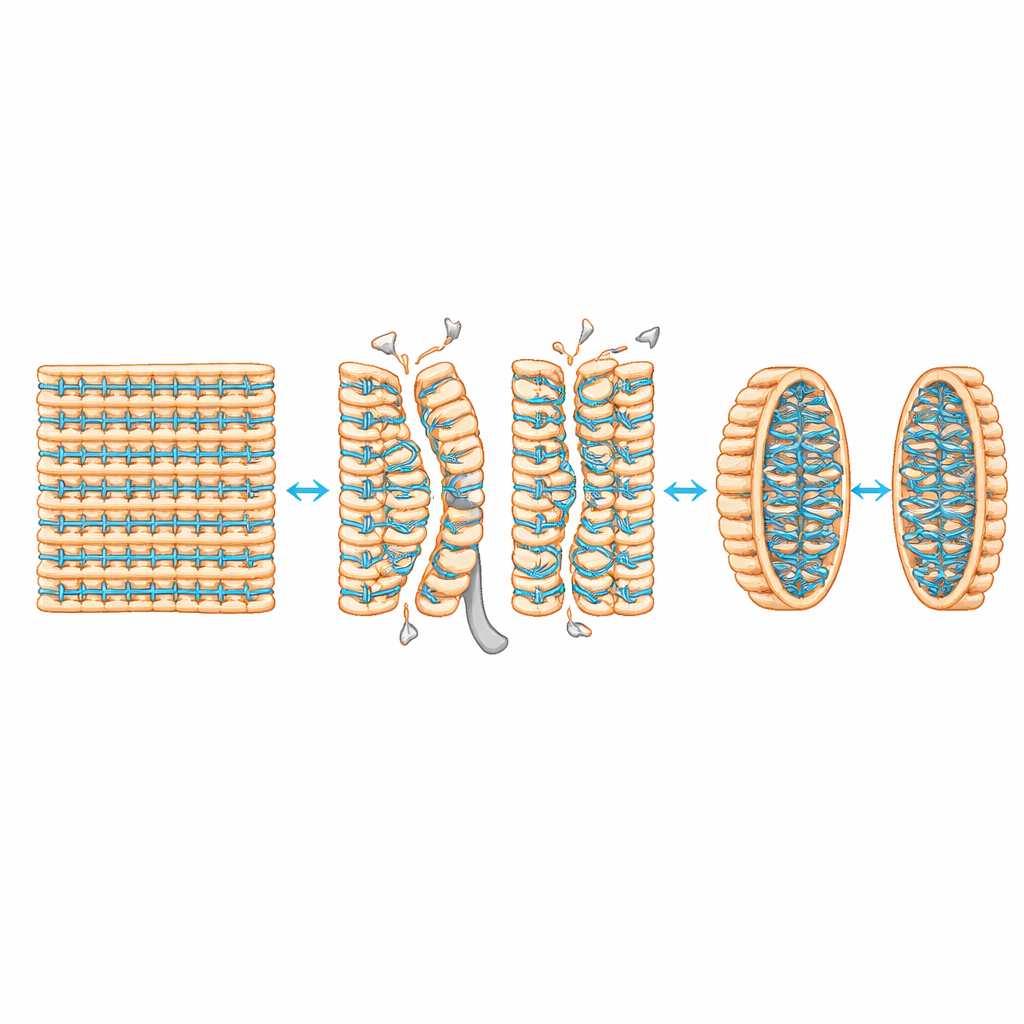
第二波为何重要
随着扁平的隔膜被重新塑形为两个圆形极点,肽聚糖所承受的机械负荷发生剧烈变化:新极点不再受到两侧的对称压迫,而必须承受来自子细胞内部的内压。作者提出,第二波交联在壁被切割并弯曲时使其变刚并稳定,防止破裂。由于许多其他革兰氏阳性细菌也以类似的两步方式分裂——先完成隔膜,再分离——这种重塑波可能是这些微生物安全完成分裂的普遍特征。通过揭示这一隐藏的最后步骤,该研究细化了细菌细胞分裂的教科书式描述,并为旨在在细菌最脆弱时刻削弱其细胞壁的抗生素提供了新的潜在靶点。
引用: Patel, V., Hsu, YP., Debnath, M. et al. Cell wall hydrolysis promotes a second wave of transpeptidation to achieve cell separation following septation in Bacillus subtilis. Nat Commun 17, 2689 (2026). https://doi.org/10.1038/s41467-026-69404-1
关键词: 细菌细胞分裂, 肽聚糖, 巴氏芽孢杆菌, 细胞壁重塑, 转肽酶