Clear Sky Science · zh
源自巨噬细胞的乳酸通过MCT1诱导的组蛋白H3第23位赖氨酸乳酸化驱动增生性瘢痕中皮肤真皮成纤维细胞表型重塑
为何有些瘢痕变得又厚又高
大多数割伤和烧伤最终会淡化为薄而平的瘢痕。但有些伤口愈合后出现厚而凸起的组织带,称为增生性瘢痕,可能伴随瘙痒、疼痛并限制活动。该研究揭示了这些顽固瘢痕的一个意想不到的驱动因素:一种常见的代谢副产物——乳酸,由在僵硬愈合皮肤中的免疫细胞产生,能重编程邻近修复细胞,使其表现出更具攻击性、更倾向瘢痕化的行为。
从正常修复到问题性瘢痕
在健康的伤口愈合过程中,皮肤细胞协同工作以闭合损伤并重建组织。成纤维细胞是皮肤深层的主要修复细胞,会在短时间内转为更强的表型以合成胶原——皮肤的蛋白质支架。伤口封闭后,这些细胞会再次静止。然而在增生性瘢痕中,成纤维细胞停留在这一过度活跃的状态,沉积过多的胶原,形成厚且紊乱的束。作者首先比较了正常皮肤与增生性瘢痕组织,发现明显的代谢转变:瘢痕环境偏向快速的糖代谢产生大量乳酸,并伴有高水平的运输蛋白MCT1,负责将乳酸运入细胞。 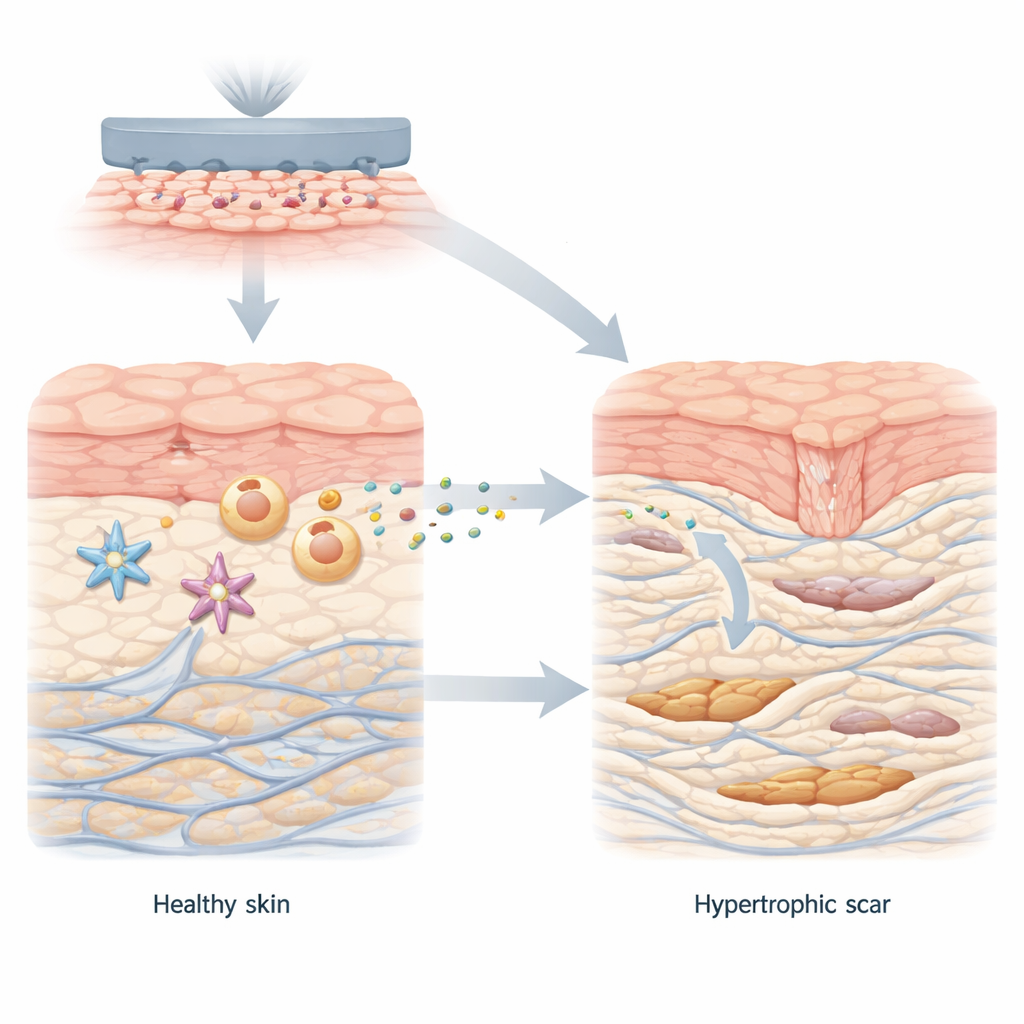
免疫细胞是意想不到的乳酸工厂
为找出这些乳酸的来源,研究团队检查了来自人皮肤和小鼠模型的不同细胞类型:巨噬细胞(清除碎片并协调愈合的免疫细胞)、血管细胞和成纤维细胞。他们在模拟正常与瘢痕皮肤的软或硬基材上培养这些细胞。在刚性表面上,唯有巨噬细胞转向高度有氧糖酵解(或称“嗜糖”)模式并大量释放乳酸——这一现象既在体外培养中出现,也在实际瘢痕组织中观察到。当在愈合的小鼠伤口中移除巨噬细胞时,组织乳酸水平下降且瘢痕形成减轻。这些结果表明,尤其是在感知到刚性环境的情况下,巨噬细胞是塑造瘢痕微环境的主要乳酸制造者。
乳酸作为重编程成纤维细胞的信号
接下来,研究人员探讨了过量乳酸如何影响成纤维细胞。当成纤维细胞被浸泡在来自刚性培养巨噬细胞的乳酸丰富液体中时,它们增殖更快、迁移能力增强,并产生更多胶原,这些都是具侵袭性肌成纤维细胞表型的标志。阻断成纤维细胞上的MCT1运输蛋白或减少巨噬细胞的乳酸生成,能显著降低这些变化。在成纤维细胞内,外来的乳酸不仅作为能量底物:它触发了组蛋白蛋白上的特定化学标记,这些组蛋白用于在细胞核中包装DNA。这种标记称为H3K23乳酸化,在形成瘢痕的成纤维细胞中显著更高,且像开关一样启动了两个关键基因HEY2和COL11A1,二者共同增强瘢痕化信号。
自我增强的瘢痕循环
由该组蛋白标记驱动的蛋白质构成了一个强大的反馈回路。HEY2增强了涉及YAP1和SMAD2的通路活性,该通路已知促使成纤维细胞趋向更具收缩性和胶原生成的状态。COL11A1作为一种与胶原相关的结构蛋白,物理性地与成纤维细胞上的MCT1运输蛋白相互作用,帮助稳定MCT1并提高乳酸摄取效率。换言之,进入细胞的乳酸通过改变基因调控,进一步增强乳酸进入和胶原生成,使成纤维细胞被锁定为有利于瘢痕形成的身份。 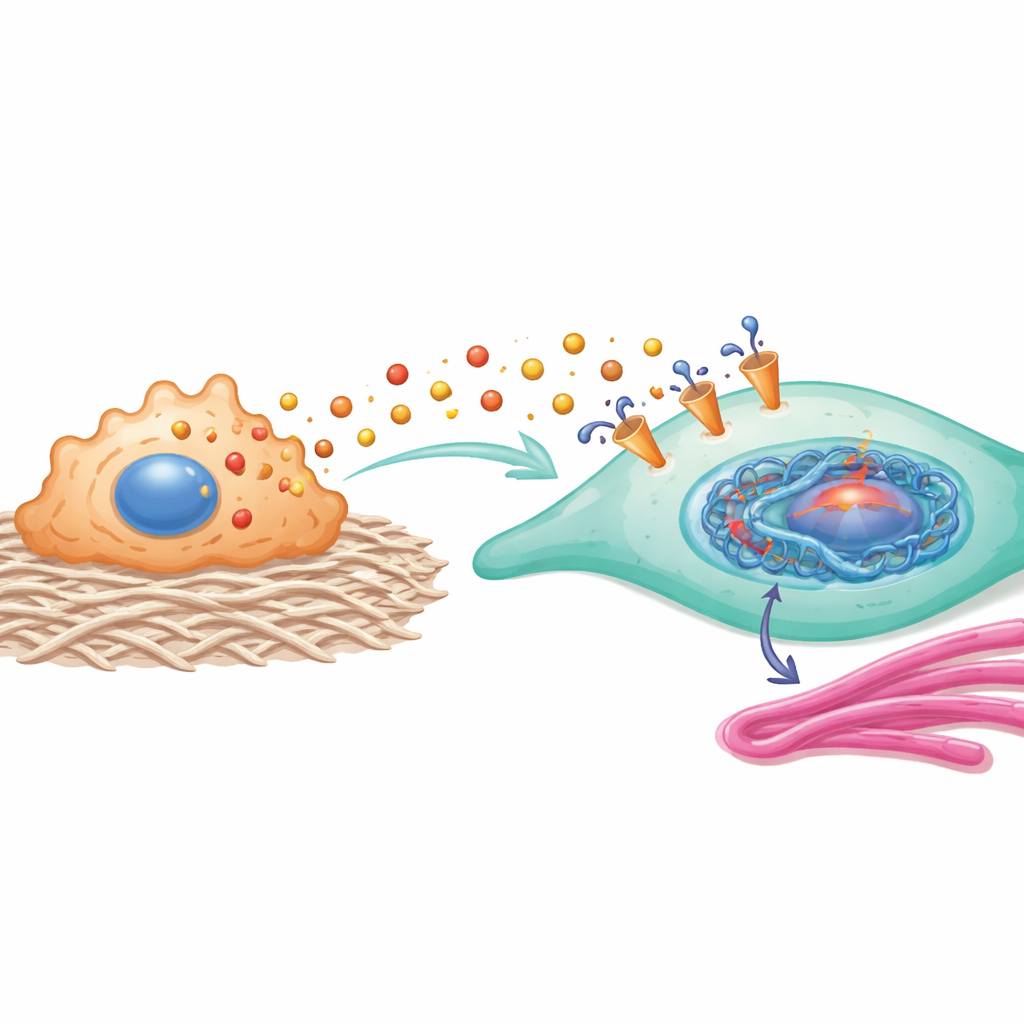
关闭该循环以改善愈合
为测试中断该循环是否能改善愈合,团队使用了可以选择性从成纤维细胞中删除MCT1的小鼠,以及一种阻断MCT1的药物。在两种情况下,伤口愈合更快,新生皮肤结构更有序,胶原纤维更细且排列更好,具有的增生性瘢痕特征减少。特定的组蛋白标记及其下游基因也显著下降。耗竭巨噬细胞这一主要乳酸来源或化学降低乳酸水平,也产生了类似的抗瘢痕效果。这些实验证明,刚性伤口—巨噬细胞—乳酸—成纤维细胞链条不仅是相关性观察,而是病理性瘢痕形成的关键驱动因素。
这对未来瘢痕治疗意味着什么
这项工作将乳酸从单纯的代谢废物重新定位为在创伤愈合中连接力学、代谢与基因控制的强大信使。通过展示巨噬细胞来源的乳酸通过MCT1被转运、改变组蛋白并在成纤维细胞中启动自我强化的瘢痕程序,研究突出了若干有前景的治疗靶点。调节乳酸产生、阻断MCT1或干预特定组蛋白修饰的药物,未来或可帮助伤口更快愈合并形成更平、更不明显的瘢痕。
引用: Yuan, Y., Xiao, Y., Zou, J. et al. Lactate derived from macrophages drives skin dermal fibroblasts phenotypic remodeling via MCT1-primed histone H3 lysine 23 lactylation in hypertrophic scar. Nat Commun 17, 2694 (2026). https://doi.org/10.1038/s41467-026-69388-y
关键词: 增生性瘢痕, 乳酸信号, 巨噬细胞—成纤维细胞串话, 组蛋白乳酸化, 创伤愈合疗法