Clear Sky Science · zh
为炎性肠病递送抗体的工程化外泌体纳米囊泡
为顽固肠道疾病带来新希望
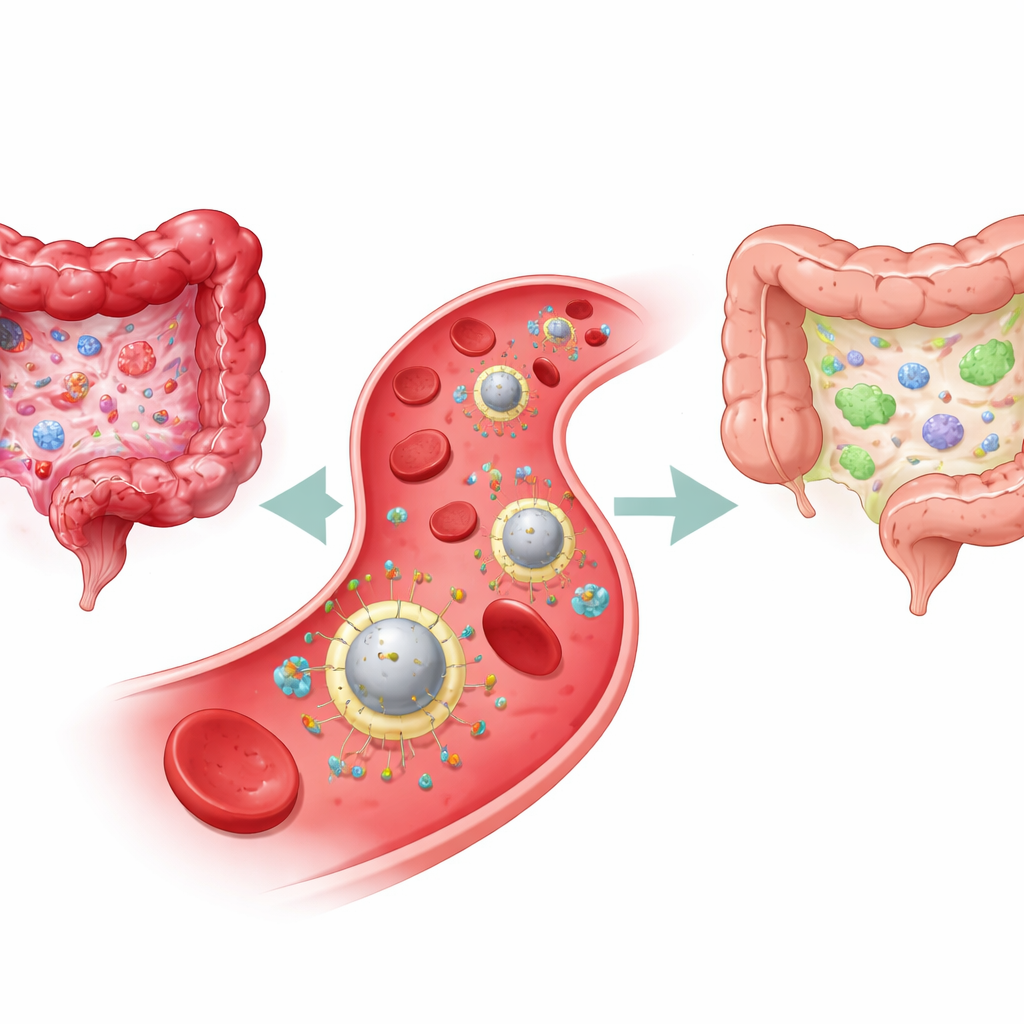
炎性肠病(IBD)会把日常生活变成与疼痛、腹泻和疲劳的持续斗争,并增加长期患结肠癌的风险。许多现有药物能够缓解发作,但并未真正重置驱动疾病的错误免疫反应,因此症状常常会复发。本研究介绍了一种巧妙设计的“智能”纳米颗粒,它随血液循环,定位肠道炎症部位,并递送一种双重疗法,既抑制有害炎症,又重建持久的免疫平衡。
为何现有治疗不够
IBD 包括克罗恩病和溃疡性结肠炎,源于肠道免疫系统的慢性拉锯战。一方是具有攻击性的免疫细胞和损伤肠道黏膜的炎性分子;另一方是通常负责抑制该反应的调节细胞。常规疗法——如类固醇、免疫抑制剂和生物制剂——主要试图在全身范围内钝化炎症。它们可以缓解症状,但常常难以恢复根本的免疫平衡,而且广泛的免疫抑制会增加感染风险。即便是阻断一种关键炎性信号白介素‑23(IL‑23)的新型抗体药,也仅对部分患者有效,而且仍在全身循环,而非只在需要的部位发挥作用。
构建一种能归巢、会变形的药物
研究人员旨在设计一种更像活细胞而非单纯药物的疗法。他们以调节性T细胞天然释放的微小囊泡为起点——这些免疫细胞有助于促成耐受和维持免疫“和平”。这些被称为外泌体的囊泡携带蛋白质和遗传物质,能够引导其他免疫细胞进入更为平和的状态。团队将这些外泌体与血小板膜片段融合,借用血小板粘附受损血管、定位炎症组织的特性。在这个混合外壳表面,他们用一种可被仅在炎症肠组织中丰富的酶(基质金属蛋白酶)切割的分子“绳索”固定了阻断 IL‑23 的抗体。最终产物命名为 PrEXO‑a23,这是一种在血液中循环、能黏附受损肠道血管并仅在疾病活跃处释放抗体负载的纳米囊泡。
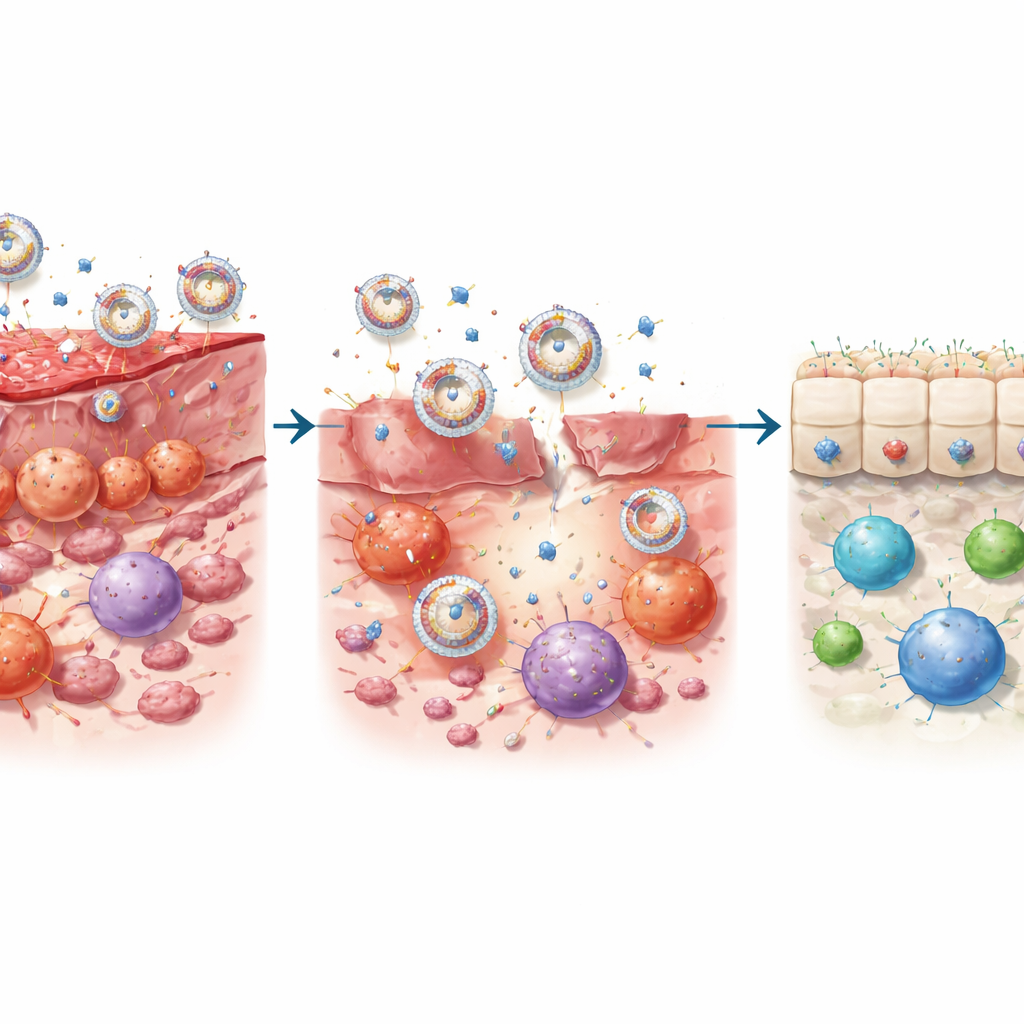
重塑肠道免疫小环境
在细胞实验中,PrEXO‑a23 的表现优于单独使用抗体或外泌体。它显著减少了促炎的辅助性T细胞17(Th17)细胞的形成以及损伤肠道黏膜的有害细胞因子的释放,同时保护了人类肠上皮细胞免于死亡。与此同时,它将树突状细胞——指导T细胞的“门卫”——从一种有敌意的激活状态推向一种鼓励调节性T细胞生长的“耐受”状态。在结肠炎小鼠模型中,这些纳米囊泡能够高效归巢至炎性结肠组织,被多种免疫细胞摄取,并响应局部酶活性释放抗体。这种双重作用——阻断 IL‑23 驱动的炎症并增强促耐受信号——使炎性标志物接近正常水平,并恢复更健康的T细胞比例。
修复组织并预防长期损伤
在化学诱导的结肠炎小鼠中,接受 PrEXO‑a23 处理的动物体重下降较少,结肠更长、更健康,脾脏肿大也较轻,后者是全身性炎症的一个标志。显微检查显示肠道结构保存良好,上皮细胞间的连接更紧密,表明屏障功能得到修复。该疗法还帮助重塑肠道菌群,增加与肠道健康相关的细菌族群,减少与疾病相关的菌群。在一个模拟慢性结肠炎进展为结肠癌的更严重模型中,PrEXO‑a23 不仅缓解了持续性炎症,还完全阻止了肿瘤的发生,并抑制了表征纤维化的肠壁增厚与瘢痕形成。分子分析指向保护性 p53 信号通路的恢复——这一防癌关键节点对其抗癌效应至关重要。
迈向更智能、更持久的 IBD 护理
对非专业读者而言,核心信息是这项工作超越了单纯“降低”炎症的思路。通过将靶向递送、原位抗体释放和具有免疫平和功能的外泌体货物整合到一个微小载体中,PrEXO‑a23 在平息活动性疾病的同时帮助重新训练免疫系统以实现持久耐受。在小鼠中,这不仅带来了症状缓解,还防止了瘢痕形成和结肠癌——两种长期 IBD 最令人担忧的并发症。尽管在此类疗法进入临床病人之前仍需大量测试,该研究展示了受生物启发的纳米医学如何有朝一日为像 IBD 这样复杂的免疫疾病提供更精确、更持久的控制。
引用: Cao, J., Luo, R., Miao, R. et al. Engineered exosome nanovesicles for delivery of antibodies to treat inflammatory bowel disease. Nat Commun 17, 2737 (2026). https://doi.org/10.1038/s41467-026-69382-4
关键词: 炎性肠病, 纳米医学, 免疫耐受, 外泌体, 结直肠癌预防