Clear Sky Science · zh
淀粉样β纤维中的结构缺陷驱动二级成核
为何脑内蛋白的微小缺陷重要
在阿尔茨海默病及相关脑部疾病中,某些蛋白会聚集成长而细的线状结构,称为淀粉样纤维。这些纤维不仅是疾病的标志;它们还促进产生新的、高度有毒的蛋白颗粒,能够损伤脑细胞。本研究提出了一个简单而有力的问题:淀粉样纤维内部罕见的结构“缺陷”是否作为主要热点,引发有害的新生长?答案可能指出新的干预路径——通过靶向少数关键位点而不是整个蛋白表面来减缓或阻止这些疾病。 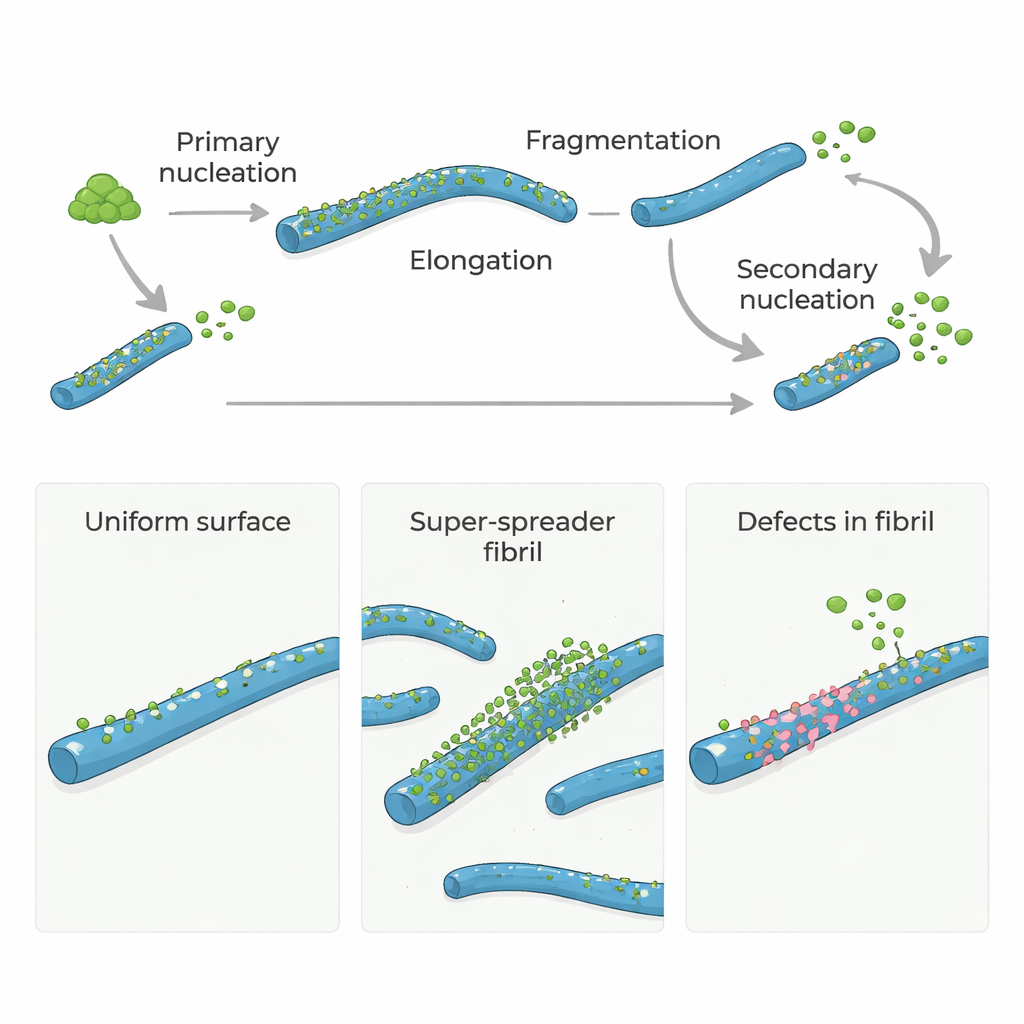
从静止的蛋白到失控的连锁反应
淀粉样-β(Aβ)蛋白是阿尔茨海默病的核心,在正常情况下这些蛋白不会很快自行聚集。起始阶段需要少量单体缓慢组装成最初的小纤维,这一步称为初级成核。一旦这些初始纤维存在,更多单体就会快速添加到纤维末端促其生长。更为关键的是,已有的纤维能在其表面触发新的纤维出现,这一过程称为二级成核。由表面驱动的这一环节可以在体系中迅速产生大量新纤维和小的有毒寡聚体,把缓慢的渗流变为失控的连锁反应。
所有纤维表面都同样危险吗?
许多模型假设淀粉样纤维的整个表面对二级成核具有相同的催化能力。然而,近期实验提示只有一小部分表面真正起作用。为探查这一点,作者使用了一种天然分子“伴侣”Brichos,已知其能阻断Aβ40和Aβ42(二种关键的淀粉样-β形式)的二级成核。通过仔细测量荧光标记的Brichos与纤维的结合量,他们发现Brichos结合很紧密但数量非常稀少:大约每100–150个Aβ分子才对应一个Brichos分子。然而,这种稀疏覆盖就足以抑制超过90%的二级成核,说明只有罕见的局部位点——而非整个表面——主导新有毒组装体的产生。
探查隐藏缺陷的作用
这些发现表明关键的成核位点可能是结构缺陷——纤维生长过程中形成的小不规则处,例如层错位或部分暴露的内核。为直接检验这一想法,研究者在两种不同条件下生长了Aβ40纤维。一组作为“对照”纤维,在典型的强过饱和条件下形成,这有利于快速生长并将缺陷陷入动力学俘获。另一组采用缓慢的温控退火方案制备:在非常低的有效驱动力、接近溶解度极限的条件下生长,错误结构可以在被锁定之前溶解或修复。高分辨率低温电子显微镜显示,两组纤维在整体形状和螺旋扭曲上基本相同,表明退火过程并未改变其基本形态。 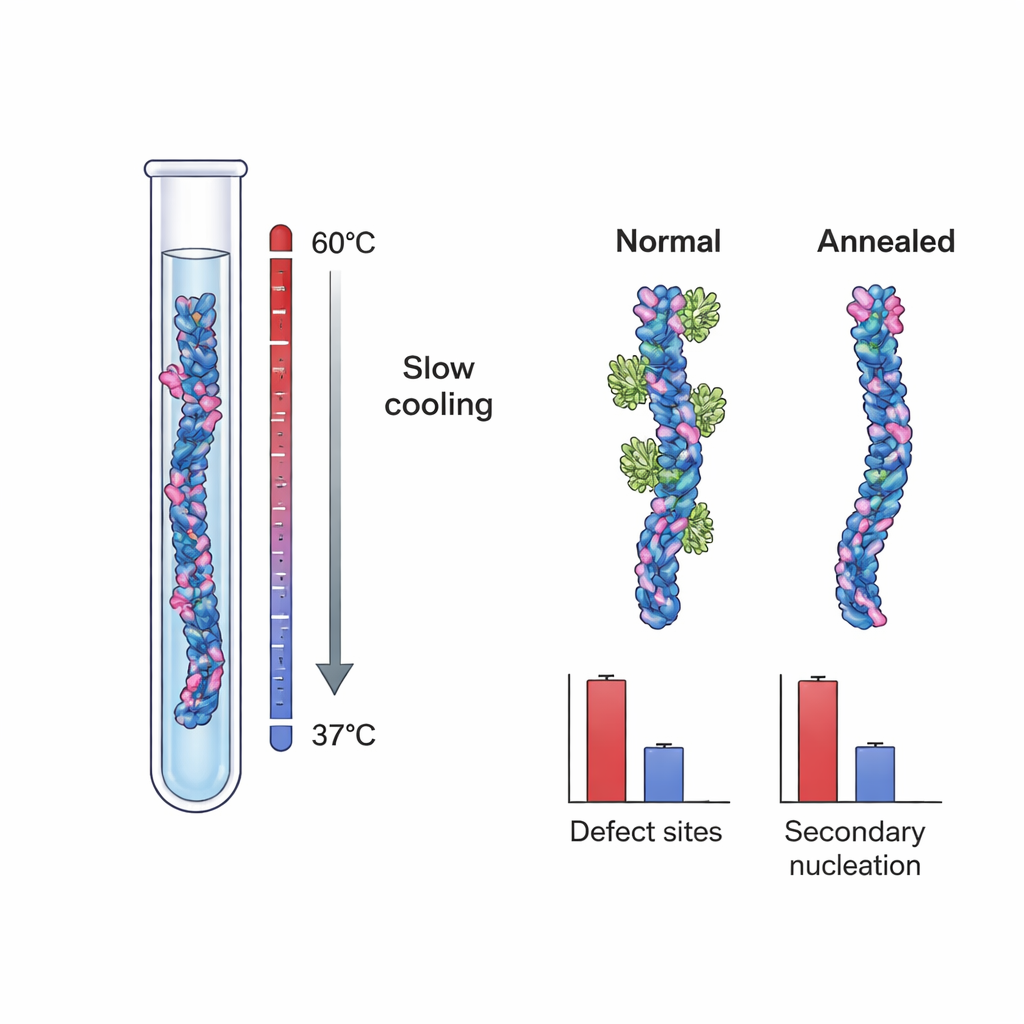
缺陷越少,危险生长位点越少
当团队测量Brichos与这两类纤维的结合时,发现了明显差异。对照Aβ40纤维约每~100个单体有一个Brichos结合位点,再次表明位点稀少但重要。退火纤维则约每~800个单体才有一个位点——位点频率几乎降低了90%。在将这些纤维作为“种子”加入新鲜Aβ40溶液的独立测试中,即使两组纤维的总质量一致,退火纤维触发新聚集的效果也远弱于对照纤维。详细的动力学建模显示,这种接种活性下降不能仅用纤维长度差异解释。相反,其数量级上与Brichos结合位点减少相一致,强烈支持了生长缺陷作为二级成核主要驱动力的观点。
具有治疗潜力的一般性原理
通过结合热力学论证、对早期工作的重新分析以及多个形成淀粉样体的蛋白之间的比较,作者认为罕见的生长缺陷很可能在许多体系的二级成核中起关键作用,而不仅限于与阿尔茨海默相关的Aβ。这些缺陷部分暴露了纤维紧密堆积的内核,为新的寡聚体和纤维提供了一个现成的支架,使其比在光滑表面上更容易形成。将这些缺陷视为主要元凶为药物设计开辟了新途径。与其尝试阻断纤维表面上的所有可能相互作用,不如针对性地屏蔽或修复这些稀少的缺陷位点,或减少导致其产生的条件。从实际角度看,这可能意味着降低脑中易形成淀粉样的蛋白的有效浓度,或设计受Brichos启发的分子,识别并中和由缺陷驱动的成核热点。如果成功,这类策略可切断有毒寡聚体的主要来源,减缓淀粉样相关疾病的进展。
引用: Hu, J., Scheidt, T., Thacker, D. et al. Structural defects in amyloid-β fibrils drive secondary nucleation. Nat Commun 17, 1933 (2026). https://doi.org/10.1038/s41467-026-69377-1
关键词: 淀粉样纤维, 阿尔茨海默病, 二级成核, 蛋白质聚集, Brichos 分子伴侣