Clear Sky Science · zh
生物分子凝聚体中的氧气枯竭以大分子密度为主导
活细胞内看不见的小口袋
在我们的细胞内部,许多化学反应依赖于稳定的氧气供应。但细胞并非简单的液体囊:它们含有称为生物分子凝聚体的微小类液滴状隔室,这些隔室在没有膜的情况下形成。本文提出了一个看似简单但影响深远的问题:这些液滴是否改变了细胞不同区域内的氧气可用性,如果改变,原因是什么?答案挑战了人们关于小分子在这些拥挤微环境中行为的主流观念。

没有围墙的液滴
生物分子凝聚体是由蛋白质和核酸组成的柔软、类液体簇,它们可以根据需要组装和解体。它们通过浓缩某些分子并排斥其他分子来帮助组织生物化学过程,尽管它们缺乏包围的膜。先前的研究表明,许多小代谢物和药物样化合物会被吸引进入这些液滴,通常是因为其内部与细胞的水性液相相比,表现得有点像油性溶剂。然而,氧气是一个特殊情况:它是一种小型气体分子,既为呼吸提供燃料,又能促成有害的副反应。凝聚体是富集还是耗竭氧气,因而可能影响酶的工作效率以及在这些液滴附近或内部发生的氧化损伤程度。
在微小隔室中测量氧气
为了探测凝聚体内部的氧气含量,研究人员构建了一个简单但可调的模型体系,使用人工设计的、柔软的蛋白质在盐溶液中容易形成液滴。研究人员首先通过离心生成大的宏观相,然后插入头发丝般细的电化学微电极,直接读取蛋白质富集相与蛋白质稀相之间边界处的氧气浓度。这些测量显示,当探针进入蛋白质致密相时氧气含量下降:液滴部分地排斥氧气,而不是吸收它。
用特殊染料点亮氧气
因为电极会干扰小液滴,研究团队转而使用磷光寿命成像显微镜,这是一种光学方法,利用某些特殊染料分子的发光寿命在氧气更多时更短的特性。通过追踪单个液滴内外的发光寿命,并仔细校正液滴环境如何改变染料的基线行为,他们可以在不物理扰动凝聚体的情况下推断氧气浓度。在一系列条件下,光学数据与电极测量结果一致:凝聚体内部的氧气始终低于周围溶液。使用粗粒度分子模型的计算机模拟支持了这一图景,显示氧气在致密蛋白质区域内停留的时间相对较短。
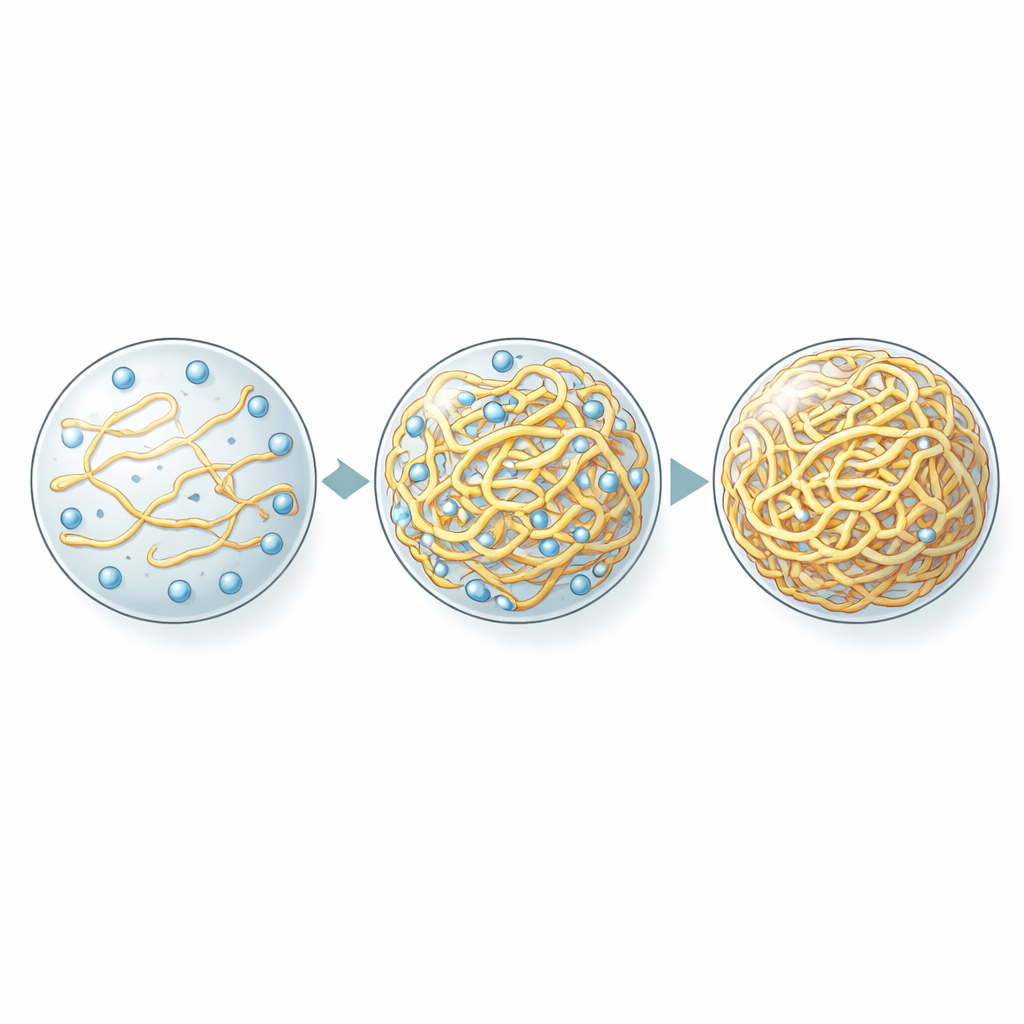
决定氧气水平的是密度,不是“油腻”
控制氧气摄取的明显嫌疑者是疏水性——液滴内部的“油腻程度”——此前已被认为是许多其他小分子如何在凝聚体中分配的关键因素。为检验这一点,作者系统性地改变蛋白质序列以同时改变重复单元数量及其疏水特性,然后测量所得液滴内的氧气含量。出人意料的是,氧气水平并不随液滴的油性或水性而变化。相反,它们与致密相中蛋白质的填充程度呈强烈且反向的相关性。形成更拥挤凝聚体的变体含氧量更低,即便它们总体上不那么疏水。其他小型油溶性染料则表现不同:它们仍然偏好更疏水的液滴,这证实了氧气打破了通常的规则。
关于纳米尺度氧气梯度的新视角
这些发现引出了关于凝聚体如何塑造其化学环境的修订观点。对于那些不会强烈粘附于支架蛋白的小分子来说,大分子的纯粹密度成为主导因素:蛋白质占据的体积越多,留给溶解氧的空间就越少。这意味着细胞可以仅通过形成或溶解凝聚体,或改变这些液滴的紧密程度,在纳米到微米尺度上产生氧气梯度。在实际层面上,这项工作表明无膜细胞器可以通过一种物理的拥挤效应,而非特定的化学结合,微妙地调节附近反应的氧气可用性——可能加速某些反应、减慢其他反应,或保护敏感组分。
引用: Garg, A., Brasnett, C., Marrink, S.J. et al. Oxygen depletion in biomolecular condensates is dominated by macromolecular density. Nat Commun 17, 2603 (2026). https://doi.org/10.1038/s41467-026-69376-2
关键词: 生物分子凝聚体, 氧气分配, 大分子拥挤, 相分离, 细胞微环境