Clear Sky Science · zh
STING与TOX协同抑制HO-1表达,触发肿瘤浸润CD8+ T细胞铁死亡并导致免疫治疗耐受
这项研究对癌症治疗的重要性
现代癌症免疫疗法依赖释放心体内的杀伤性T细胞,但许多肿瘤仍能使这些细胞失效。本研究揭示了肿瘤利用的一种隐藏在CD8+“杀手”T细胞内的自毁开关,并展示了关闭该开关如何显著增强免疫治疗的效果。
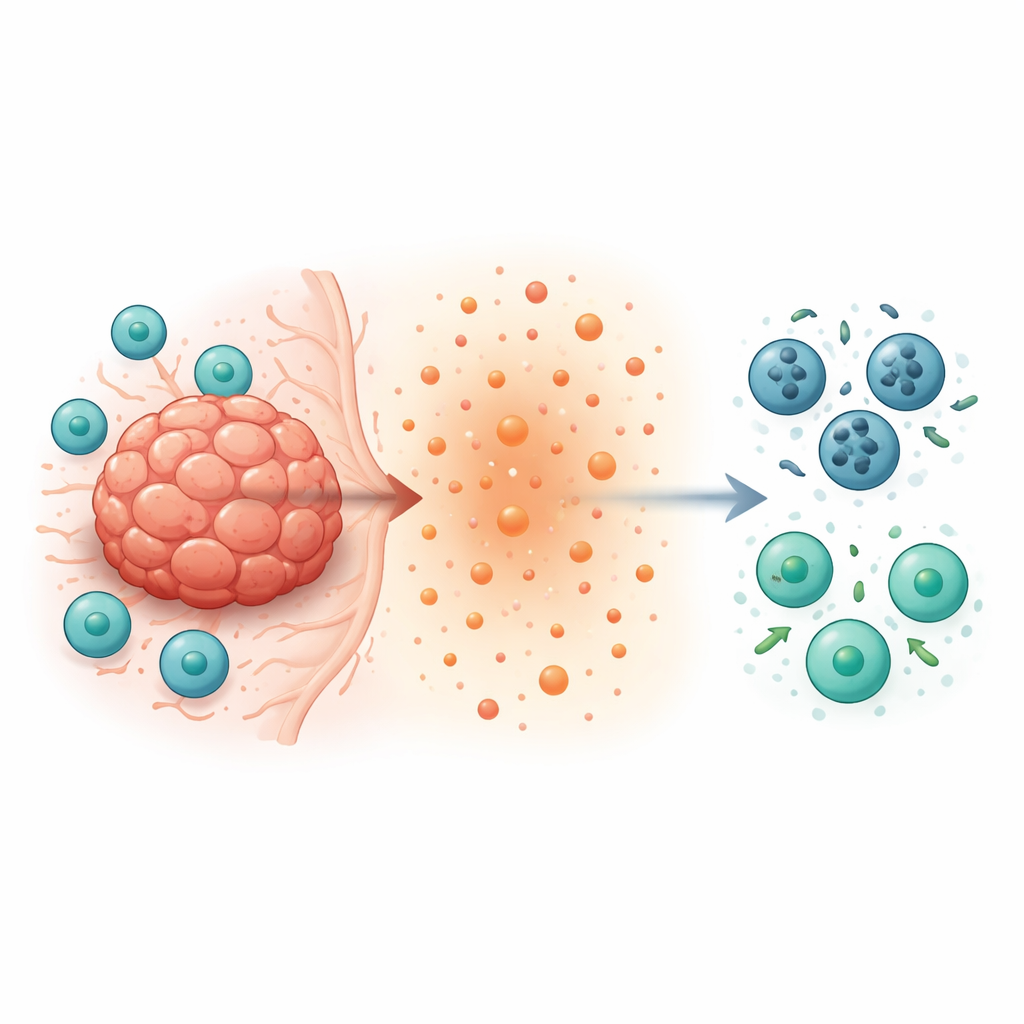
肿瘤杀伤性T细胞内的隐匿死亡通路
在肿瘤内,CD8+ T细胞本应追踪并清除癌细胞,但它们常常稀少、迟滞且寿命短。作者将注意力集中在T细胞内的两个分子——作为DNA损伤传感器的STING和与T细胞衰竭相关的蛋白TOX。他们构建了在CD8+ T细胞中缺失STING、TOX或两者的老鼠模型,并移植多种肿瘤。出人意料的是,T细胞缺失STING或TOX的老鼠更能清除肿瘤:肿瘤生长更慢,肿瘤中CD8+ T细胞显著增多,这些T细胞分泌更多的杀癌分子,如干扰素-γ和颗粒酶B。这些发现指向一种在肿瘤内悄然破坏T细胞的内部程序。
铁驱动的细胞死亡如何削弱免疫力
通过分析肿瘤浸润T细胞的基因活动,研究者发现肿瘤内的正常T细胞被预设为一种特定形式的细胞死亡——铁死亡。与凋亡不同,铁死亡由铁过载和细胞膜脂质损伤累积触发。在暴露于肿瘤环境的普通CD8+ T细胞中,促进铁积累和脂质损伤的基因被激活,而保护性基因被下调。相反,缺失STING或TOX的T细胞呈现相反模式:它们表达更多保护性酶HO-1和GPX4,铁含量更低,脂质过氧化减少,线粒体更健康,并抵抗铁死亡。体外实验证实,化学阻断铁死亡可保持正常T细胞存活,而删除STING或TOX则使T细胞天然耐受铁死亡。
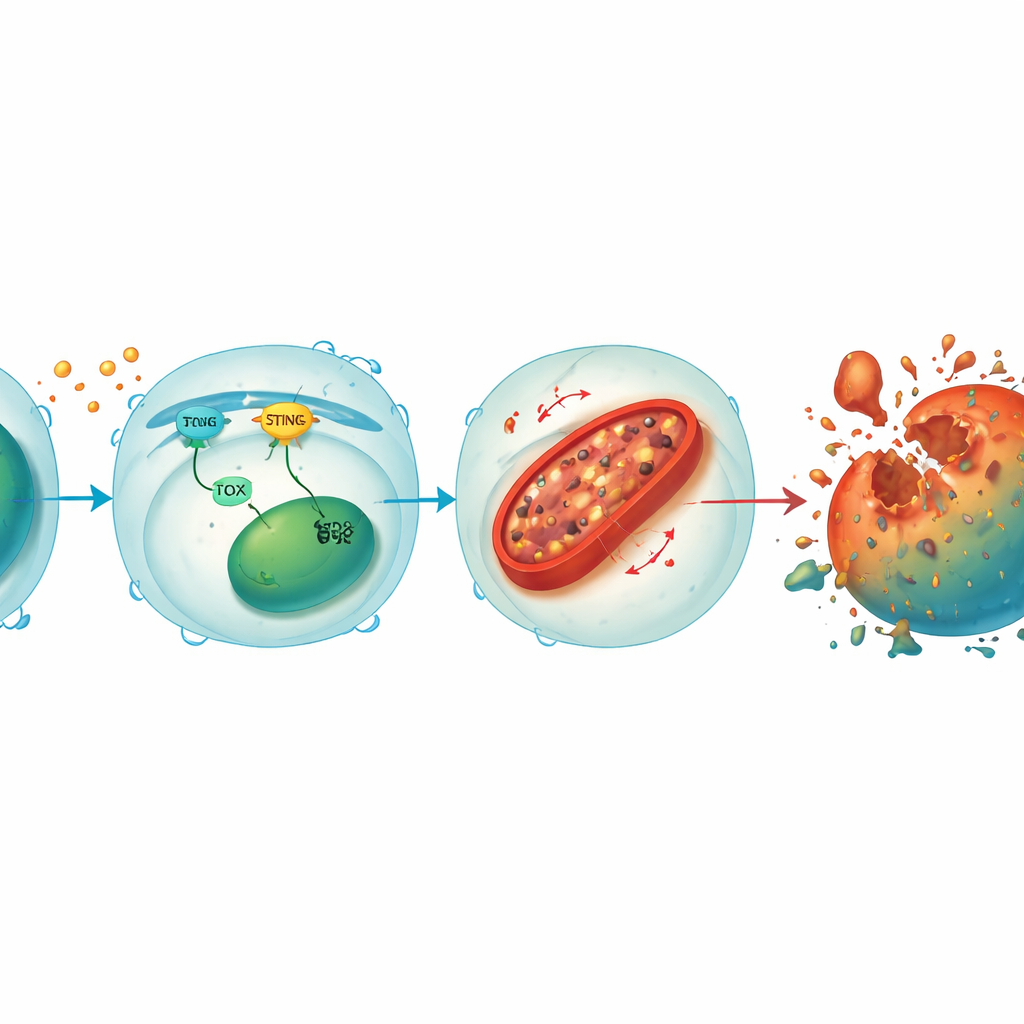
将应激信号与线粒体损伤相连的环路
进一步研究表明,STING和TOX在CD8+ T细胞内形成一个相互增强的环路。当肿瘤或病毒信号激活STING时,会触发下游因子促进TOX表达,而TOX又有助于维持STING活性。二者共同抑制HO-1这一通常用于控制细胞内铁稳态的酶。HO-1被压低后,铁在细胞的能量工厂——线粒体中积聚,导致活性氧增多和膜脂质氧化。线粒体受损耗尽能量产生,最终推动T细胞走向铁死亡。将STING或TOX恢复到敲除的T细胞会重新引发铁过载和细胞死亡,而进一步降低HO-1会使即便受保护的T细胞再次变得脆弱,凸显HO-1在该破坏性通路中的关键制动作用。
肿瘤产生的乳酸如何扣下扳机
肿瘤微环境中富含乳酸,这是癌细胞代谢改变的副产物。研究显示,乳酸不仅是代谢废物——它主动帮助翻转T细胞的铁死亡开关。相比其他细胞,CD8+ T细胞对乳酸尤为敏感。乳酸通过特定转运子进入细胞,导致铁积累、线粒体缩小、线粒体DNA丢失以及更多氧化损伤。与此同时,乳酸增强STING和TOX活性并进一步抑制HO-1。缺失STING或TOX的T细胞对乳酸诱导的损伤具有更强的抗性。在小鼠中用药物(AZD3965)阻断关键乳酸转运子可保护CD8+ T细胞免受铁死亡,增加其在肿瘤内的数量并减缓肿瘤生长,类似于在T细胞中基因性删除STING带来的益处。
将脆弱性转化为治疗优势
这些机制性见解具有实际意义。研究者在采用过继细胞疗法(向小鼠输注体外激活的T细胞)时发现,工程改造为缺失STING或TOX的T细胞比正常T细胞产生更强的肿瘤控制效果。此外,将这些“抗铁死亡”T细胞与现有治疗手段(如PD-1或TIM-3免疫检查点抑制剂、顺铂化疗或STING激活药物)联合使用,较任何单一疗法均产生显著更好的肿瘤缩小效果。最后,在宫颈癌患者的肿瘤样本中,肿瘤浸润淋巴细胞中TOX较高且HO-1较低与更差的生存率相关,表明该通路也影响人体临床结局。
对未来癌症护理的意义
简言之,本研究揭示肿瘤可以通过驱动一种铁催化的细胞死亡,让我们最有力的抗癌T细胞从内到外“生锈”。乳酸–STING–TOX回路削弱了HO-1的保护作用,损害线粒体并导致铁死亡,削薄了有效CD8+ T细胞的数量。扰乱该回路——通过构建缺失STING或TOX的T细胞、增强HO-1或阻断乳酸进入——可使T细胞存活、保持活力并继续攻击癌细胞。这项工作为下一代免疫疗法指明了方向,建议将代谢与基因调控的T细胞工程与现有药物结合,以克服耐受并提供更持久的癌症控制。
引用: Zhu, Q., Zhang, Jb., Nie, Cp. et al. STING synergizes with TOX suppressing HO-1 expression to trigger ferroptosis in tumor-infiltrating CD8+ T cell and immunotherapy resistance. Nat Commun 17, 2543 (2026). https://doi.org/10.1038/s41467-026-69350-y
关键词: 癌症免疫治疗, CD8 T细胞, 铁死亡, 肿瘤微环境, STING TOX HO-1通路