Clear Sky Science · zh
通过电子共振激发拉曼散射实现无荧光单分子显微成像
观察单个分子的全新方式
能够直接观察单个分子的活动已改变了生物学和医学,从追踪蛋白在细胞内的运动到读取 DNA 序列。如今,这通常依赖发光的荧光标签,但当存在多种不同类型时,这些标签的光谱会互相重叠而模糊不清。本研究引入了一种不依赖发光的新型显微对比机制。它不是“看光”,而是“听”经过专门设计的分子的细微振动,为以单分子水平更清晰、更详尽且更灵活地成像生命体打开了道路。 
荧光染料为何到了极限
荧光染料一直是现代显微镜的主力。它们亮度高、可特异性标记目标分子,灵敏度足以显现单个蛋白或 DNA 链。然而,每种荧光染料的发射覆盖相对宽的颜色范围。当需要同时成像许多不同靶标时,这些宽谱会互相重叠,使得难以区分不同分子。为了解决这一问题,研究人员常要反复进行染色和洗涤循环,这既耗时又可能扰动脆弱样品。
用分子振动取代光学发光
每种分子也有独特的振动模式,像是原子如何抖动和伸缩的指纹。这些振动可以通过拉曼或红外光谱等技术探测,当光与振动的化学键相互作用时会产生极微小的频移。与荧光光谱相比,振动指纹极其狭窄,因此理论上可以同时区分数十种不同分子。问题在于振动信号本身很弱,早期方法要么依赖金属纳米结构来增强信号,要么仍借助荧光来读出效应,从而带回了相同的背景问题。
一种无荧光的拉曼信号增强方案
作者基于一种称为电子共振激发拉曼散射(ER-SRS)的方法,该方法通过将一束激光的颜色与分子的电子跃迁匹配,并使两束激光之间的色差对应特定振动,从而显著放大振动信号。早期的 ER-SRS 遇到的难题是,放大拉曼信号的同一条件也会产生很大的不需要的电子与荧光背景。为了解决这一点,团队从两方面入手:他们开发了一套具有两束可独立调谐激光的系统,并创造了一类在近红外区有强吸收但几乎不发荧光的新型分子探针。这些“拉曼放大非荧光分子探针”(RANMPs)以一个共轭核心为基础,携带四个富含振动的腈基,提供强且锐利的拉曼指纹。
设计安静但响应灵敏的分子探针
关键的化学技巧在于让 RANMP 分子将能量快速引导到不发光的三重态,而不是以荧光再发射出去。结构中如硫等重原子可以提高这种能量转移速率,有效地猝灭荧光,同时仍允许激光驱动振动模式。量子化学计算指导了设计,使得吸收波长与腈基振动与激光的调谐范围相匹配。通过精细调节分子结构,研究者可以移动振动频率与强度,制造出几种相关但各有微小差别的探针,具有不同且彼此紧密分布的拉曼指纹。在优化的 ER-SRS 条件下,这些分子产生的振动信号比早期工作中使用的标准荧光染料强数百倍,同时背景远低得多。
观测单个颗粒与单个分子
具备这些要素后,团队展示了该方法的能力。首先,他们将 RANMP 染料装入称为高分子点(polymer dots)的小聚合物纳米颗粒中,进一步浓缩探针并抑制任何残余荧光。利用 ER-SRS,他们在溶液中成像到单个纳米点,并区分出两种腈基振动仅有微小差别的探针,实际上在单次扫描中实现了双色单颗粒成像。随后,他们将探针稀释至薄塑料膜中仅有数个分子的水平。通过保护样品免受损伤并调整激光功率与时序,他们记录到清晰、接近衍射极限的点状信号,这些点以单阶跃方式闪灭,体现了单分子检测的标志性特征。他们还证明,当两束激光的时序或频差偏离腈基振动时这些点消失,而在恢复时再次出现,从而确认信号确实来源于特定化学键的振动。 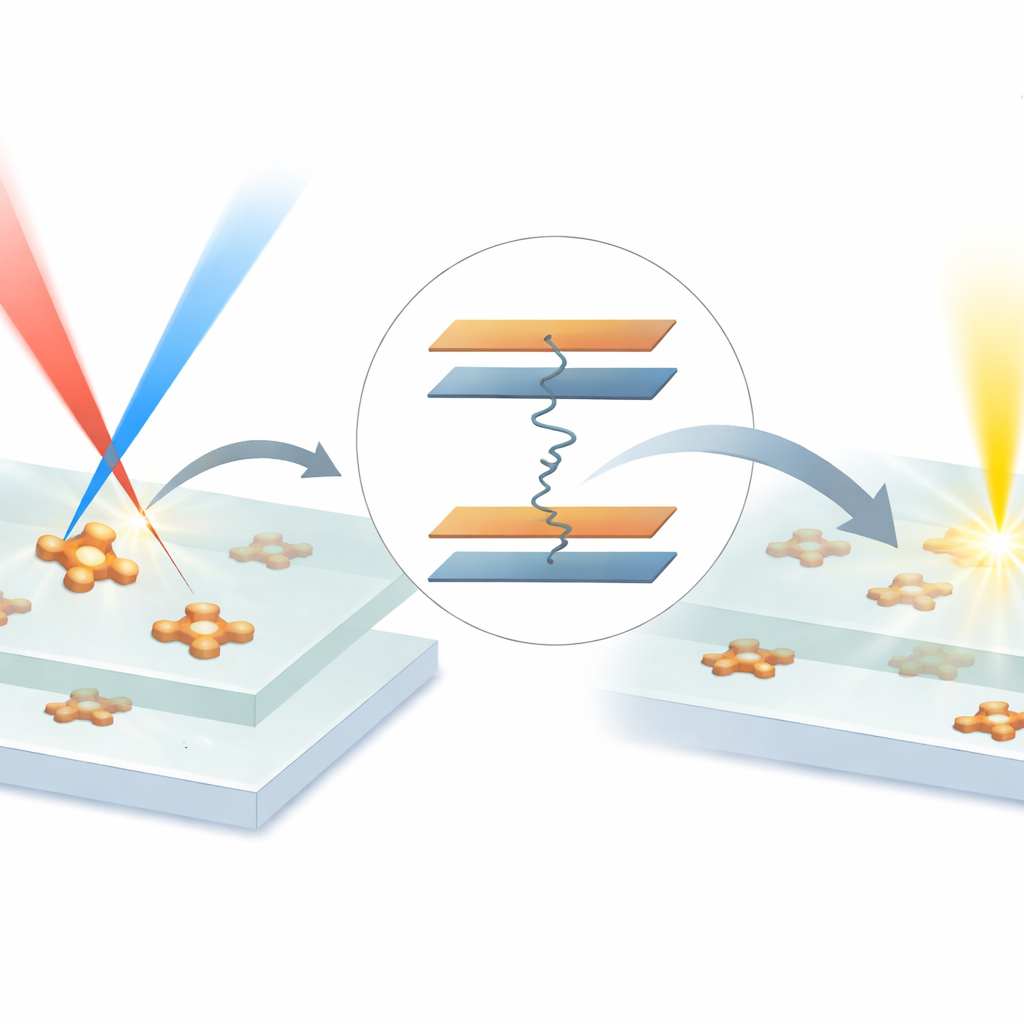
这对未来成像的意义
用通俗的话说,这项研究证明了可以仅凭分子的振动指纹来观察并区分单个分子,而无需依赖发光。由于振动线窄且可通过化学设计进行调节,这为同时标记许多不同靶标而几乎无重叠提供了强有力的途径。探针的非发光特性也降低了背景噪声,并有助于更容易地向组织深处成像,在那里散射的荧光通常会占主导地位。尽管还需进一步工作以将这些探针适配到活细胞并扩展颜色组合,ER-SRS 配合 RANMPs 指向了一个前景:可以以前所未有的清晰度和多重标记能力绘制复杂生物样本的单分子图谱。
引用: Oh, S., Eom, Y., Kim, H.Y. et al. Fluorescence-free single-molecule microscopy via electronic resonance stimulated Raman scattering. Nat Commun 17, 2720 (2026). https://doi.org/10.1038/s41467-026-69348-6
关键词: 单分子显微镜, 激发拉曼散射, 振动成像, 非荧光探针, 多重生物成像