Clear Sky Science · zh
Seq-Scope-eXpanded:超越光学分辨率的空间组学
以更清晰的细节观察细胞
我们的身体由无数微小细胞构成,每个细胞内都在进行着通常即便借助强力显微镜也难以直接可见的活跃过程。本文介绍了 Seq-Scope-X——一种让研究者以前所未有的清晰度放大组织内部活动的技术,能够在细胞内外的精确位置绘制出哪些基因和蛋白处于活跃状态。这一层次的细节有可能改变我们对发育、免疫系统以及癌症或肝损伤等疾病的研究方式。
为什么要在原位绘制分子分布?
细胞并非孤立工作:它们生活在社区中、构成层次并根据所处位置分化。传统的基因测序方法会将组织解离,从而丢失空间语境。近来的“空间组学”工具则可保持分子的原位信息,但存在权衡。基于成像的方法可见极细的结构,但通常只能追踪有限的基因集合;基于测序的方法可以一次读取几乎所有基因,却往往模糊细微特征,常将信号摊到几个微米范围——这比许多亚细胞结构还大。作者们旨在缩小这一差距:既保留测序的无偏丰富读出,又达到甚至超越现代显微镜的分辨率。
通过拉伸组织突破光学极限
Seq-Scope-X 的核心想法看似简单:温和地放大组织本身,使原本纳米级的结构变得更易分辨。研究团队首先将 RNA 分子或与抗体连接的特殊 DNA 标签固定在围绕组织切片构建的柔软水凝胶中。随后他们消化掉原始组织,并在含盐溶液中使凝胶膨胀,物理上将一切放大约三倍,同时尽量保持相对位置不变。将这种膨胀的凝胶覆盖到涂有捕获探针的超高密度测序芯片上,通过精确加热的方式,将被固定的分子从凝胶中释放并重新连接到芯片,随后对芯片进行测序以揭示每个微小坐标处存在的基因或蛋白。 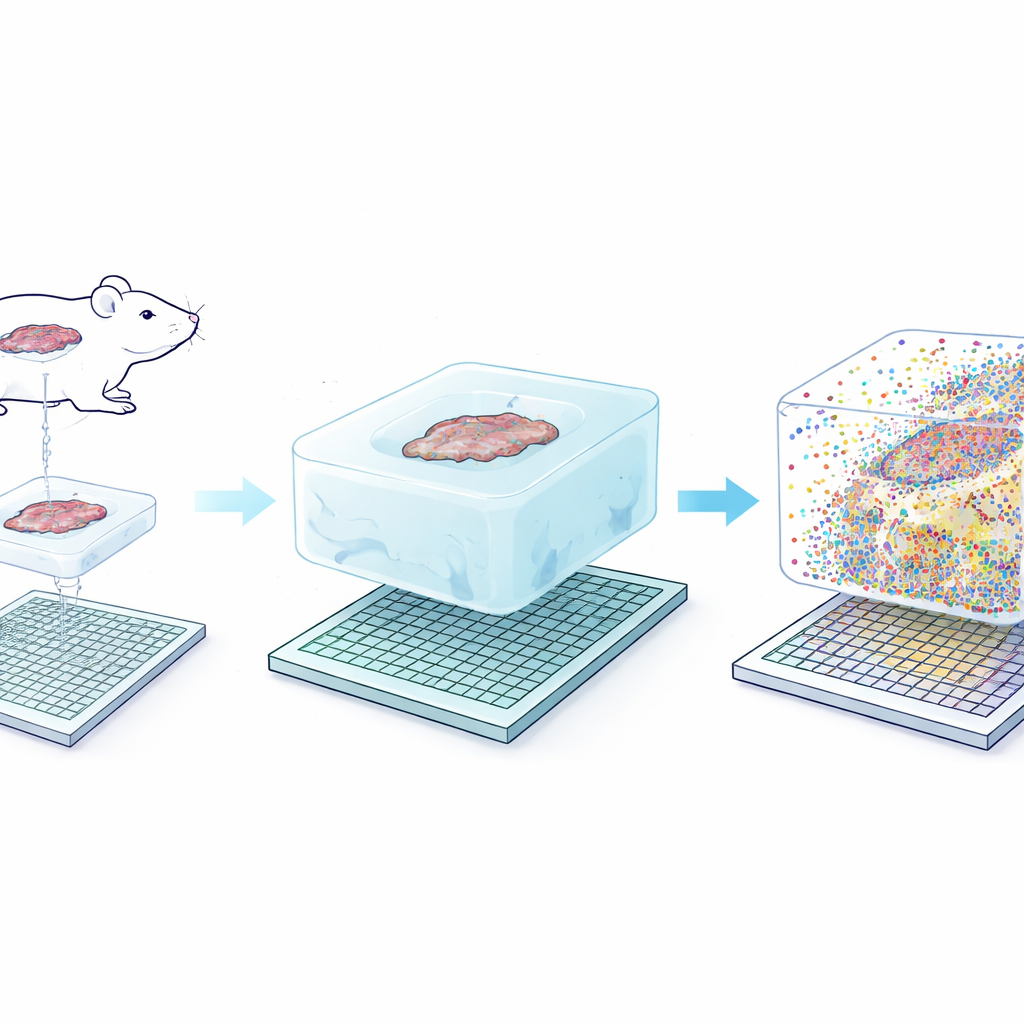
从模糊的细胞到亚细胞级图谱
当研究者将 Seq-Scope-X 应用于小鼠肝脏时,发现该方法将空间分辨率从约 0.6 微米提高到约 0.2 微米,并使每平方毫米可测位置的数量几乎增加了十倍。实用上,以前看起来像模糊信号团块的区域现在分辨成清晰的单个细胞轮廓。更显著的是,尚未完全加工的 RNA(未剪接)群落紧密对齐于细胞核中心,而成熟的 RNA(已剪接)则分布在周围细胞质中。这使作者能够仅凭 RNA 就勾画出细胞边界,并将近乎每个肝细胞的核与细胞质的基因读数区分开来——这是此前基于测序的方法仅能略有暗示的能力。
具有“分裂性格”的细胞
凭借这种新的清晰度,团队发现了肝细胞内一种意想不到的分子“二重生活”形式。沿肝小叶从门脉侧到中央静脉侧的已知梯度,肝细胞在不同区域承担不同的代谢任务。Seq-Scope-X 显示,在许多细胞中,核内的基因模式并不与周围细胞质的模式一致。约三分之一的肝细胞表现出核型与一个分区对齐、而细胞质型与相邻分区对齐。独立的成像方法,包括 MERFISH 和单分子 RNA 荧光分析,证实单个转录本可集中在核内或细胞质中。综合这些发现,提示肝细胞可以动态地改变它们的代谢角色:细胞核为未来的状态做准备,而细胞质则反映当前状态。 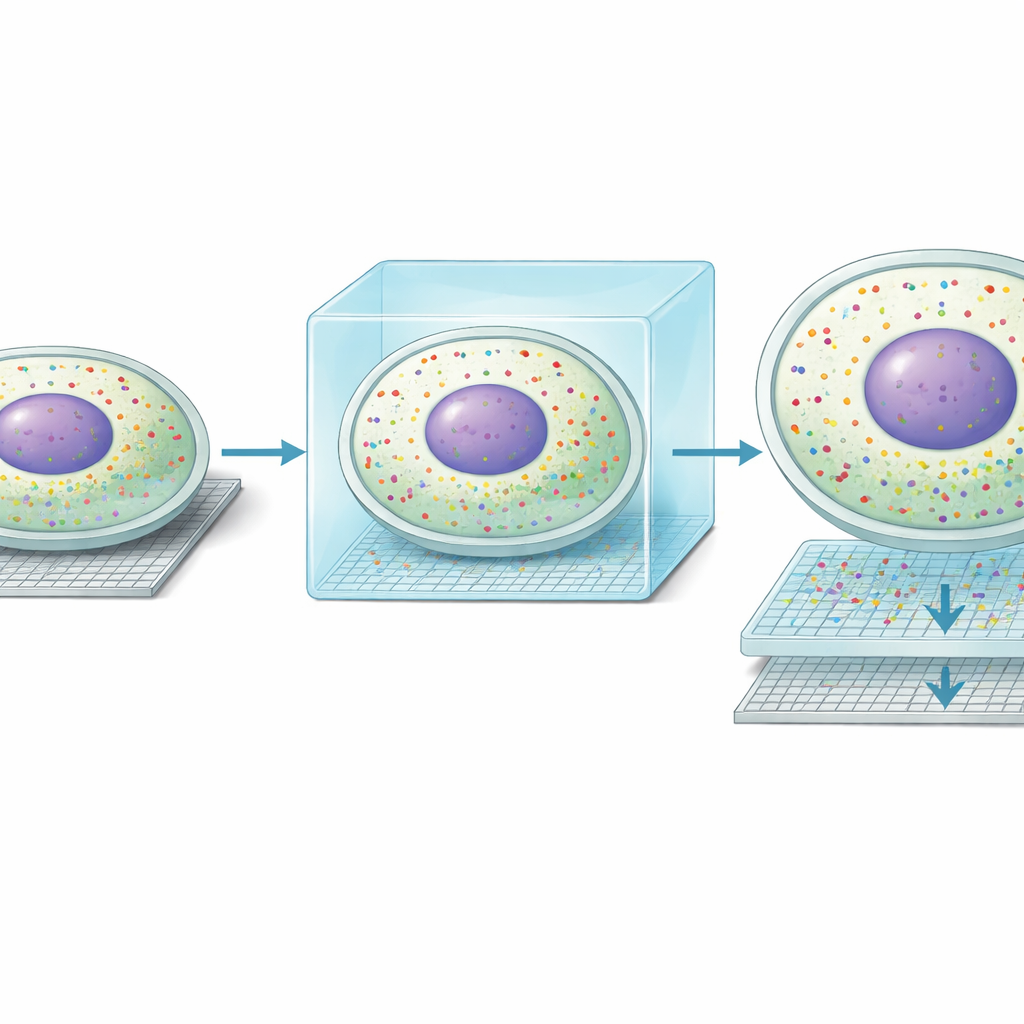
超越肝脏:大脑、肠道与免疫组织
作者随后测试了 Seq-Scope-X 在其他器官中的适用性。在大脑中,该方法清晰地区分了不同类型的神经元和支持细胞,并揭示了围绕细胞核的亚细胞 RNA 模式。在结肠中,它分辨出不同的杯状细胞亚型和沿隐窝至表面的结肠细胞层级,再次捕捉到核信号。也许最引人注目的是,团队通过在小鼠脾脏和人类扁桃体中使用带有 DNA 条码的抗体将该方法扩展到蛋白质检测。Seq-Scope-X 能在单细胞分辨率下同时绘制一百多种细胞表面标志,区分紧密聚集的 T、B 细胞亚群和髓系细胞。通过切换到更可膨胀的凝胶化学体系,他们将有效分辨率推向真实的纳米尺度,同时在足够保留组织结构的基础上实现详细映射。
对未来的意义
Seq-Scope-X 表明,在测序前对组织进行物理放大可以克服长期存在的分辨率限制,在实现近显微镜级细节的同时仍能一次读取数千个基因或蛋白标签。对非专业读者而言,这意味着科学家现在可以构建“分子地图”,不仅标记细胞的位置,还揭示每个细胞不同部分内部正在发生的事情。这类图谱可帮助解释组织如何对损伤作出反应、免疫细胞在淋巴器官和肿瘤中的组织方式,或细胞内部细微变化如何预示疾病。尽管仍需在扩大覆盖范围和改进某些染色面板方面进行进一步改良,Seq-Scope-X 为观察构成健康与疾病基础的微观景观打开了一扇强有力的新窗口。
引用: Anacleto, A., Cheng, W., Feng, Q. et al. Seq-Scope-eXpanded: spatial omics beyond optical resolution. Nat Commun 17, 2564 (2026). https://doi.org/10.1038/s41467-026-69346-8
关键词: 空间转录组学, 组织膨胀, 单细胞组学, 空间蛋白组学, 肝脏分区