Clear Sky Science · zh
微生物来源的 IPA 通过调节肠道 HMGCS2 介导的生酮作用来保护结肠炎并促进黏膜愈合
肠道细菌为何对受损肠道至关重要
当肠道内壁受损——例如在炎性肠病(IBD)或强烈医疗处理后——机体必须迅速修复这一“内皮肤”,以防有害物质泄漏入血。该研究揭示了一种由有益肠道细菌产生的单一分子如何帮助肠道自我修复,提示了在不全面抑制免疫系统的情况下治疗慢性肠疾的新路径。
来自友好微生物的有益信号
研究人员首先比较了 IBD 患者与健康志愿者的粪便化学指纹,并在多种小鼠结肠炎模型中进行了分析。在数百种分子中,有一种脱颖而出:吲哚-3-丙酸(IPA),这是某些肠道细菌将饮食氨基酸色氨酸分解后产生的产物。与健康对照相比,克罗恩病患者和患结肠炎的小鼠体内的 IPA 水平始终较低。这表明 IPA 的缺失可能是肠道黏膜发炎并未能修复时出错的一个环节。
加强肠道的保护屏障
为检验 IPA 是仅作为疾病标志物还是确实具有保护作用,团队在诱发多种肠损伤(包括化学性结肠炎和放射损伤)之前给予小鼠 IPA。接受足量 IPA 的小鼠结肠更长、更健康,镜检下炎性改变更少,黏液层更厚、细胞连接更紧密。它们血清中炎性标志物外泄更少、杯状细胞更多(杯状细胞负责产生保护性黏液)。重要的是,即使在无菌小鼠(缺乏常驻微生物组)中也观察到这些益处,表明一旦存在 IPA,它可以直接作用于肠道上皮而无需其他微生物参与。
用一种特殊能量供养干细胞
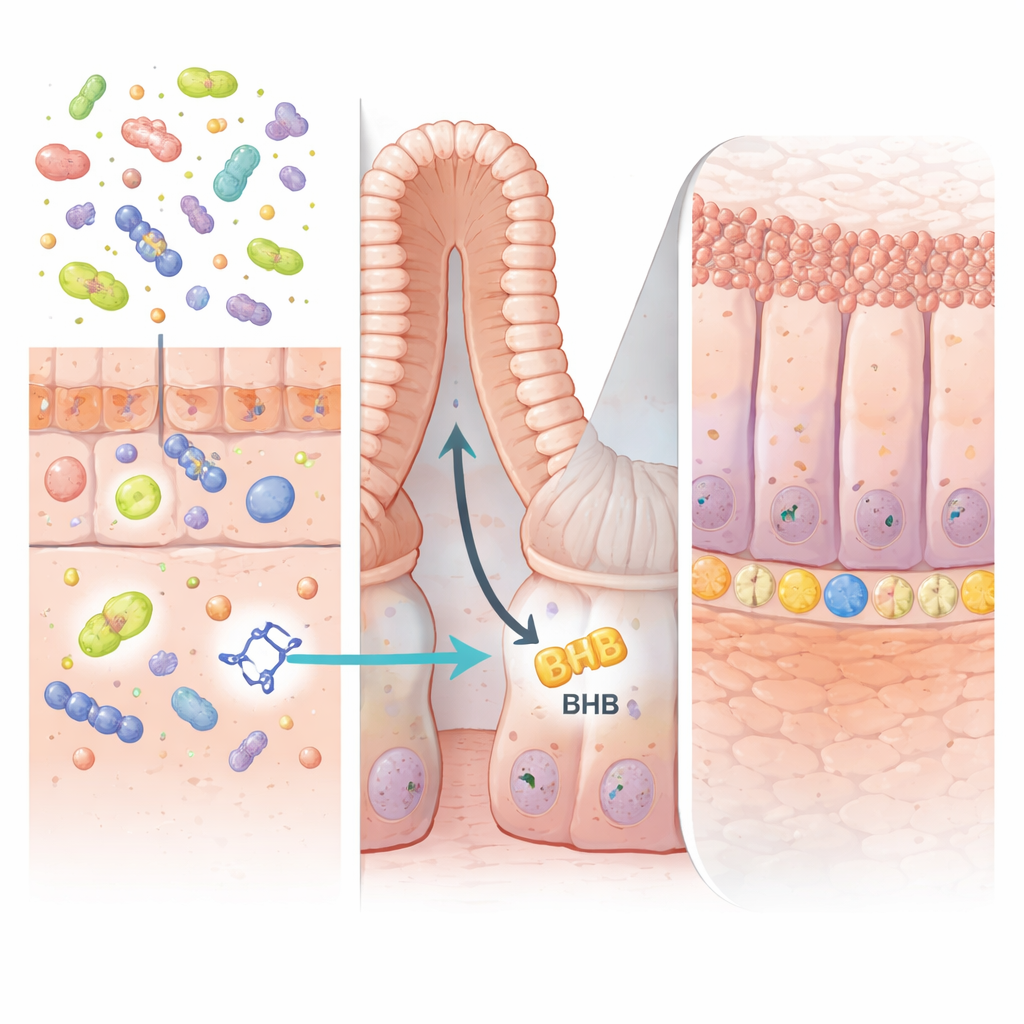
IPA 的作用关键位于肠道“隐窝”深处——干细胞所在并不断更新上皮的微小口袋。作者表明,IPA 在肠上皮细胞中激活一种名为 PPARα 的蛋白。继而,这提升了一种名为 HMGCS2 的酶的产生,HMGCS2 驱动生酮作用——生成高能分子β-羟基丁酸(BHB)的过程。肠壁内 BHB 的升高刺激了 LGR5 阳性的干细胞扩增并更快地再生受损组织。当小鼠肠道细胞中选择性缺失 HMGCS2 酶或 PPARα 时,IPA 无法再增强干细胞活性或对结肠炎提供保护,证实了该产酮通路的必要性。
从细菌工厂到人类组织
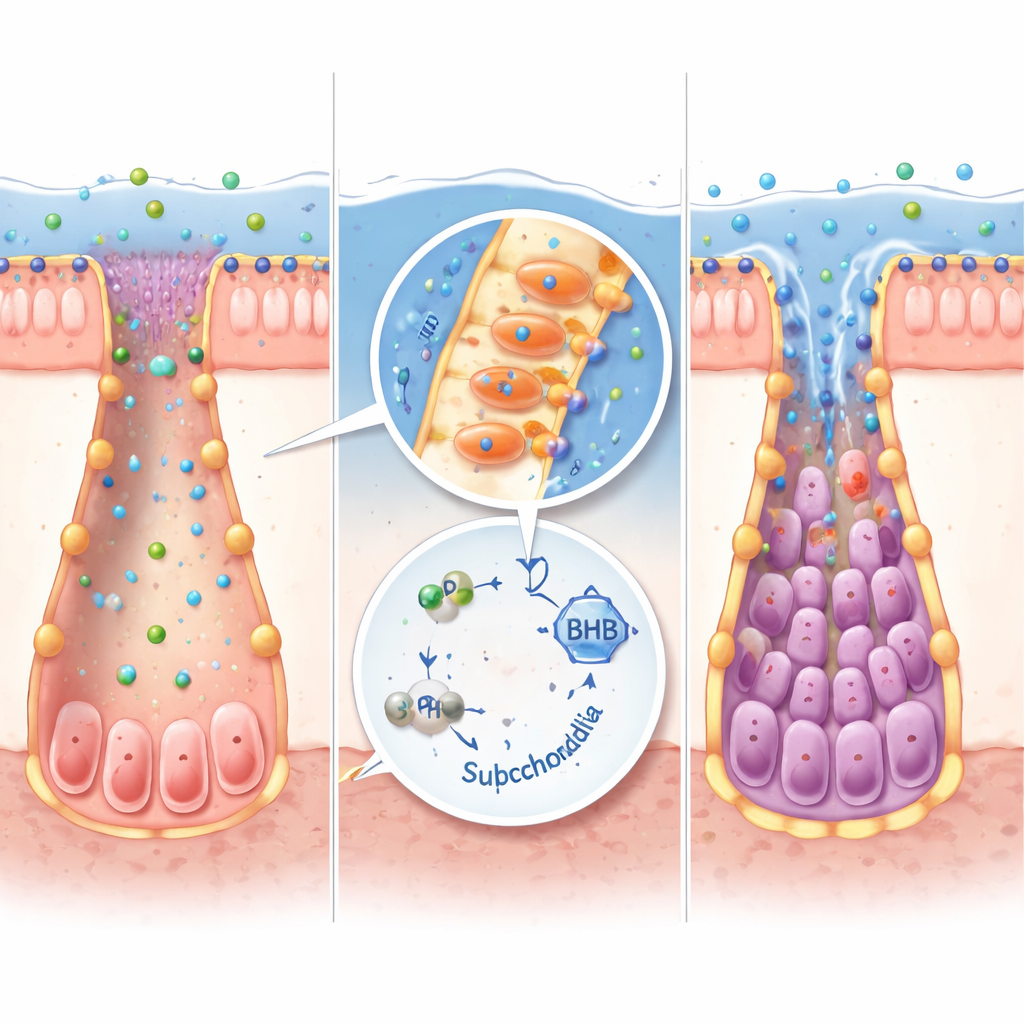
并非所有肠道细菌都能产生 IPA。通过重新分析大型微生物组数据集,研究人员识别出 Peptostreptococcus russellii 为一种关键的 IPA 生产者,在多个 IBD 队列中该菌丰度减少。在体外培养中,这种细菌能高效地将色氨酸转化为 IPA。当无菌小鼠被定植 P. russellii 后,其体内 IPA 水平上升,产酮相关基因被激活,干细胞标记增加,与接受普通微生物移植的小鼠相比结肠炎严重程度下降。同样的 IPA–酮体通路在由小鼠和人类组织培养的微型肠类器官中也可运行,在这些模型中加入 IPA 或 BHB 有助于干细胞在炎性损伤后恢复,同时降低促炎信号。
这对未来治疗可能意味着什么
综合而言,这项工作描绘了一条简单而有力的事件链:某些肠道细菌将食物中的色氨酸转化为 IPA;IPA 在肠细胞中触发一种代谢开关;该开关提升 BHB 的生成;而 BHB 反过来唤醒重建肠道内壁的干细胞。对于 IBD 患者或其他损伤肠道屏障的病症,通过饮食、定向益生菌或设计药物恢复 IPA 或安全模拟其作用的疗法,可能在不广泛抑制免疫的情况下促进真正的黏膜愈合。尽管还需在患者中开展更多研究,这条微生物—代谢物—干细胞轴为从内而外修复肠道提供了一个有希望的新思路。
引用: Zhang, Y., Tu, S., Shao, X. et al. Microbiota-derived IPA protects against colitis by regulating intestinal HMGCS2-mediated ketogenesis to facilitate mucosal healing. Nat Commun 17, 2437 (2026). https://doi.org/10.1038/s41467-026-69341-z
关键词: 肠道微生物组, 肠道干细胞, 炎性肠病, 微生物代谢产物, 黏膜愈合