Clear Sky Science · zh
使用磷酸化蛋白质组学和激酶-底物相互作用对EGF信号通路推断进行基准测试
这项工作在实验室之外的重要性
我们的细胞持续接收并响应来自周围环境的信号。其中最重要的信号之一是表皮生长因子(EGF),它帮助控制细胞的生长、分裂与存活。当这一通信系统失常时,可能驱动癌症和其他疾病。本研究提出了一个看似简单但影响深远的问题:如果我们利用当今强大的测量技术与计算模型,能否比教科书上的示意图更好地理解EGF信号通路,程度有多大?
从直线式到更贴近现实的电路图
传统的“信号通路”常被画成整齐、几乎线性的蛋白质链,从细胞表面将信息传递到细胞核。这些图谱是在几十年中通过缓慢、针对性的实验构建的,每次只能研究少数蛋白。作者认为,这导致我们形成了狭窄的“路灯下”视角:对那些易于研究的少数蛋白我们知道很多,但对真实细胞中可能存在的更广泛连接网络了解甚少。
一次监听数千个分子开关
为超越这种有限视角,团队使用了磷酸化蛋白质组学——一种质谱技术,可以在一次实验中跟踪成千上万个位点上的微小化学标签(磷酸基)。这些标签由称为激酶的酶添加,作为信号传递的快速开—关开关。研究者首先通过整合三类信息构建了迄今最全面的“谁能磷酸化谁”图谱:文献中的人工整理结果、基于蛋白序列的人工智能预测模型,以及大规模实验筛选得到的激酶偏好性数据。这大幅扩展了已知或疑似激酶—底物关系的覆盖范围,从可测位点的大约5%提升到约70–80%。
在大量实验中对应激EGF信号进行压力测试
接着,他们聚焦于EGF应答——一个经典通路,也是肺、乳腺、皮肤和脑部癌症中的重要参与者。研究组将三组最先进的已发表数据与三组新的、在肾源性细胞中进行的深度时间分辨测量结合起来,还包括两个使用不同刺激的对照研究。这些实验每个数据集中测量了超过40,000个磷酸化位点,并追踪它们在EGF刺激后数分钟内的升降情况。尽管不同细胞类型和技术之间的整体模式存在差异,EGF通路中的关键磷酸化位点在多次实验中反复被激活,证实了核心信号即使在多样化实验中仍具稳健性。
重建激酶之间的隐性对话
在推断出哪些激酶活性增强或减弱之后,作者尝试重建它们之间的潜在“对话”:哪些激酶可能激活或影响其他激酶。他们将激酶—底物图谱转换为激酶—激酶网络,并应用了三种计算策略,范围从简单的排序方案到一种更复杂的方法,该方法强制结果看起来像以EGF受体为根的有向树。他们将推断出的通路与若干“基准真相”进行比较:数据库中精心整理的EGF图谱、大规模单一激酶过表达实验,以及那些随时间行为高度相关的激酶位点对。
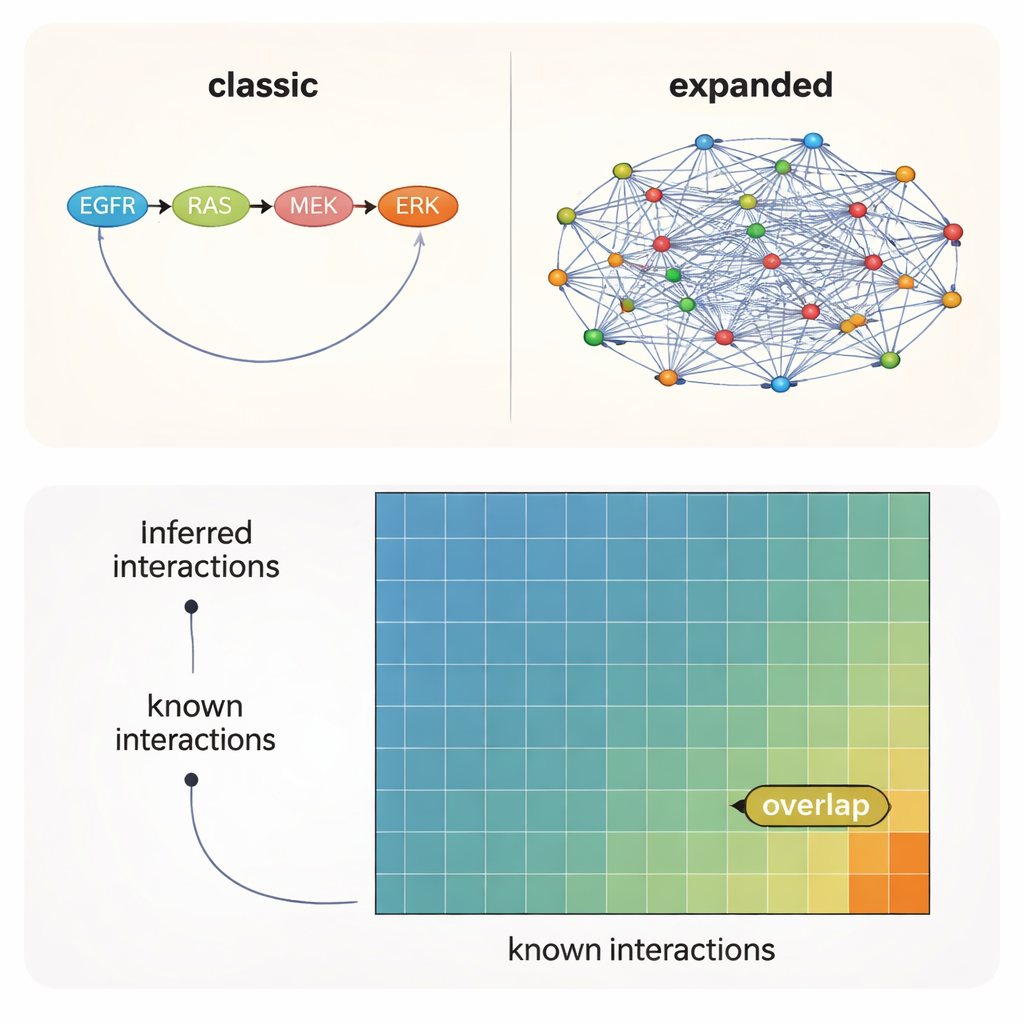
最可信的联系大多不在官方图谱上
在所有测试中,一个信息很明确:先验知识的选择——你在算法中输入的起始网络——比具体的方法乃至实验背景更为重要。基于文献构建的网络找回了最多的已知相互作用,而更广泛的预测性资源指向了许多尚未被正式记录的、却合情合理的额外连接。然而,即便在最佳条件下,数据和模型所提示的相互作用中只有约10–12%出现在任何参考集合中。换言之,大约90%的有支持证据的激酶—激酶连接依然处于未绘制的未知领域。
这对未来治疗意味着什么
对非专业读者而言,结论是:教科书中广为人知的EGF通路图很可能只是冰山一角。现代磷酸化蛋白质组学结合先进的计算方法揭示了一个更加丰富且复杂的信号网络。这些新提出的许多连接可能代表癌细胞重新绕道以逃避药物的被忽视途径,或为设计更聪明的药物组合提供新的机会。该研究并不证明每一条新联系都是确凿的,但它为研究者提供了路线图和开放工具,以便检验这些假设,最终目标是在EGF信号发挥核心作用的疾病中实现更精确、更有效的治疗。
引用: Garrido-Rodriguez, M., Potel, C., Burtscher, M.L. et al. Benchmarking EGF signaling pathway inference using phosphoproteomics and kinase-substrate interactions. Nat Commun 17, 2071 (2026). https://doi.org/10.1038/s41467-026-69332-0
关键词: EGF 信号, 磷酸化蛋白质组学, 蛋白激酶, 细胞信号网络, 癌症生物学