Clear Sky Science · zh
结核分枝杆菌调节宿主ATP6V1E1的磷酸化以促进细胞内存活
这对抗结核为何重要
结核病仍是全球最致命的传染病之一,每年夺走超过一百万人生命。我们的免疫细胞配备了强大的“酸性回收箱”,通常可消化入侵的微生物。本文揭示了结核分枝杆菌(Mycobacterium tuberculosis,简称Mtb)如何破坏我们细胞内的酸化系统,并表明针对这一伎俩的药物可以帮助受感染的动物更有效地清除感染。
细胞对病原体的酸性浴
当结核菌被吸入肺部时,迅速被称为巨噬细胞的免疫细胞吞噬。细菌被包裹在膜泡内,这些膜泡应与溶酶体融合——溶酶体是充满消化酶的小囊,且在强酸性环境下活性最佳。此酸性由一类分子泵—囊泡ATP酶(V-ATPase)产生,它利用细胞能量将质子泵入溶酶体以降低内部pH。适当的酸化对于分解Mtb至关重要,但数十年的研究表明该病原体以某种方式使其所在的隔室保持较低的酸性,从而存活下来。
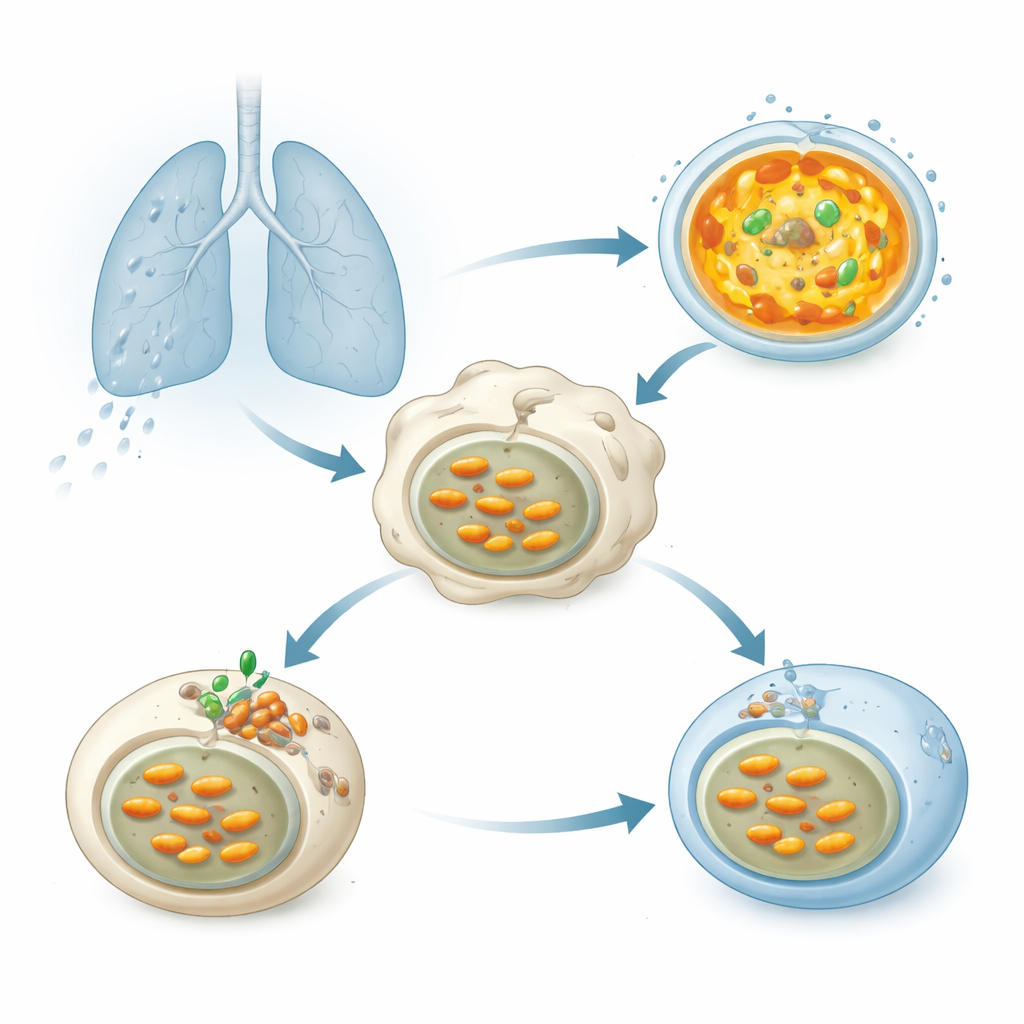
阻止酸化的细菌“帮手”
研究者筛选了Mtb可释放的200多种蛋白,寻找哪些会削弱人类细胞中溶酶体的酸化。其中一个蛋白脱颖而出:一种名为Chp2(亦称Rv1184)的酶。当细胞产生Chp2时,其溶酶体在酸敏染料下的信号变弱,表明pH升高、环境不再那么敌对。被改造为缺失Chp2的Mtb菌株不再抑制酸化;在感染的巨噬细胞和小鼠体内,这些突变菌更易被清除,并引起较轻的肺损伤。将Chp2恢复到突变株后,酸化阻断和更高的细菌负荷也随之回归,确认Chp2是帮助Mtb在宿主细胞内持续存在的毒力因子。
作为控制开关的宿主泵亚基
为弄清Chp2如何干扰酸化,研究团队寻找其可能结合的宿主成分。结果发现Chp2直接附着于V-ATPase的一个特定亚基——称为ATP6V1E1(简称E1),该亚基有助于稳定泵的结构。在细胞中增加E1的含量可增强溶酶体酸化并使Mtb更难存活,而降低E1则产生相反效果。携带仅一份功能性E1基因的小鼠具有较低的溶酶体酸性、肺内更高的细菌负荷以及更严重的组织损伤,表明E1是抵御结核的重要宿主防御因子。
使泵活性下降的激酶标记
作者接着探问E1上的化学“标记”是否会调节泵的活性。他们发现,在E1的两个特定位点酪氨酸(Tyr56和Tyr57)上添加磷酸基起到刹车作用:模拟磷酸化会降低酸化并阻碍V-ATPase的完整组装,而阻止磷酸化则产生相反的效果。通过筛选一组酶,他们鉴定出一位名为BMX的激酶为将该标记加到E1上的宿主蛋白。当通过基因学方法或小分子抑制剂阻断BMX时,E1的磷酸化下降,泵在溶酶体膜上的组装更为高效,溶酶体变得更酸性,Mtb在巨噬细胞内的存活率降低。
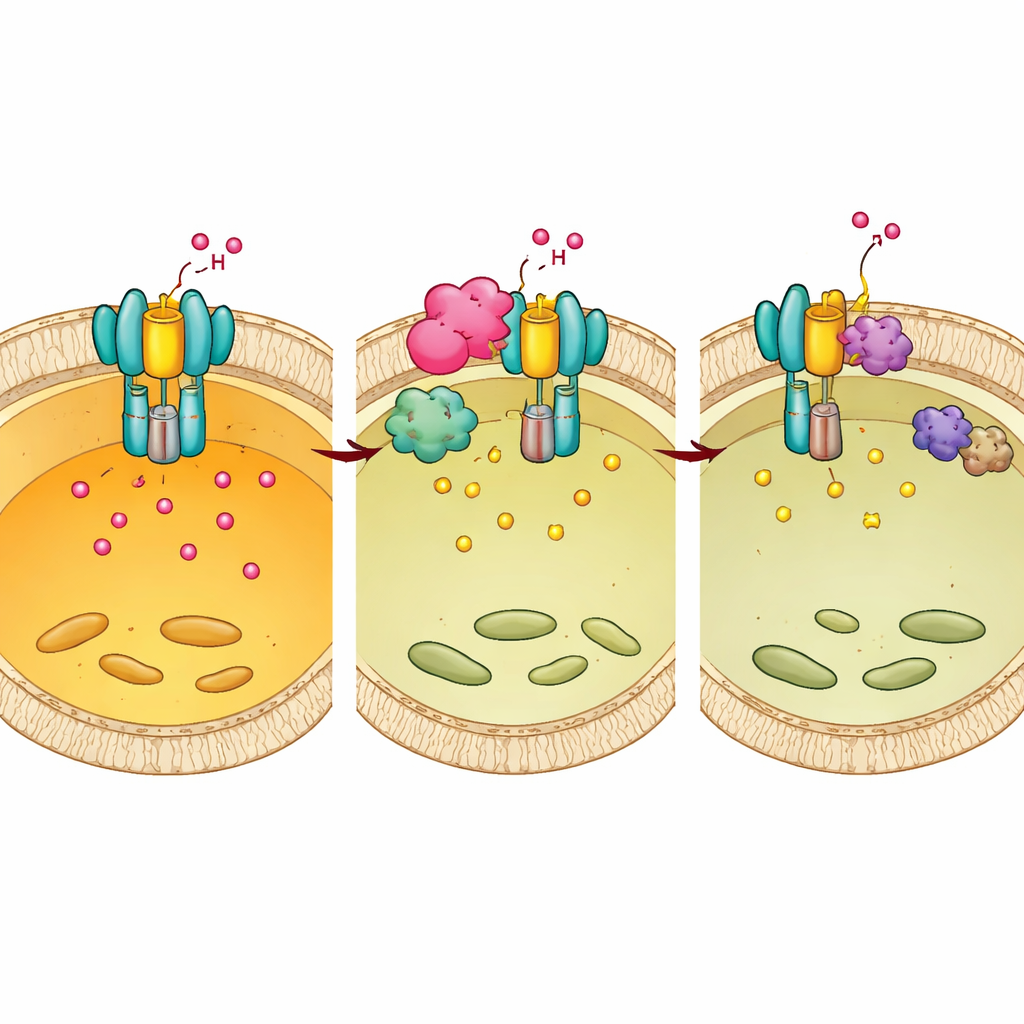
Mtb如何将宿主开关改写为己用
事实证明Chp2和BMX协同工作。结构和生化实验显示Chp2充当支架,将E1和BMX在溶酶体表面近距离带到一起,增强E1在Tyr56/57位点的磷酸化。这种额外的标记干扰了泵的完整组装,提高了溶酶体pH,从而创造了一个更温和的环境,便于Mtb存活。当抑制BMX时,Chp2带来的存活优势在细胞培养和感染小鼠中均消失。重要的是,在感染后给小鼠使用BMX抑制剂能降低正常动物的细菌负荷和肺部病理,但对E1功能受损的小鼠无效,表明该药通过恢复E1驱动的有效酸化发挥作用。
将病原体伎俩转化为治疗思路
通俗地说,这项研究表明结核菌向我们的细胞中投放了一个“帮手”蛋白,干扰垃圾处理装置上的“酸泵”,将其适度调低,使微生物得以避开破坏。通过识别作为关键控制旋钮的泵亚基(E1)和切换它的宿主酶(BMX),作者揭示了一个精确的药物干预点。在小鼠中抑制BMX可有效重新激活细胞内的酸性环境并改善细菌清除。这些发现为宿主导向疗法铺平了道路,使我们的细胞对Mtb更具敌意,可能与抗生素联用并有助于对抗耐药结核。
引用: Chen, J., Tang, F., Qin, L. et al. Mycobacterium tuberculosis modulates phosphorylation of host ATP6V1E1 to promote intracellular survival. Nat Commun 17, 2434 (2026). https://doi.org/10.1038/s41467-026-69331-1
关键词: 结核病, 溶酶体, 宿主导向疗法, 结核分枝杆菌, V-ATP酶