Clear Sky Science · zh
用于治疗人类偏肺病毒感染的高效单克隆抗体的开发
为何这个隐藏的冬季病毒重要
在每一个感冒和流感季节中,一种鲜为人知的病毒——人类偏肺病毒(HMPV)悄然将数以百万计的幼童、老年人以及免疫系统受损的人送入门诊和医院。与其“表亲”呼吸道合胞病毒(RSV)不同,针对HMPV目前没有疫苗或特异性治疗方法。本研究报道了一种强效的实验室制备抗体,称为4F11,能够在细胞中阻断HMPV并保护受感染的动物,指向为最脆弱患者开发的一种迫切需要的新药物。
在雷达下飞行的病毒
HMPV是全球常见的呼吸道病毒,每年估计导致约1400万例五岁以下儿童的下呼吸道感染,并且对60岁以上的成年人也造成沉重负担。对于免疫系统严重受损的患者——例如造血干细胞移植受者——HMPV肺部感染的死亡率可能非常高。与RSV等相关病毒的疫苗才刚刚出现,即便存在HMPV疫苗,许多严重免疫抑制的患者也可能产生不佳的应答。正因如此,研究者正转向单克隆抗体——可作为药物给予的精确靶向免疫蛋白——以预防或治疗重症感染。
寻找突出保护性的抗体
研究团队着手寻找具有三项关键特征的抗体:必须极其有效、能对抗多种HMPV株,并且使病毒难以发展出耐药性。他们将注意力集中在病毒的融合蛋白上——这是病毒表面一个需形变以允许病毒与并进入肺细胞的“发条”结构。采用“一种诱饵换取另一种”的策略,他们从血液和脾脏样本中挑选出罕见的人体B细胞,这些细胞能识别一种HMPV株但能中和另一种,从而富集出广谱抗体。在一千多个候选细胞中,他们分离出三种有前景的抗体,发现其中一种——4F11——异常强效,在阻断细胞感染方面所需浓度比之前的领先抗体低近50倍,并能对抗四种主要的全球HMPV亚型。
4F11如何抓住病毒的薄弱点
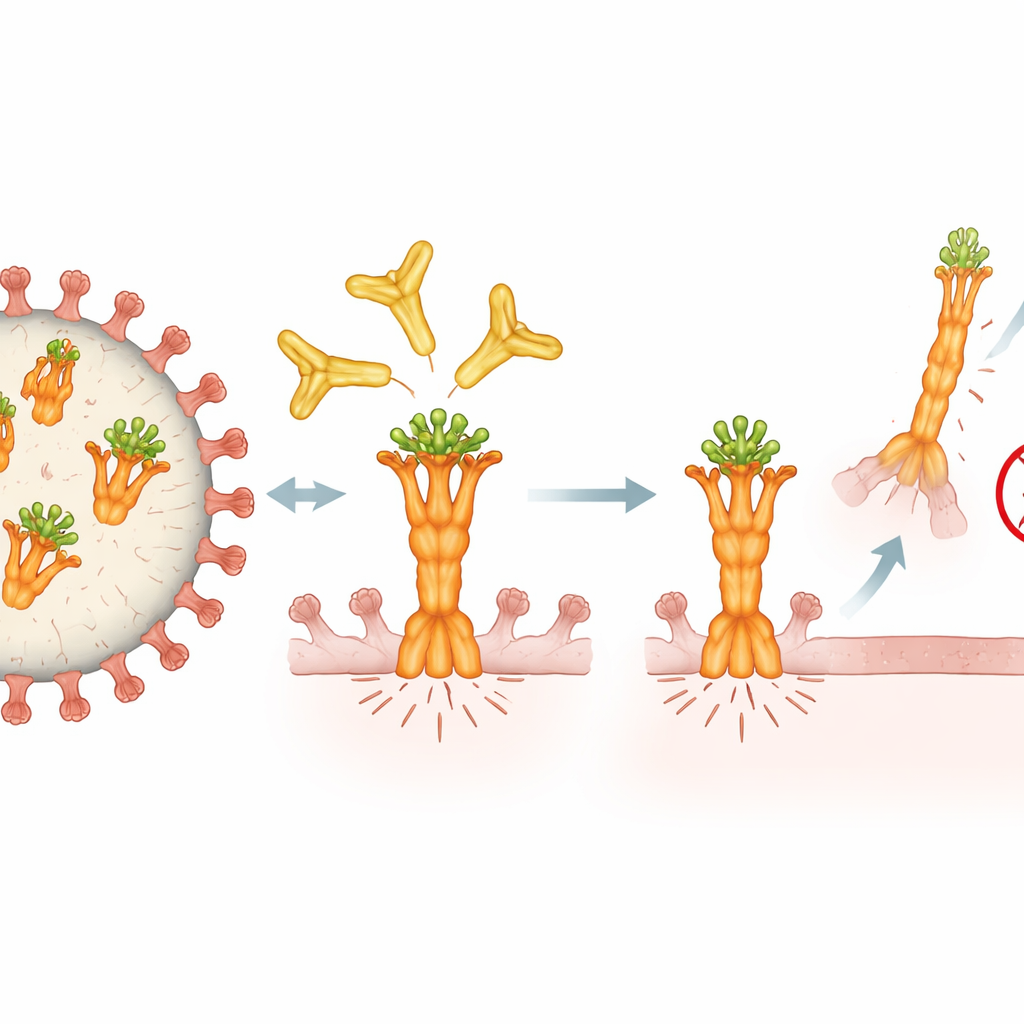
为了解4F11为何如此有效,研究者使用高分辨率冷冻电子显微镜可视化其如何锁定融合蛋白。他们发现4F11定位在蛋白预融合构象顶部的一个极小且高度保守的区域——即发条尚未释放的状态。与其他能在每个融合蛋白上结合三个抗体的情况不同,4F11以一对一的方式独自位于顶端,直直下探,甚至抓住了一个遮蔽表面的糖基修饰。这个不寻常的结合角度及对该糖的依赖,使4F11成为一种独特类型的抗体。它仅识别预融合构象——存在于具有感染性的病毒上——并很可能阻止该蛋白重折叠为穿刺并与宿主细胞融合所需的形状。
病毒能否逃脱——代价几何?
团队随后在持续存在4F11的细胞培养中强迫病毒生长,以观察其进化出逃逸的难易程度。与另一种对照抗体相比(该对照抗体迅速促成了若干逃逸突变的出现),HMPV更难以绕过4F11。只有融合蛋白发生单一变化——在第179位氨基酸的替换——能完全破坏4F11的结合。然而,携带该突变的病毒生长明显差于野生型病毒,表明病毒适应性遭受了严重的损失。对数百个HMPV序列的数据库检索显示,这种有害的变化在自然界中从未被观察到,提示尽管病毒在实验室条件下原则上可以逃逸4F11,但其在生长上付出的高昂代价使其在现实世界中广泛传播的可能性很小。
在动物模型中测试保护效应
实验室中的高效仍需转化为真实的保护。为测试这一点,研究者用HMPV感染金仓鼠并在一天后给予4F11治疗——模拟早期治疗而非预防。一次低剂量注射4F11即可显著降低肺和鼻腔中的病毒水平,而在更高剂量下,大多数动物肺内可检测到的病毒被完全清除。值得注意的是,这些剂量低于若干已获批用于人类RSV的单克隆抗体所用剂量。相比之下,以相同剂量给予的一种先前描述的可交叉反应多种病毒的抗体几乎没有保护作用,凸显了作为专注于HMPV疗法的4F11的特别优势。
这对患者意味着什么
综上,这些发现使4F11成为临床开发的有力候选者。它结合了高效力、对流行HMPV株的广泛覆盖、对融合蛋白脆弱区域的独特结合方式,以及一种抗性格局——病毒明显的逃逸路线伴随着显著的自我损害。对于高危重症HMPV疾病的婴儿、老年人和免疫受损患者,基于4F11的药物未来或可既作为感染后的紧急治疗,也可作为与疫苗并用或替代疫苗的额外保护手段。
引用: Harris, E.D., McGovern, M., Pernikoff, S. et al. Development of a potent monoclonal antibody for treatment of human metapneumovirus infections. Nat Commun 17, 2714 (2026). https://doi.org/10.1038/s41467-026-69328-w
关键词: 人类偏肺病毒, 单克隆抗体, 呼吸道感染, 融合蛋白, 抗病毒疗法