Clear Sky Science · zh
用于研究肠-神经病理发生双向串扰的3D肠-脑-血管平台
为什么你的肠道可能与大脑息息相关
“你就是你吃的东西”这一说法有了新的延伸:越来越多的证据表明,肠道内发生的事情会影响大脑健康。本文介绍了一种先进的实验室模型,将人体肠道、血管和脑组织的小型模拟结构连接在同一芯片上。通过观察信号如何沿着这条微小通道传播,研究者探讨了肠道问题如何可能触发阿尔茨海默病和帕金森病等脑部疾病——反过来,大脑问题又如何将压力传回肠道。
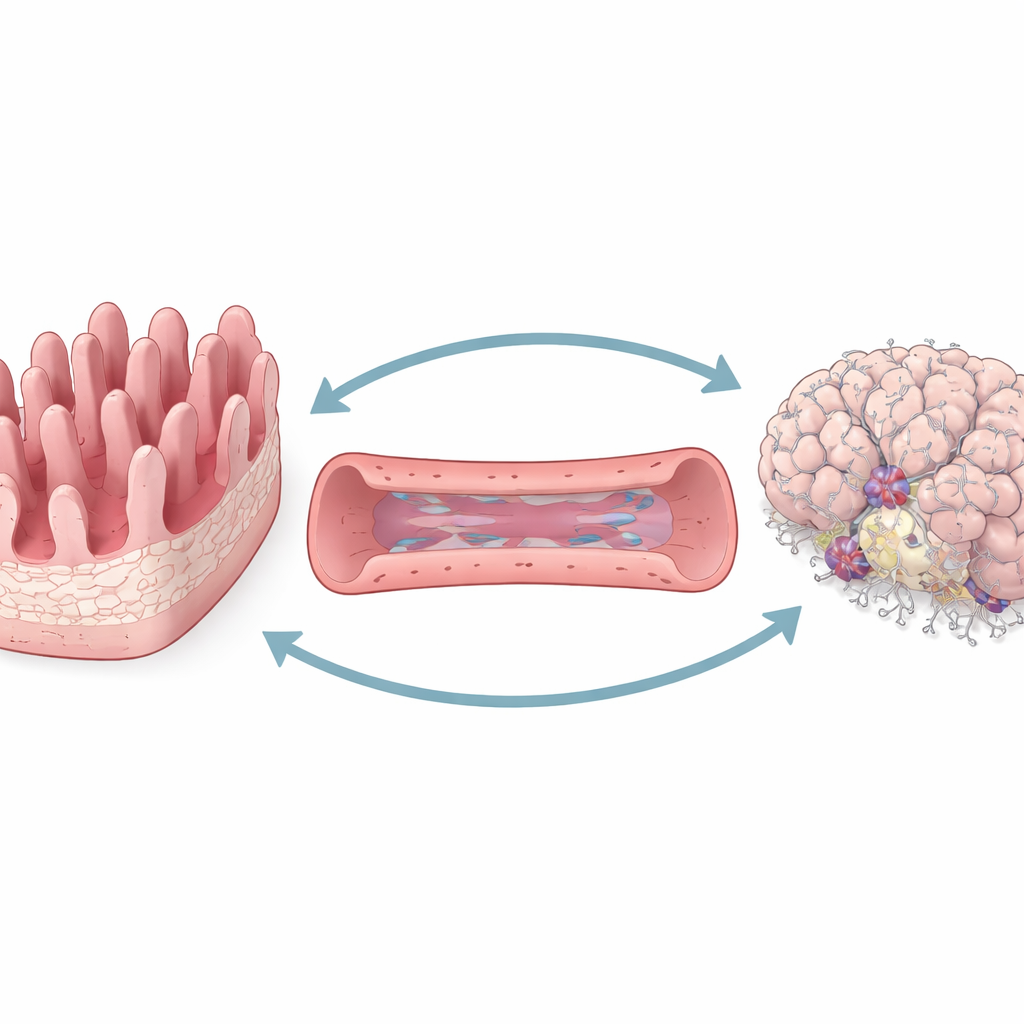
在芯片上构建微型人体
为了在可控条件下研究肠-脑间的通讯,团队构建了一个三部分的“器官芯片”平台。一个隔室模拟肠道内表面,具有指状突起,形成肠内容物与身体其余部分之间的屏障。第二个隔室代表内衬脑样血管细胞的血管。第三个隔室容纳活体人类神经元和支持细胞,排列成类似小块脑组织的结构。流体可以在这些隔室之间流动,使分子得以像在体内循环中那样传播。
让模型更像真实组织
芯片的设计使细胞经历轻微的摇摆流动,而不是静置在平皿中。这种运动促使肠层形成更厚、更逼真的褶皱,并在细胞之间形成更紧密的连接,使其不那么易漏。血管层在流动方向上伸展,这是健康血管的特征,并对大分子表现出强的屏障功能。在脑隔室中,神经元形成活跃的网络并发出有节律的钙信号,表明电活动,同时支持细胞像真实脑组织中那样环绕邻近血管。总体来看,这些特征表明三部分的行为比传统平面细胞培养更接近体内状态。
当肠道刺激物引发大脑问题
为模拟由肠道驱动的疾病,研究者在芯片的肠侧加入了细菌产物——来自大肠杆菌培养的材料或一种名为LPS的纯化毒素。这些刺激削弱了肠屏障,使更多大分子和细菌痕迹渗入血管隔室,随后到达脑隔室。随着渗漏增加,血管壁变得不那么紧密,星形的脑支持细胞转为反应性、警报状态。在类脑组织中,与阿尔茨海默和帕金森相关的有害蛋白片段积累,神经元之间的保护性连接减少,炎症信号激增。从肠道紊乱出发、最终导致脑细胞受压的这一序列,与动物研究和患者中观察到的模式相一致。
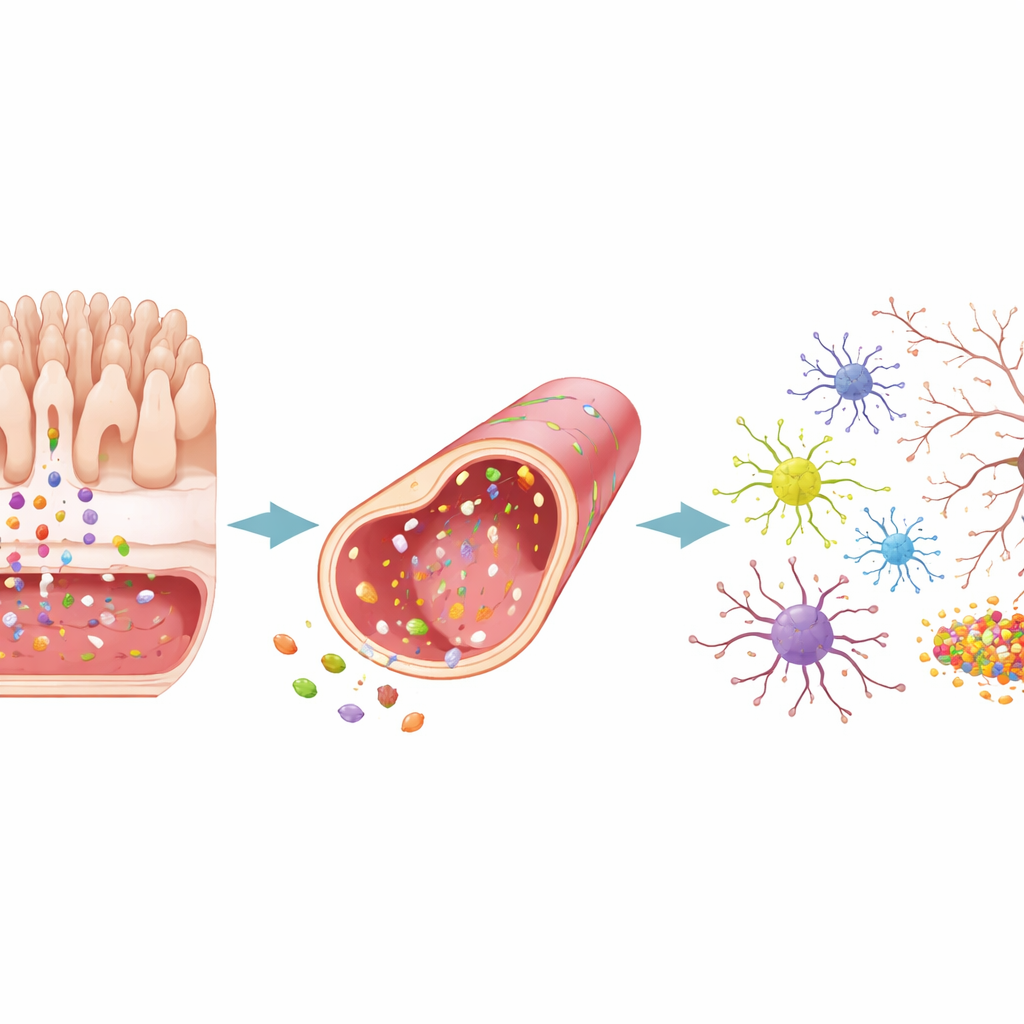
当脑病向外传递信号
随后团队反转了实验方向。他们通过让芯片上的脑细胞过度产生黏性的淀粉样片段来模拟阿尔茨海默样状况,通过使其暴露于α-突触核蛋白聚集物来模拟帕金森样状况。在这两种情形中,有毒蛋白首先在脑隔室积累,随后出现在血管和肠区。脑组织释放出波状的炎性分子,突触连接丧失,并显示出其他退行性特征。这些源自大脑的危险信号强烈干扰了血管层,使其屏障松动并激活附近的支持细胞。然而肠层仅显示出有限的结构性变化:表面有所改变并呈现更多“激活”特征,但其紧密连接总体保持,渗漏仅略有增加。
这对未来治疗意味着什么
通俗而言,该芯片表明,病变的肠道比病变的大脑更可能直接驱动脑部炎症和损伤。源自肠道的细菌产物和炎症似乎能削弱血管和脑组织,而起源于大脑的炎症主要作用于血管,并仅对肠道造成轻微改变。由于整个系统由人类细胞构建,它为旨在平抑肠道炎症、修复屏障或阻断有害蛋白扩散的疗法提供了有前景的测试床。最终,类似的平台可能帮助医生确定哪些患者最有可能从以肠道为中心的策略中获益,从而减缓或预防神经退行性疾病。
引用: Tran, M., Jeong, H.W., An, M. et al. A 3D gut-brain-vascular platform for bidirectional crosstalk in gut-neuropathogenesis. Nat Commun 17, 2504 (2026). https://doi.org/10.1038/s41467-026-69318-y
关键词: 肠-脑轴, 器官芯片, 神经炎症, 阿尔茨海默病, 帕金森病