Clear Sky Science · zh
前视区kisspeptin-nNOS-GnRH (KiNG) 神经网络通过激活-抑制机制调节小鼠黄体生成素节律性
这个脑科学发现为何关系到生育
排卵和生育依赖于一小群以脉冲和偶发性激增方式释放主导激素的脑细胞。当这种时序紊乱时,生殖功能可能受损。这项研究揭示了小鼠大脑中两类信号分子如何协同作用:一类激活神经活动,另一类则悄然将其关停,从而塑造这些激素节律。理解这一隐秘的时序回路,可能最终有助于解释某些形式的不孕不育并提示新的治疗思路。
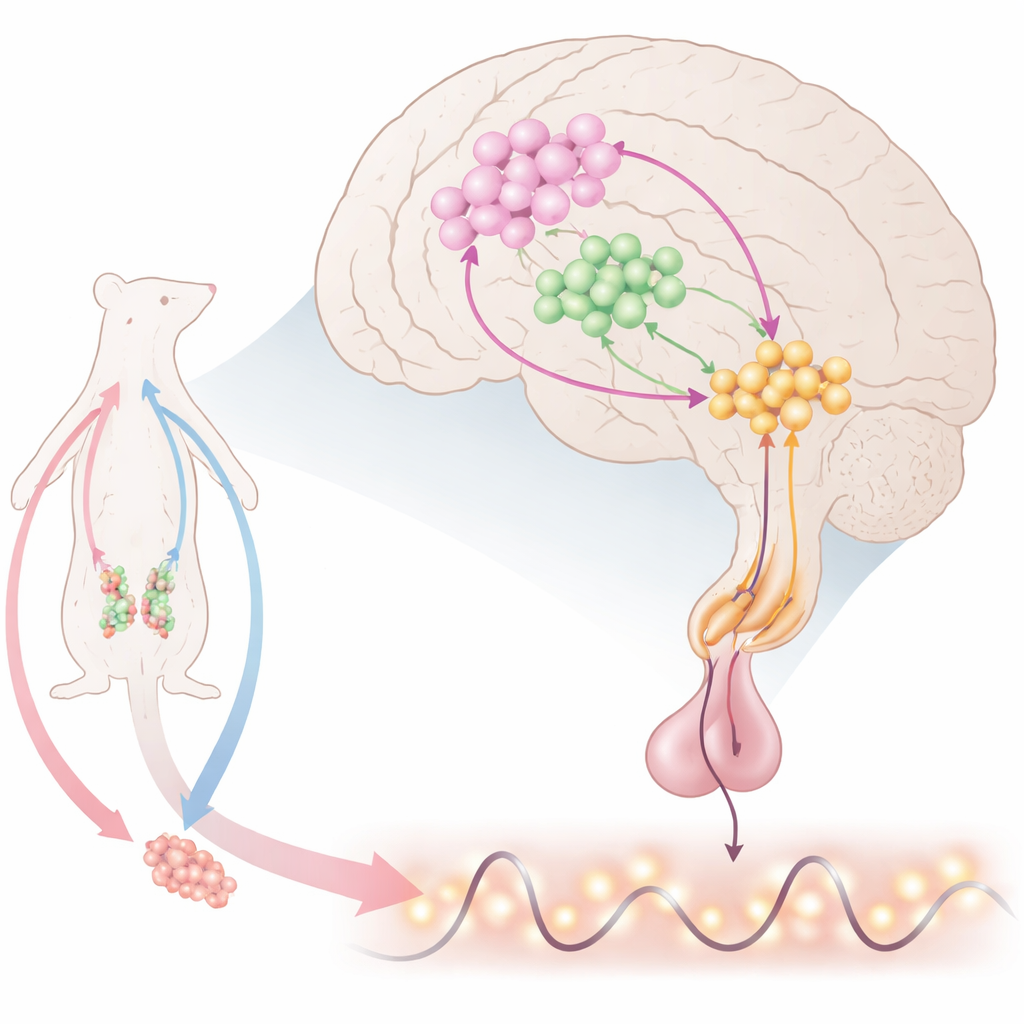
大脑中的生殖计时器
在大脑深处,特殊的神经细胞释放促性腺激素释放激素(GnRH),它告诉脑垂体分泌黄体生成素(LH)和促卵泡激素(FSH)。这些激素反过来调控卵巢和睾丸。GnRH并非持续恒定释放;相反,它以规律的脉冲出现,在雌性中还有一次大的排卵前激增。科学家们知道有许多信号输入到GnRH细胞,但产生脉冲与激增两种模式的确切组合仍不明朗。本研究聚焦于下丘脑前部的一个小区域,在此GnRH细胞与两类重要细胞相互接触:产生kisspeptin并兴奋GnRH的神经元,以及产生一氧化氮(NO)的神经元,NO是一种可在短距离内弥散的气体信号。
两种信号之间的开—关搭档
研究者提出了一个由kisspeptin、产生NO的nNOS神经元和GnRH细胞组成的三部分“KiNG”网络。Kisspeptin是强有力的激活因子,能够驱动GnRH和LH的释放,但持续刺激会使系统关闭,这提示需要内在的刹车机制。通过高灵敏度的分子探针、基因工具和小鼠脑片记录,研究团队显示kisspeptin不仅直接兴奋GnRH神经元。它还激活前视区附近的nNOS神经元,特别是在称为OV/MePO的区域。当kisspeptin水平上升时,这些nNOS细胞产生NO爆发,触发周围细胞(包括GnRH神经元)内第二信使cGMP的产生。该NO–cGMP信号抑制GnRH的放电,为kisspeptin驱动提供了一个内建的关闭开关。
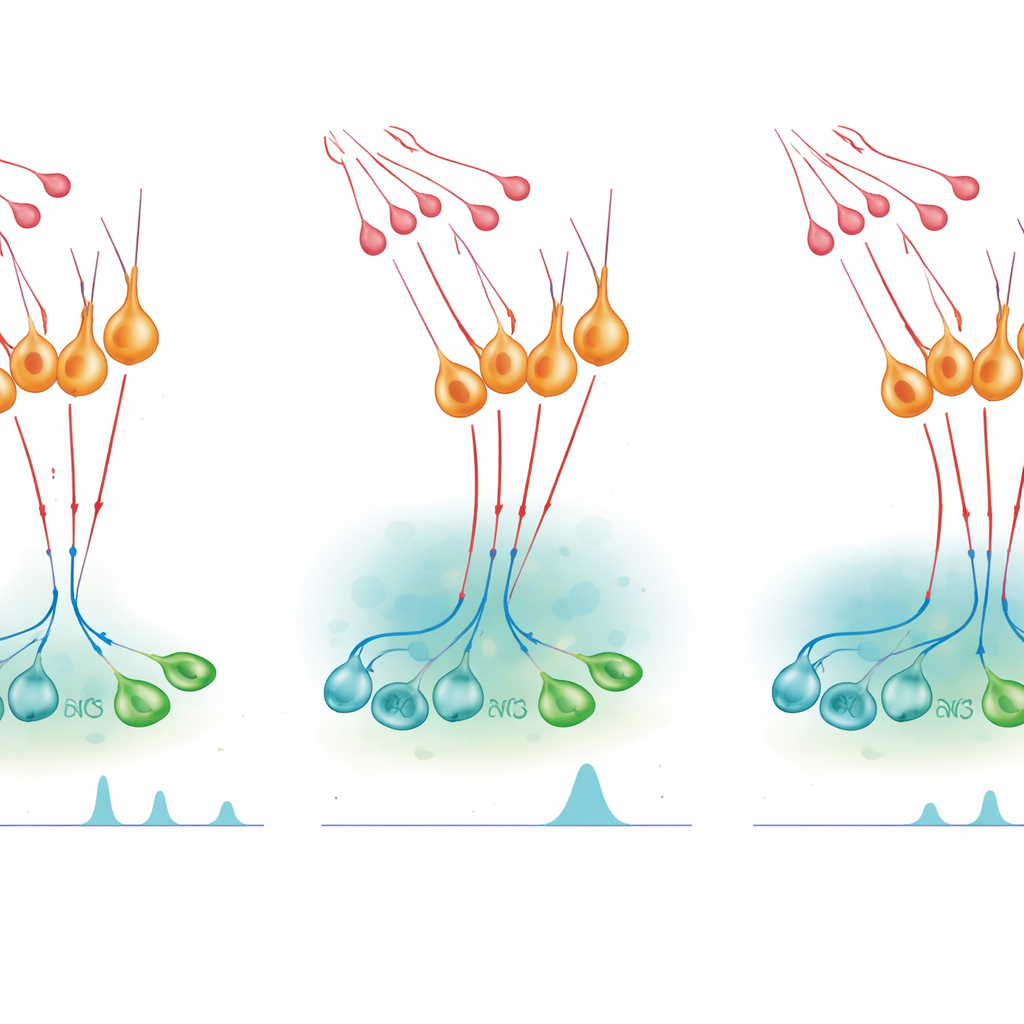
开启激素激增并对其加以收束
为测试该微电路如何影响激素释放,团队使用了化学遗传学开关——经工程化受体由一种本身无活性的药物激活——在活体小鼠中开启或关闭nNOS神经元。在雌性周期通常安静的阶段人工激活nNOS细胞,就足以诱发类似激增的血中LH升高,雄性亦然。阻断NO产生则抹除了该效应,表明这些神经元释放的NO对激增是必要的。然而,当科学家抑制nNOS神经元或降低其对kisspeptin的敏感性时,一次kisspeptin注射会导致更夸张且持续的LH升高。阻断NO合成的药理药物具有类似的放大作用,而延长cGMP信号的药物则缩短了kisspeptin反应并减少了随后LH的输出。综上,这些实验表明NO既有助于同步GnRH神经元以产生激增,又限制kisspeptin维持其放电的时长。
跨卵巢周期的灵活节律
研究还表明这种开—关平衡随雌性周期变化而调整。利用一种灵敏的RNA检测方法,作者发现排卵前一天(雌激素水平高且发生LH激增时)更多的nNOS神经元表达kisspeptin受体。在较安静的阶段,较少的nNOS神经元对kisspeptin有反应,只产生小范围的局部NO,温和地抑制GnRH脉冲而不停止它们。在激增日,较强的kisspeptin输入和受体表达的上调大幅提升NO产出,使NO传播得更远并短暂地沉默大量GnRH神经元。当NO信号消退时,这些细胞一起反弹,产生所需的大规模协调性LH激增以触发排卵。
对人类健康的意义
简言之,这项工作表明,启动GnRH神经元的同一信号——kisspeptin——也通过NO招募了一个延迟的制动系统,确保激素爆发强烈但不会失控。因此,KiNG网络既是生殖时序的加速器,也是刹车,调节周期大部分时间的GnRH脉冲并塑造触发排卵的激增。因为在患有生殖问题的人群中已发现kisspeptin和NO通路的基因改变,理解这一精细平衡的回路可能为诊断和治疗不孕及相关疾病提供新的思路。
引用: Delli, V., Moulinier, M., Lazaridou, AM. et al. Preoptic kisspeptin-nNOS-GnRH (KiNG) neuronal network regulates LH rhythmicity through activation-inhibition in mice. Nat Commun 17, 2558 (2026). https://doi.org/10.1038/s41467-026-69316-0
关键词: 生殖激素, 下丘脑, kisspeptin, 一氧化氮, 排卵时机