Clear Sky Science · zh
组蛋白乳酰化通过增加CXCL1表达促进胰腺癌中中性粒细胞浸润与免疫逃逸
这项癌症研究为何重要
胰腺癌是致死率极高的癌症之一,部分原因在于它常对其他肿瘤中有效的现代免疫疗法产生抵抗。该研究揭示了胰腺肿瘤如何改写自身的糖代谢来默默削弱免疫系统,以及阻断这一过程如何可能为机体防御——以及现有药物——重新打开反击的通路。
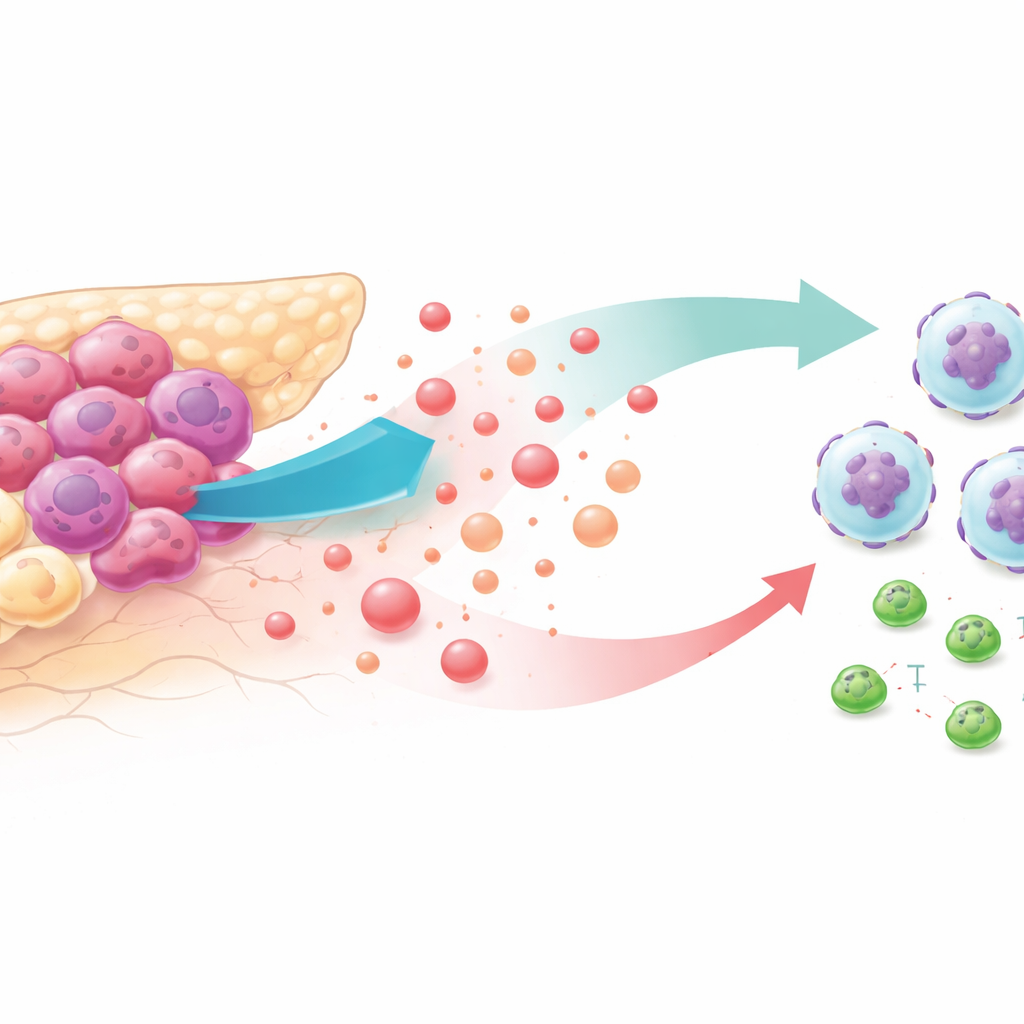
嗜糖肿瘤与敌对的微环境
癌细胞以高速消耗葡萄糖而臭名昭著,即便在氧气充足的情况下也如此。这种“高糖酵解”生活方式将乳酸这一曾被视为代谢废物的产物大量释放到肿瘤周围环境中。通过分析患者肿瘤数据库和小鼠模型,研究者发现糖酵解最强烈的胰腺癌伴随大量中性粒细胞——在此情境下这些白细胞反而帮助肿瘤生长——同时致癌性CD8 T细胞减少。出现这种代谢与免疫特征的患者生存期较短,提示代谢改变与免疫逃逸密切相关。
肿瘤如何利用乳酸招来错误的“援军”
为弄清糖酵解如何吸引中性粒细胞,团队在胰腺癌细胞系和小鼠中通过药物或遗传手段降低肿瘤糖酵解。当阻断糖分分解时,肿瘤细胞释放的名为CXCL1的化学信号大幅减少,循环中该信号的水平在小鼠和患者样本中均下降。在体外趋化实验中,中性粒细胞积极向高糖酵解癌细胞培养上清移动,但不会向被抑制糖酵解的培养上清移动——除非研究者补回纯化的CXCL1。在活体小鼠中,对糖酵解被抑制的肿瘤恢复表达CXCL1会使中性粒细胞数量回升,并削弱抑制糖酵解的抗肿瘤效果。
由乳酸驱动的新型表观遗传开关
研究接着聚焦到DNA包装层面。我们的基因缠绕在类似线轴的蛋白质——组蛋白上,其化学标记充当基因活动的开/关开关。作者展示,在胰腺癌中,由糖酵解产生的乳酸会向一种组蛋白位点添加特定的“乳酰”标记,即H3K18位点。该修饰,称为组蛋白H3K18乳酰化,在肿瘤组织中明显高于正常胰腺组织。当糖酵解被阻断时,H3K18处的乳酰化尤其在CXCL1基因调控区域附近下降,CXCL1的产生也随之减少。补回乳酸可恢复该组蛋白标记和CXCL1表达。在患者样本中,H3K18乳酰化较多的肿瘤也显示出更高的CXCL1,将这一分子标记与促肿瘤的免疫环境联系起来。
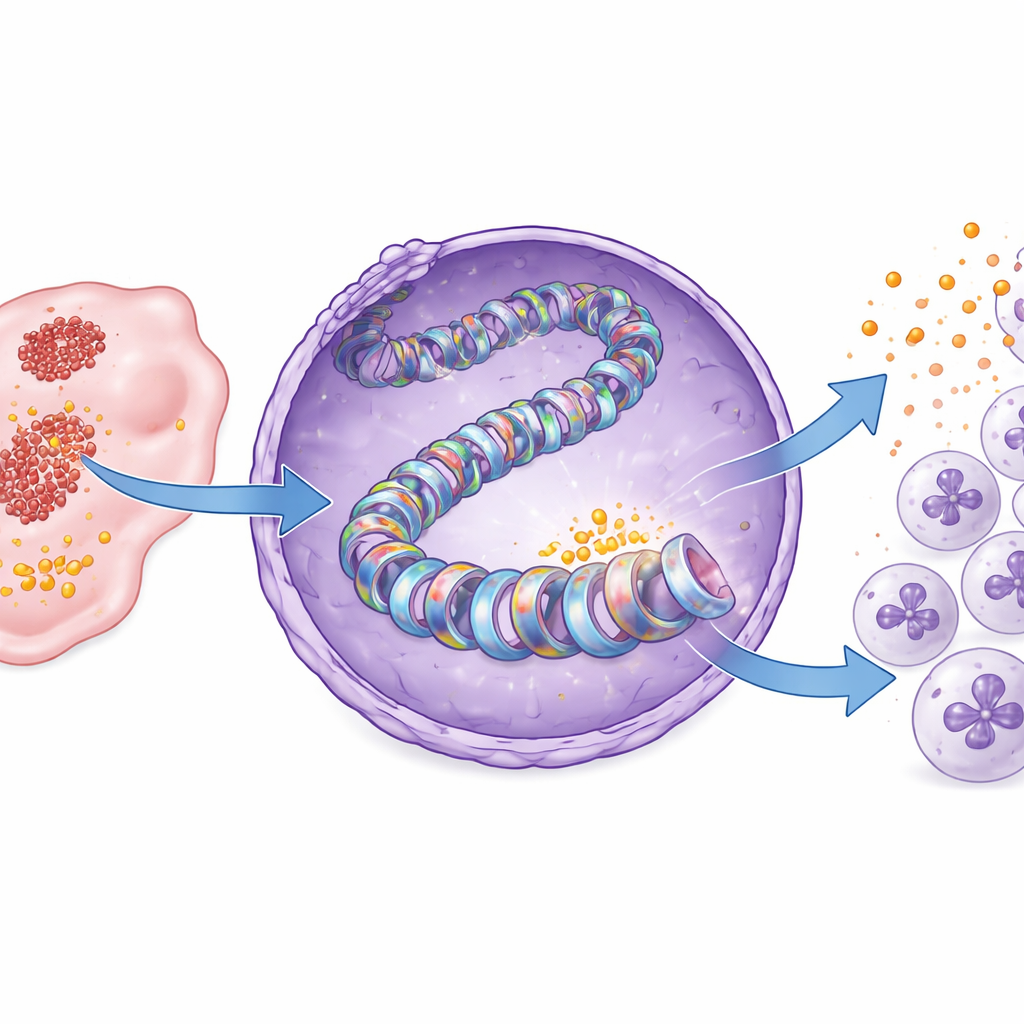
鉴定出写入酶与可药物化的薄弱环节
组蛋白标记由专门的酶写入。通过筛选已知组蛋白修饰蛋白的抑制剂,研究者锁定了一种名为PCAF的酶,作为胰腺癌中H3K18乳酰化标记的关键写入者。结构建模表明PCAF可结合乳酰辅酶A(乳酸的活化用于标记的形式),生化实验证实纯化的PCAF能直接向组蛋白H3添加乳酰基。用小分子抑制PCAF(溴孢素)可降低癌细胞和小鼠肿瘤中的H3K18乳酰化及CXCL1产生。结果是进入肿瘤的中性粒细胞减少,CD8 T细胞增加,肿瘤生长减缓,同时小鼠未出现明显体重下降或毒性。
用联合疗法将“冷肿瘤”变“热”
由于像抗PD-1抗体这样的标准免疫检查点药物在胰腺癌中效果有限,团队测试了拆解乳酸–PCAF–CXCL1通路是否能提高这些肿瘤的响应性。在皮下和胰腺原位小鼠模型中,溴孢素与抗PD-1联合治疗比任一单独疗法都能更有效缩小肿瘤,减少中性粒细胞浸润,增强活跃的CD8 T细胞,并显著延长存活期。这表明切断肿瘤招募中性粒细胞的代谢“警报器”有助于将免疫学上“冷”的肿瘤转变为对检查点疗法更易被激活的“更热”肿瘤。
对未来治疗的意义
简单来说,该研究揭示了一条链式反应:胰腺肿瘤大量消耗糖,释放乳酸,利用乳酸在其DNA包装蛋白上翻转一个表观遗传开关,上调CXCL1,从而招募有利于肿瘤的中性粒细胞,帮助肿瘤躲避杀伤性T细胞。在PCAF步骤用药中断这条链,不仅能减缓肿瘤生长,还能在小鼠中增强现有免疫治疗的效力。尽管仍需更多工作以确保安全性并找到在人类中最佳的干预方式,这些发现强调了一种有希望的策略:重新编程肿瘤的代谢与基因开关,为免疫系统创造更公平的抗衡条件。
引用: Zhang, P., Ma, J., Wan, Y. et al. Histone lactylation increases CXCL1 expression for neutrophil infiltration and immune escape in pancreatic cancer. Nat Commun 17, 2526 (2026). https://doi.org/10.1038/s41467-026-69311-5
关键词: 胰腺癌, 肿瘤代谢, 组蛋白乳酰化, 肿瘤微环境, 癌症免疫治疗