Clear Sky Science · zh
利用 DNA-PAINT 可预测的结合动力学来为超分辨率图像去噪
透视微观世界的更清晰视野
现代显微镜现在可以“看到”细胞内的单个分子,但这些图像常常被误导性的背景点斑驳。该研究介绍了一种利用 DNA 片段自然结合与解离的时间特性来清理此类图像的方法。结果是细胞内分子机器的图像更加清晰,这对基础生物学到药物发现等各个领域都很重要。
一种闪烁技巧如何揭示隐藏细节
一种强大的成像方法称为 DNA-PAINT,它将短 DNA 链的随机结合转化为超分辨显微成像工具。一端的 DNA 链连接到研究者想要观察的蛋白;匹配的携带荧光染料的短链漂浮在溶液中。当漂浮的链短暂结合到其配对上时,会产生微弱的光闪。通过记录许多此类闪烁并精确定位其位置,研究者可以以纳米级精度重建蛋白的位置——远比传统光学显微镜更清晰。
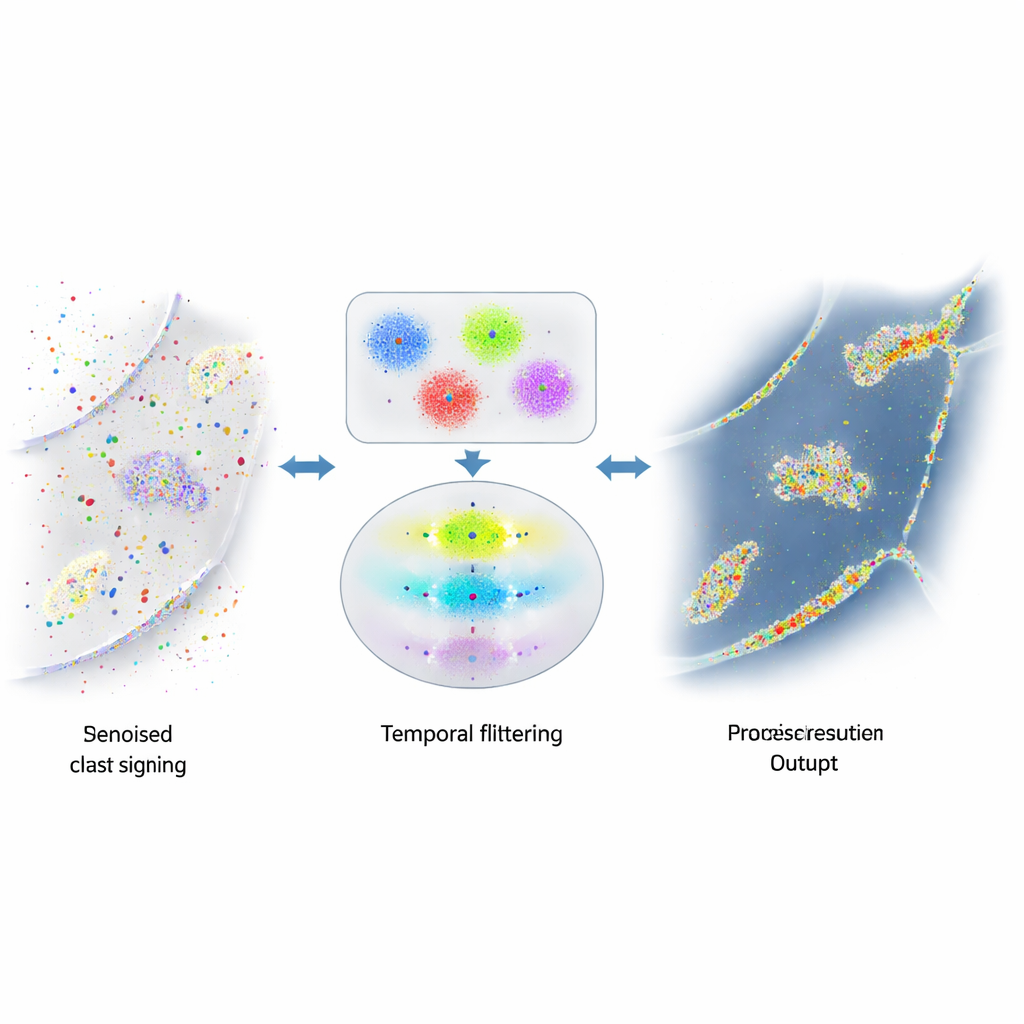
当有用信号被噪声掩埋时
DNA-PAINT 的优势——大量自由移动的荧光链——也带来问题。这些链有时会在不该出现的地方粘附,例如随机的细胞表面或细胞核内丰富的 DNA 上。那些意外的闪烁在外观上无法与真实信号区分,从而在最终图像中产生假点和伪簇。早期减少这类噪声的尝试侧重于改变化学条件以降低非特异性结合的频率,或使用粗略的规则来识别明显的异常点。然而,大量误导性信号仍然存在,限制了科学家对蛋白数量或空间关系进行可靠测量的能力。
用时间来分辨真与伪
作者意识到,在 DNA-PAINT 中真实的 DNA 配对遵循一个简单的时间规律:真实结合事件之间的间隔服从可预测的指数分布。而随机粘附事件则不符合这一规律。他们构建了一个多步骤算法,首先基于位置将相近的闪烁分组为小簇,使用基于密度和 k-means 的组合来将复杂形状拆分为与定位精度相当的单元。对每个簇,他们随后构建了一个结合事件的“时间轨迹”,并在构建时小心地将来自同一结合位点的快速开关闪烁合并为单个事件。最后,他们应用统计检验来判断每个簇中事件间的间隔是否符合预期的指数行为。通过检验的簇被视为真实信号;未通过的则作为噪声丢弃。
在真实细胞中检验该方法
为了测试他们的方法,团队在果蝇卵室中成像了细胞黏附蛋白 E-cadherin,其中一些细胞表达带标记的蛋白,而相邻细胞则不表达。这样形成了并列的真实信号丰富区域和应仅包含背景的区域。通过调整在对簇进行检验前必须显示的结合事件数量,他们找到了能去除超过 90% 伪簇同时保留细胞边界处超过 98% 真实簇的参数设置。在去噪后的图像中,诸如细长管状结构和囊泡等细微特征变得更加清晰。相同策略在其他系统中也有效,包括线粒体和微管,甚至对那些分布更为弥散、无明显空间图案可供辨别真实信号的蛋白也适用。
为未来研究提供更清晰的分子图谱
通过聆听 DNA 结合的“节奏”而不仅仅观察闪烁发生的位置,该方法可靠地剥离了 DNA-PAINT 数据中的误导性背景。对非专业读者而言,关键结果很简单:细胞内更清晰、更可信的分子图谱。这使得计数蛋白分子数量、评估不同蛋白相互靠近的程度,以及构建更准确的细胞内部景象更加可靠。随着基于 DNA 的成像技术继续发展,这类智能去噪对将原始斑驳图像转化为可靠的生物学洞见将至关重要。
引用: Sirinakis, G., Allgeyer, E.S., Richens, J.H. et al. Utilizing the predictable binding kinetics of DNA-PAINT to denoise super-resolution images. Nat Commun 17, 2397 (2026). https://doi.org/10.1038/s41467-026-69304-4
关键词: DNA-PAINT, 超分辨率显微镜, 图像去噪, 单分子成像, 蛋白质定位