Clear Sky Science · zh
激活STING通过炎性细胞死亡通路在脑膜瘤中诱导细胞毒性和免疫反应
将机体的警报系统转向对抗脑肿瘤
脑膜瘤是常见的脑肿瘤之一,尽管手术和放疗常能奏效,但有些肿瘤会不断复发。这些顽固的肿块可引发癫痫、头痛和功能障碍,但尚无公认的广泛药物治疗方案。本研究探讨了一种方法,利用一种能开启先天危险感应系统STING的分子,使肿瘤细胞及其周围的免疫细胞发出强烈的内部警报。研究者的目标不仅是直接杀死肿瘤细胞,还要唤醒免疫系统并软化肿瘤的坚韧基质。
躲在“沉默”免疫邻里的肿瘤
作者首先利用单细胞测序和空间成像描绘了人类脑膜瘤内部的细胞“邻里”结构。他们发现这些肿瘤富含先天免疫细胞,尤其是巨噬细胞,而典型的抗肿瘤T细胞和自然杀伤(NK)细胞则稀少且常处于功能耗竭状态。肿瘤细胞四周被致密的胶原和其他基质蛋白包裹,形成一层装甲般的分层结构。许多位于这些区域的巨噬细胞携带可被胶原激活的抑制性受体,造成一种高度受抑制的环境,免疫细胞虽在场却被束缚,无法对抗癌症。
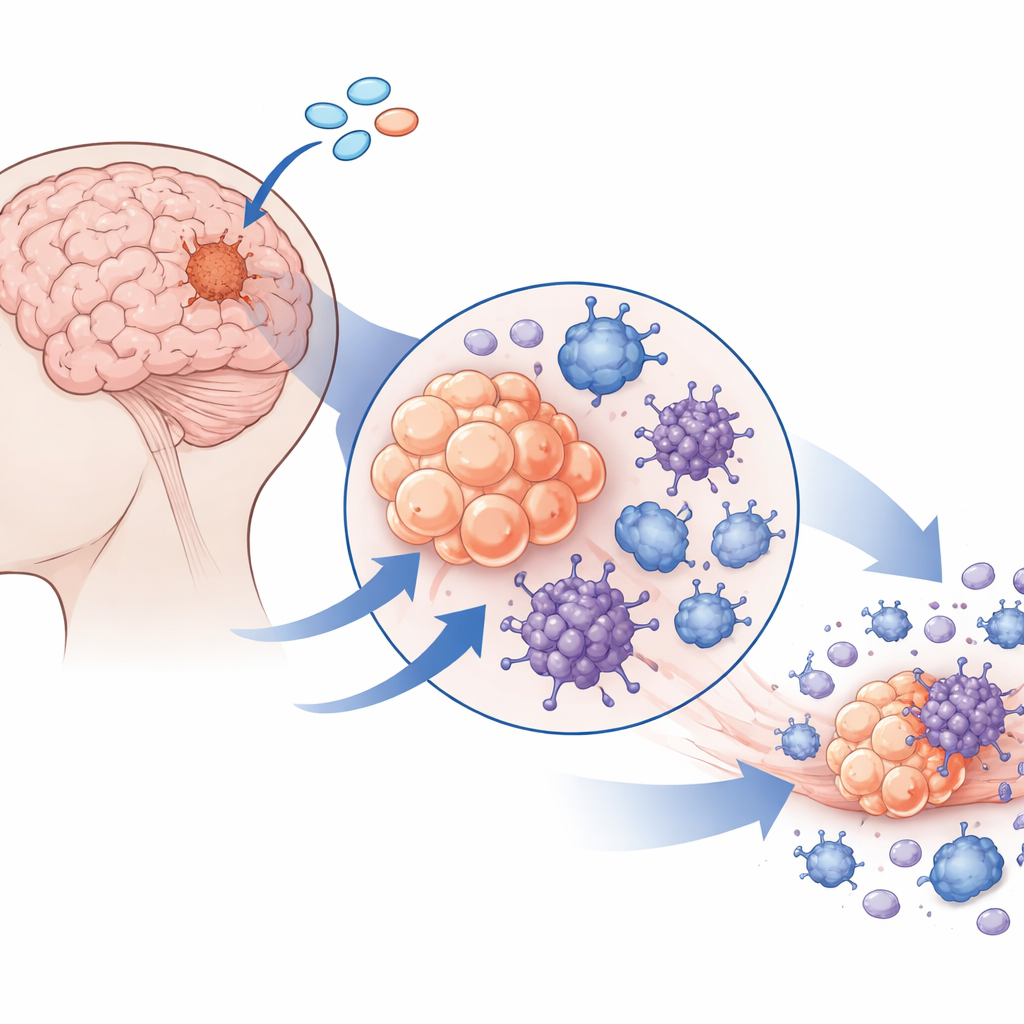
发现肿瘤细胞仍保留的开关
接着,研究团队寻找可能将这种抑制性状态转为炎性、敌对肿瘤环境的通路。他们关注STING——一种通常对细胞内错位DNA作出反应并触发抗病毒和炎性反应的感受器。与许多其他脑肿瘤不同,脑膜瘤细胞表现出异常高的STING表达。这归因于STING基因处于开放染色质状态且DNA甲基化水平较低,表明该基因在表观遗传上处于易被激活的状态。STING不仅在肿瘤细胞中丰富,也存在于附近的血管细胞和巨噬细胞中,这提示一种单一药物可能同时影响肿瘤微环境中的多个关键参与者。
将肿瘤细胞逼入炽烈的自我毁灭
研究者用一种名为8803的强效STING激动剂处理新鲜切除的患者脑膜瘤样本。即便将免疫细胞去除,肿瘤细胞仍然死亡,证明了其直接作用。通过加入选择性阻断不同细胞死亡通路的药物,并读取基因活性,他们表明8803并非简单诱导安静的凋亡。相反,它促使脑膜瘤细胞进入多种炎性死亡形式——焦亡(pyroptosis)、坏死性凋亡(necroptosis)和铁死亡(ferroptosis),这些方式使细胞破裂而非整齐分解。关键步骤包括气体胀蛋白D(gasdermin D)的激活和裂解,该蛋白在细胞膜上形成孔洞。电子显微镜显示肿瘤细胞遍布膜孔和受损线粒体,阻断活性氧可减少细胞被杀,表明线粒体应激与这种炽烈的死亡相关联。
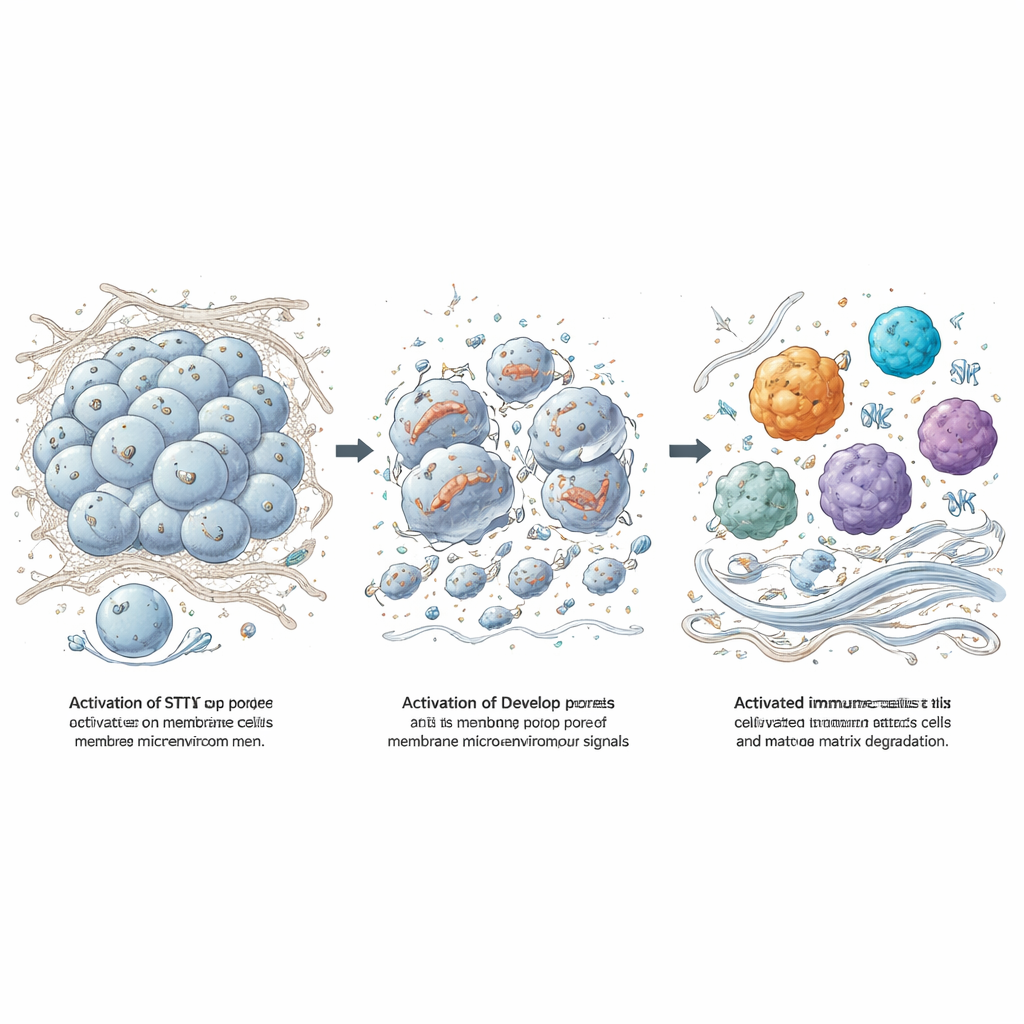
从肿瘤碎片到免疫觉醒与基质侵蚀
当肿瘤细胞以这种剧烈方式死亡时,会释放能够唤醒免疫细胞的“危险”分子。团队将裂解的脑膜瘤细胞暴露给小鼠巨噬细胞,观察到炎性因子和降解胶原的酶,尤其是基质金属蛋白酶-3(MMP-3)的显著上升。通过使用缺失特定信号适配子的鼠模型,他们显示了Toll样受体(另一类危险感应系统)对这种反应至关重要,而8803所激活的STING又为免疫刺激增添了自身的层面。在小鼠脑膜瘤模型中,直接将8803注入肿瘤可缩小或稳定肿瘤生长、延长生存,并将肿瘤部位从一个沉寂、富含胶原的肿块转变为充满活跃巨噬细胞、NK细胞和T细胞且胶原染色明显减少的区域。
为何这一策略可能改变临床治疗
总体而言,该研究表明脑膜瘤存在一种内在弱点:其肿瘤细胞保留一个可被访问的STING开关,当被8803触发时,会驱使它们进入爆炸性、炎性的细胞死亡。这一过程既能直接杀死癌细胞,也能将大量警报信号注入周围环境,从而招募并激活免疫细胞,同时有助于侵蚀那种导致占位效应的胶原支架。因为脑膜瘤通常是局限性的而非广泛转移,且复发疾病的标准治疗选择有限,局部给药的STING激动剂如8803或可提供一种新的、有针对性的方法,既减小肿瘤体积又重塑其免疫微环境,以期实现持久控制。
引用: Youngblood, M.W., Tripathi, S., Najem, H. et al. STING activation induces cytotoxic and immune responses in meningiomas via inflammatory cell death pathways. Nat Commun 17, 2685 (2026). https://doi.org/10.1038/s41467-026-69296-1
关键词: 脑膜瘤, STING通路, 脑肿瘤免疫治疗, 炎性细胞死亡, 肿瘤微环境