Clear Sky Science · zh
基于可解释人工智能的人体胰腺切片分析识别2型糖尿病特征
这项研究对日常健康的重要性
2型糖尿病影响数以亿计的人口,但临床医生仍然难以在产生胰岛素的胰腺内看到明确的、可识别的疾病体征。本研究将强大的人工智能与先进显微成像结合,用以读取人类胰腺组织中肉眼看不见的细微模式。通过这种方式,研究揭示了与2型糖尿病相关的新结构性特征,并为诊断、预防和治疗提供了新的思路。
以前所未有的细节观察胰腺
传统上,科学家们检视的是来自已故供体的胰腺组织,以寻找与2型糖尿病相关的改变,例如瘢痕化、脂肪沉积或胰岛素产生细胞的丧失。这些研究列出过许多可能的异常,但没有一种足够可靠,使病理学家仅凭显微镜切片就能自信地判断个体是否患有糖尿病。在这项工作中,研究者汇集了一套独特的超高分辨率图像,来源于100名活体手术供体的胰腺样本,其中35名为2型糖尿病患者,65名为非糖尿病者。每个样本都进行了多重染色,以突出不同的细胞类型:胰岛内的激素产生细胞、血管、脂肪细胞和神经纤维。这个丰富的视觉数据集复杂到人类无法完全处理,而这正是人工智能擅长的领域。 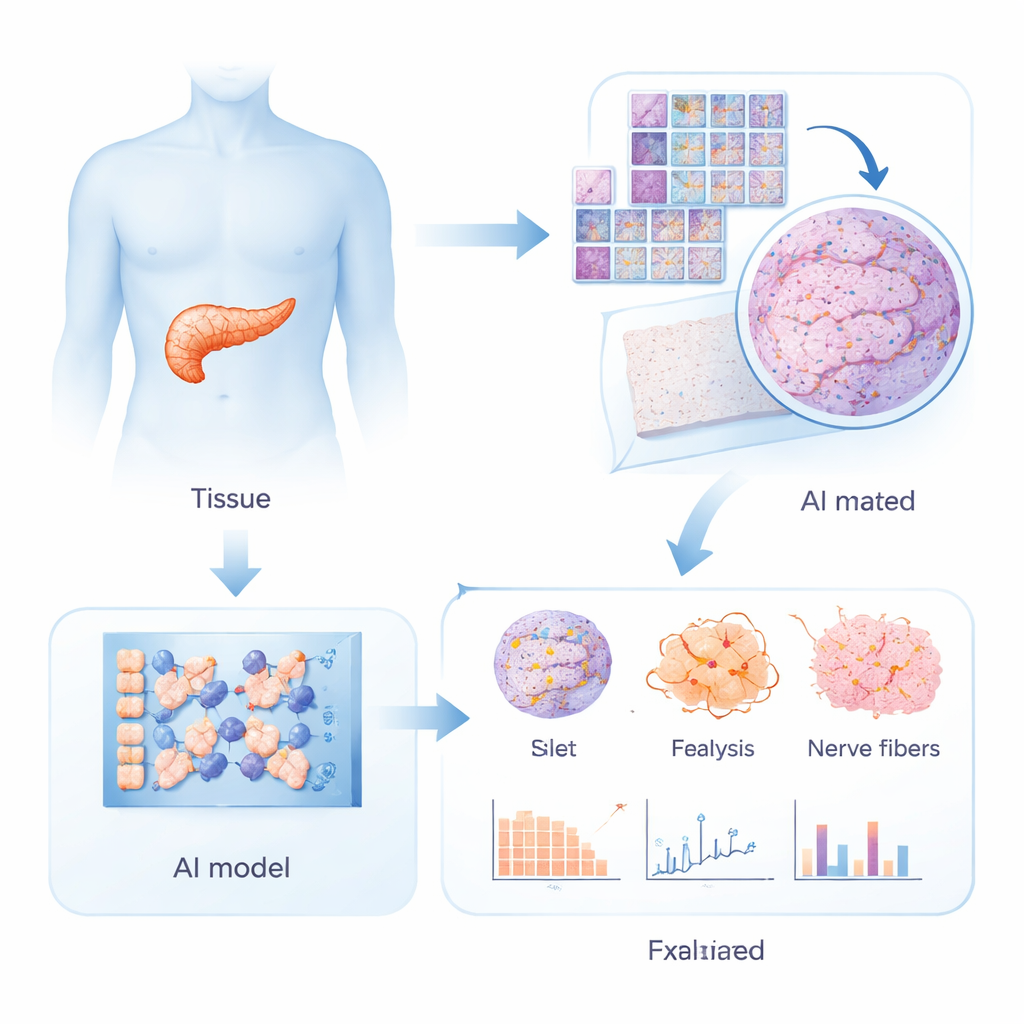
训练AI识别糖尿病胰腺
团队训练了深度学习模型来区分来自有无2型糖尿病者的组织。由于每张整片图像包含数十亿像素,他们首先将切片分割为许多小补丁。一个预训练的视觉变换器(vision transformer)从每个补丁中提取特征,随后一个专门的“多实例学习”分类器整合来自整张切片的补丁信息,以判断该切片是否来自糖尿病或非糖尿病供体。为避免过拟合,他们采用重复交叉验证,并对15个独立模型的预测取平均。表现最佳的是同时标记α细胞、δ细胞和神经纤维的多重荧光图像,其受试者工作特征曲线下面积(AUC)达到0.956——这是AI能够可靠“看见”病理学家尚未形式化的糖尿病相关模式的有力证据。
让黑箱自己解释
然而,单纯预测并非目的;作者们追求生物学见解。因此他们应用了可解释人工智能技术,以显示模型在做出决定时依赖的区域和像素。注意力图在整张切片上突出最具影响力的区域,而归因方法则缩小到单个细胞和结构的层级。为了将这些彩色热图转化为可量化的数据,团队训练了独立的分割网络,能够自动描绘胰岛、脂肪细胞簇和结缔(纤维化)组织的轮廓。随后他们量化了胰岛大小、脂肪总面积、脂肪簇数、胰岛与邻近脂肪的距离以及纤维化组织的程度等特征,并在考虑年龄、性别、身体质量指数和其他临床因素的情况下,分析这些“组织学生物标志物”与糖尿病状态和胰岛素分泌之间的关联。 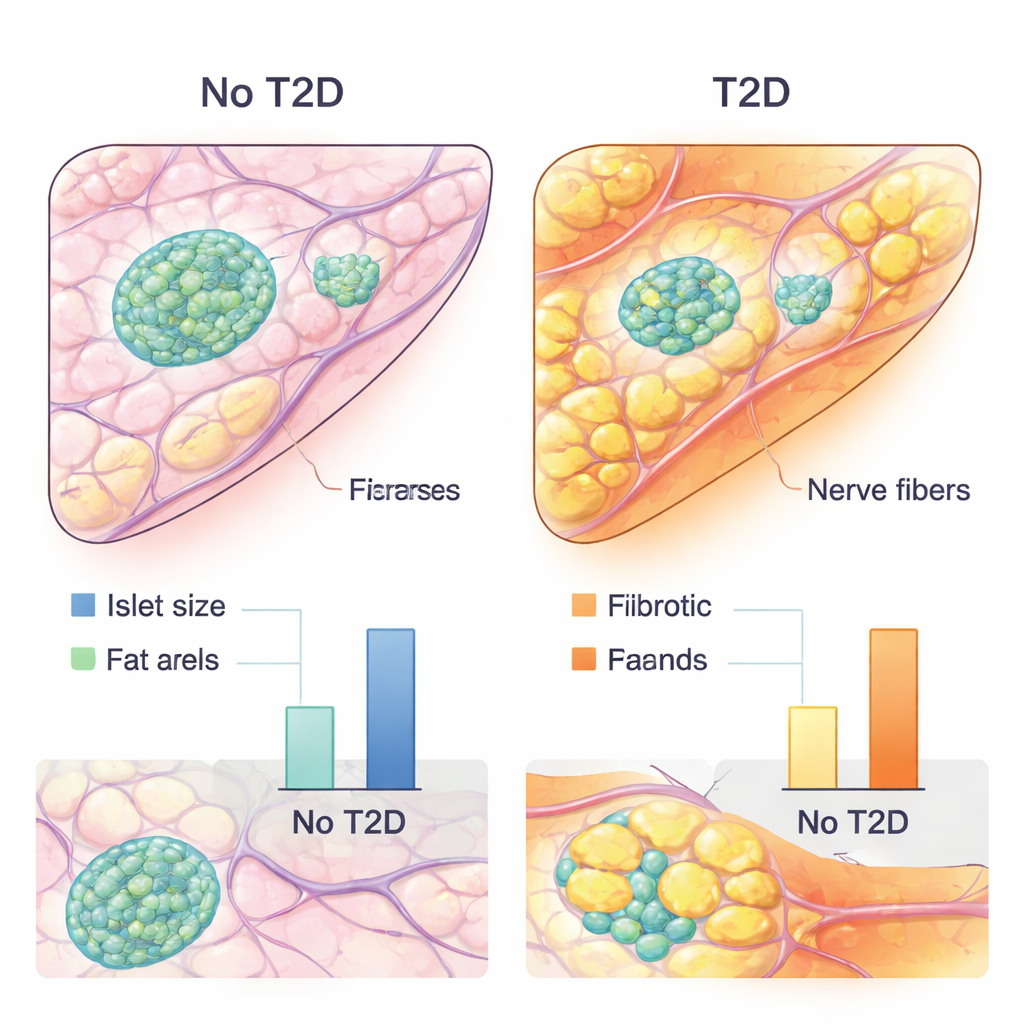
新的线索:脂肪、神经、瘢痕与缩小的胰岛
基于AI的分析揭示了若干与糖尿病胰腺一致的特征。患2型糖尿病的人倾向于具有更小的胰岛和胰腺内部更大的脂肪细胞簇。重要的是,糖尿病供体的胰岛更靠近这些脂肪沉积,提示脂肪组织对激素产生细胞有更直接的局部影响。糖尿病患者的结缔样、瘢痕样组织量也更高,并且与较差的胰岛素分泌相关。同时,AI模型对标记微管蛋白β3(tubulin beta 3,一种神经纤维标志物)染色的结构给予了出人意料的强烈权重,尤其是当这些纤维穿过或位于胰岛附近时。这提示胰腺神经支配——神经与胰岛细胞的接口方式——发生改变,可能是2型糖尿病一个重要且被低估的贡献因子。综上,这些发现表明关键的不仅是β细胞本身,周围环境——邻近的脂肪细胞、瘢痕、血管和神经——都似乎影响着胰岛的健康。
对未来护理的意义
对非专业读者而言,核心信息是:2型糖尿病在胰腺结构上留下了微妙但可检测的印记。通过将高分辨率成像与可解释的人工智能相结合,本研究把这些模式转化为可测量的特征——例如胰岛大小、脂肪分布、神经存在与纤维化程度——这些特征与糖尿病以及机体仍能产生胰岛素的能力相关。尽管该方法尚不能作为常规临床诊断工具,它为发现新的药物靶点和细化我们对糖尿病发生机制的理解提供了强有力的路线图。长期来看,来自此类AI引导的组织分析的见解可能有助于医生更好地预测高风险人群、监测疾病进展,并设计不仅保护β细胞而且保护胰腺周围环境的治疗策略。
引用: Klein, L., Ziegler, S., Gerst, F. et al. Explainable AI-based analysis of human pancreas sections identifies traits of type 2 diabetes. Nat Commun 17, 1558 (2026). https://doi.org/10.1038/s41467-026-69295-2
关键词: 2型糖尿病, 胰腺, 人工智能, 组织病理学, 生物标志物