Clear Sky Science · zh
急性坏死性脑病的遗传驱动因子 RANBP2 调控流感 A 病毒感染诱发的炎性反应
当流感损害大脑时
大多数人把流感看作一周左右的发烧、咳嗽和卧床休息。但在少数情况下,尤其是儿童,一次常见的流感感染可能突然演变为危及生命的脑部疾病——急性坏死性脑病(ANE)。长期以来,家庭和临床医生就怀疑基因会影响谁会发生这种灾难性并发症。本研究揭示了单个细胞“守门人”蛋白 RANBP2 通常如何抑制流感病毒,并防止机体的炎症反应失控。
罕见但毁灭性的流感并发症
ANE 在发热性疾病(常为流感)后突然出现,可迅速导致癫痫发作、昏迷和长期神经功能损伤。全球已有约一半已知的 ANE 病例与甲型流感病毒有关,尤其是 H1N1 亚型。携带 RANBP2 基因某些变异的儿童发生这种被称为 ANE1 的病症风险显著增加。然而直到现在,科学家们尚不清楚该蛋白在流感感染期间具体执行何种功能,以及其改变为何会使大脑内的炎症如此严重。
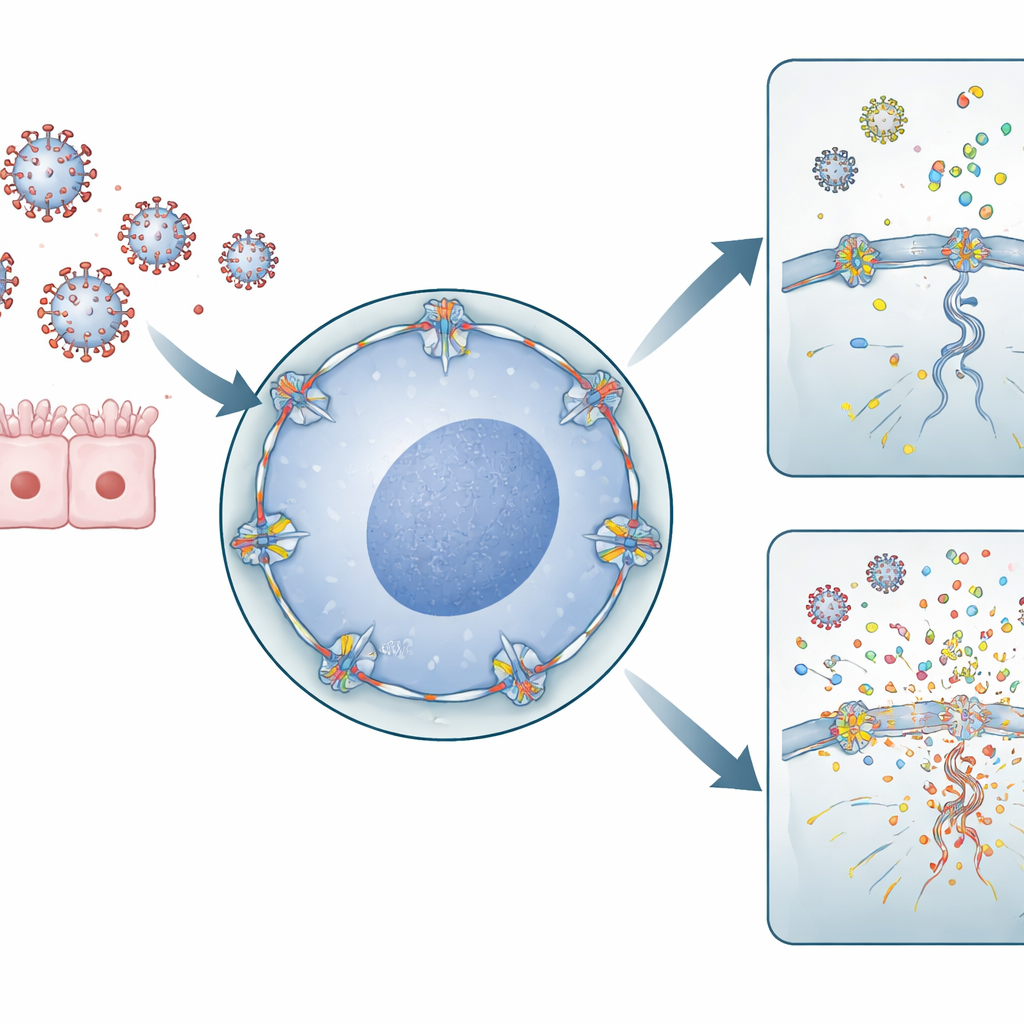
细胞闸门与病毒基因组
甲型流感病毒对于 RNA 病毒来说生活方式有些特殊:它必须进入细胞核才能复制其遗传物质。为此,病毒通过核孔——核包膜上的大型通道,控制核与胞质之间的物质进出。RANBP2 是这些核孔外侧的重要组成部分。作者使用来自人类肺的细胞和免疫细胞,降低 RANBP2 水平或引入与 ANE 相关的突变。他们发现,当 RANBP2 缺失或位置异常时,流感基因组在细胞核内的复制增多,且病毒遗传片段以不平衡的方式被输出到胞质中。出人意料的是,这种额外的病毒 RNA 并没有产生更多可感染的病毒颗粒,但确实改变了病毒物质在细胞内的分布和聚集方式。
当病毒碎片激活警报系统时
免疫系统依赖分子传感器来检测胞质中游离的病毒 RNA 片段,将其识别为危险信号。研究团队表明,在缺乏正常 RANBP2 的细胞中,额外的病毒 RNA 片段在胞质中堆积,恰好形成这些传感器能够识别的模式。在肺来源细胞中,这触发了更高水平的炎性分子,如 IL‑6 和 IL‑1β。在来自供体血液的一次性人源巨噬细胞——作为前线免疫细胞——中,RANBP2 缺失导致促炎趋化因子显著上升,包括 CXCL8、CXCL10、CCL2、CCL3 和 CCL4。这些化学信使招募并激活更多免疫细胞,从而放大整体的感染应答。
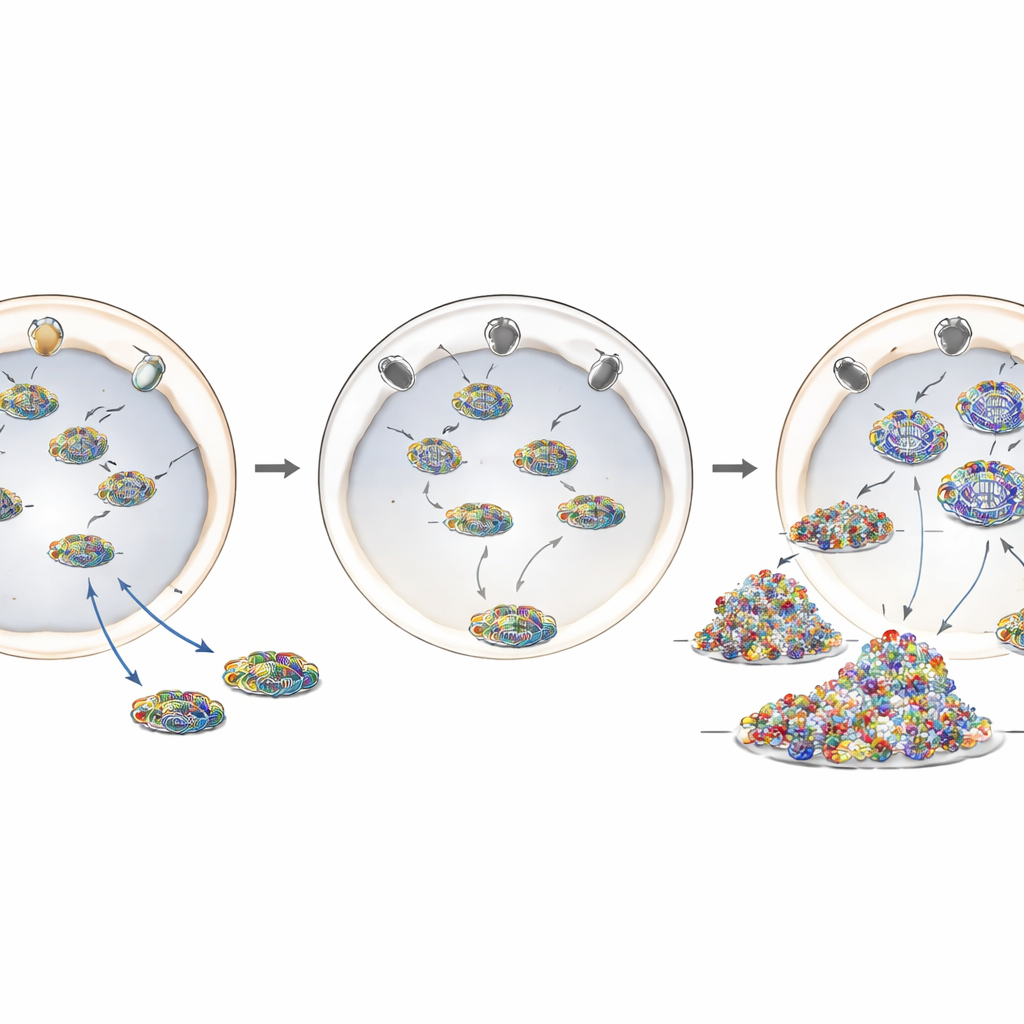
将守护蛋白错位的致病突变
为更贴近模型化 ANE1,研究者使用 CRISPR‑Cas9 基因组编辑将最常见的致病变异 T585M 引入人类 RANBP2 基因。在这些编辑细胞中,RANBP2 蛋白的总体含量大体正常,但其定位异常:蛋白未能在核包膜周围形成明亮的环状分布,反而大量错位到细胞内部。携带该突变的细胞(无论为单拷贝还是双拷贝)表现与 RANBP2 缺失细胞类似。它们支持更高水平的流感基因组复制,胞质中出现更多病毒物质,并在感染后产生更强烈的炎性反应。这表明,将 RANBP2 正确定位于核孔——而非其总体丰度——对其保护性作用至关重要。
这对有风险儿童意味着什么
综上所述,这些发现将 RANBP2 描绘为一位在细胞内微调流感遗传物质进出核区的守护者。当 RANBP2 缺失或定位异常时,病毒 RNA 出现过度复制并以混乱的方式被导出,导致胞质充斥分子碎片,从而大幅加剧免疫信号。在大多数组织中,这可能意味着更严重但可存活的流感病程。然而对于具有 ANE1 易感性的儿童,这种失控的炎症——特别是一旦波及大脑——或可解释为何在原本平常的感染后出现突发且严重的神经损伤。理解这一通路有助于未来早期识别高危患者并在免疫反应从保护性转为破坏性之前,制定针对性的抗炎治疗策略。
引用: Desgraupes, S., Decorsière, A., Perrin, S. et al. The genetic driver of Acute Necrotizing Encephalopathy, RANBP2, regulates the inflammatory response to Influenza A virus infection. Nat Commun 17, 2427 (2026). https://doi.org/10.1038/s41467-026-69288-1
关键词: 流感, 急性坏死性脑病, RANBP2, 过度炎症, 核孔