Clear Sky Science · zh
冷凝素–调节子相互作用在有丝分裂染色体组织中的作用
分裂中的细胞如何保持其遗传“家务”有序
每次细胞分裂时,都必须小心地打包并分离米级长度的DNA,以便每个子细胞获得一套完整的染色体。当这一过程出错时,可能导致细胞死亡、发育障碍或癌症。本研究揭示了两台主要分子机器——一台控制基因活性、另一台压缩DNA——如何协同工作,在细胞分裂期间折叠染色体,揭示了有丝分裂期间哪些基因被激活与染色体能否忠实分配之间的隐含联系。
关键角色:打包者与协调者
在细胞核内,一个名为冷凝素的蛋白复合体充当分子打包者,通过形成环状并收紧DNA,将其压缩成在有丝分裂中可见的粗壮染色体。另一个大型复合体——调节子(mediator)——通过与将DNA转录为RNA的RNA聚合酶协同工作,帮助控制基因的开启或关闭。作者在裂殖酵母(一种被广泛使用且其染色体生物学与人类细胞极为相似的模式生物)中研究了这些复合体。他们发现冷凝素的一个亚基Cnd1能与调节子亚基Pmc4发生物理结合。这种相互作用发生在高度活跃的基因处以及一组仅在有丝分裂期间被激活的特殊基因上。这些“有丝分裂基因”位于大型染色体邻域或结构域的边缘,似乎充当边界标记。
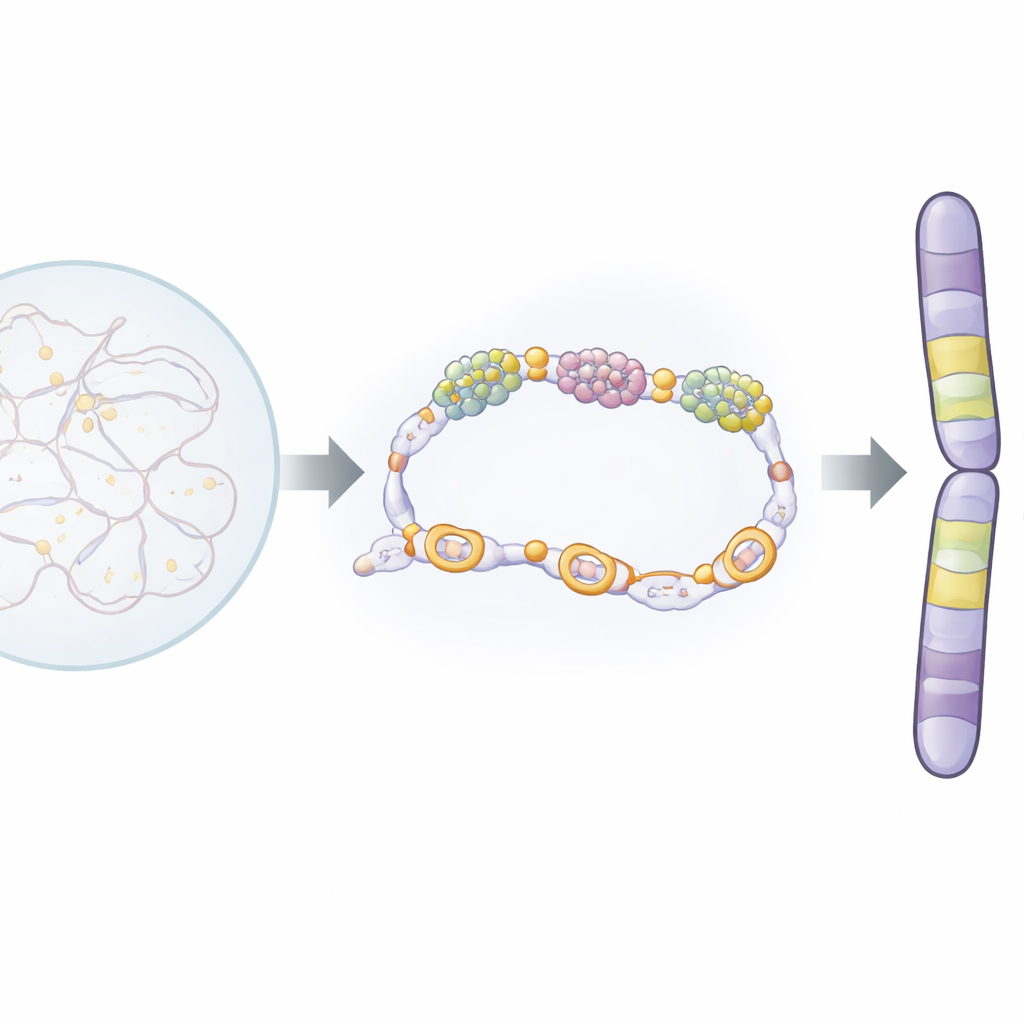
一次分子握手带来的重大后果
为检验这次握手的重要性,研究人员在Cnd1中设计了一个非常精确的突变,仅改变一个氨基酸(K658E),使Cnd1无法再与Pmc4结合,同时仍能形成正常的冷凝素复合体。携带该突变的酵母细胞能存活,但其染色体更频繁地分离错误,在有丝分裂期间出现滞后DNA片段。通过三维基因组绘制(Hi-C)和选定DNA位点之间的显微镜距离测量,团队表明突变细胞的冷凝素驱动接触减弱,染色体结构域的压缩程度下降。换言之,缺乏恰当的Cnd1–Pmc4相互作用时,冷凝素无法在细胞分裂期间高效将染色体折叠成稳固的、基于结构域的构象。
基因活性作为边界构建者
随后研究探讨了调节子如何参与此折叠过程。当Pmc4被耗竭时,许多基因处的冷凝素结合减少,冷凝素构建的结构域强度下降。显著的是,相邻结构域之间的边界变得模糊,DNA相互作用开始跨越原本清晰的边界。详尽的RNA测量显示,Pmc4缺失显著降低了一组由转录因子Ace2控制的有丝分裂激活基因的表达。这些边界基因通常显示出调节子、冷凝素以及一种称为TBP的基础转录因子高度富集。数据支持这样一个模型:调节子和TBP首先将冷凝素招募到高度活跃和有丝分裂基因的启动子;随着转录进行,冷凝素被沿基因体推移,帮助将邻近DNA编织成环路,而Ace2靶基因则划定每个凝缩结构域的边界。
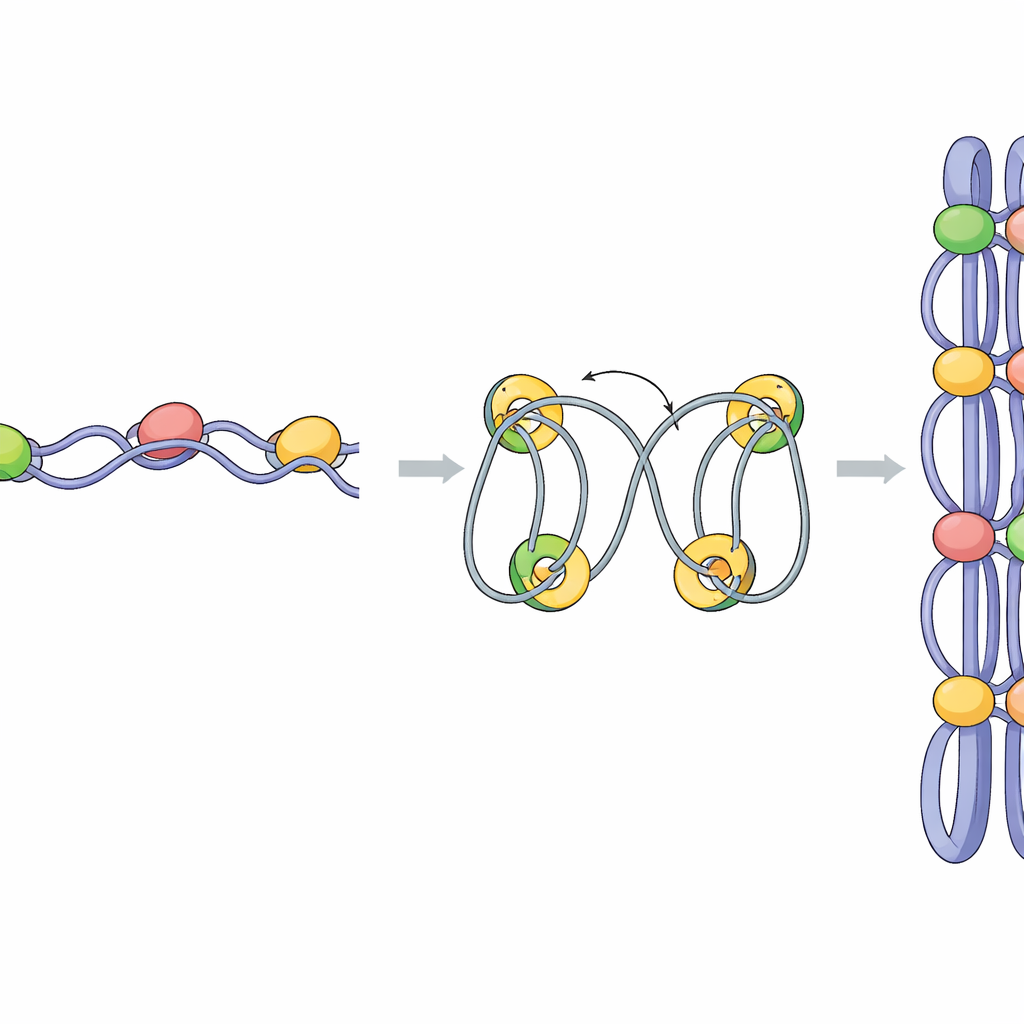
液滴状结构可能发挥的作用
在人类细胞中已知调节子可以通过相分离形成类液滴,这一过程可在细胞核中浓缩转录机器。作者发现裂殖酵母的调节子行为类似:Pmc4亚基在试管中可形成液滴,而用1,6-己二醇(一种能破坏此类凝聚体的化学物质)处理细胞,会迅速使细胞核中的调节子焦点消散。温和的己二醇处理削弱了关键基因处调节子和冷凝素的结合,并特异性地模糊了染色体结构域之间的边界,尽管整体染色体的压缩仍在进行。这表明位于有丝分裂边界基因处的调节子富集液滴可能通过将转录和冷凝素加载集中到这些位点,帮助确定结构域的起止位置。
从酵母教训到人类健康
最后,团队探查了人类细胞中是否存在类似的伙伴关系。通过相互作用测定,他们发现人类的MED4(Pmc4的对等物)能特异性地与CAP-D3(一种与酵母Cnd1密切相关的冷凝素II亚基)结合。人类CAP-D3中相当于酵母K658E的突变破坏了这种相互作用,并导致有丝分裂错误,例如染色体错位和微核形成。耗竭MED4也产生了分离缺陷。这些相似性表明,调节子与冷凝素之间的耦合是细胞将基因活性与染色体折叠协调起来的一种保守策略,确保DNA在细胞分裂时被整齐打包并均等分配。
为什么这对理解疾病很重要
这项工作表明,有丝分裂期间染色体的折叠并非仅靠强行压缩来实现。相反,它依赖于特定基因在何时何地被激活:调节子驱动的边界基因转录将冷凝素招募到这些位点,从而塑造大尺度的结构域。通过展示两个复合体之间的单一相互作用如何扩展并影响整条染色体的构象及分离准确性,这项研究为思考基因调控机械或冷凝素功能的微小变化如何导致染色体不稳定(许多癌症和遗传病的标志)提供了框架。
引用: Iwasaki, O., Tashiro, S., Chung, C.YL. et al. A role for condensin-mediator interaction in mitotic chromosome organization. Nat Commun 17, 2509 (2026). https://doi.org/10.1038/s41467-026-69270-x
关键词: 染色体结构, 冷凝素, 调节子复合体, 有丝分裂, 三维基因组组织