Clear Sky Science · zh
降解登革热病毒衣壳蛋白的分子在药理学上不同于衣壳抑制剂
将病毒的外壳变成对付它自己的武器
登革热每年感染数亿人,但医生仍缺乏可靠的抗病毒药物来治疗它。这项研究探讨了一种新的解除登革热毒性的途径:在受感染细胞内摧毁病毒的关键构件,而不是仅仅尝试阻断其功能。研究表明,经过精心设计的分子可以将关键病毒蛋白标记为细胞自身垃圾处理系统的处置对象,从而减少病毒产生并削弱其躲避免疫防御的能力。
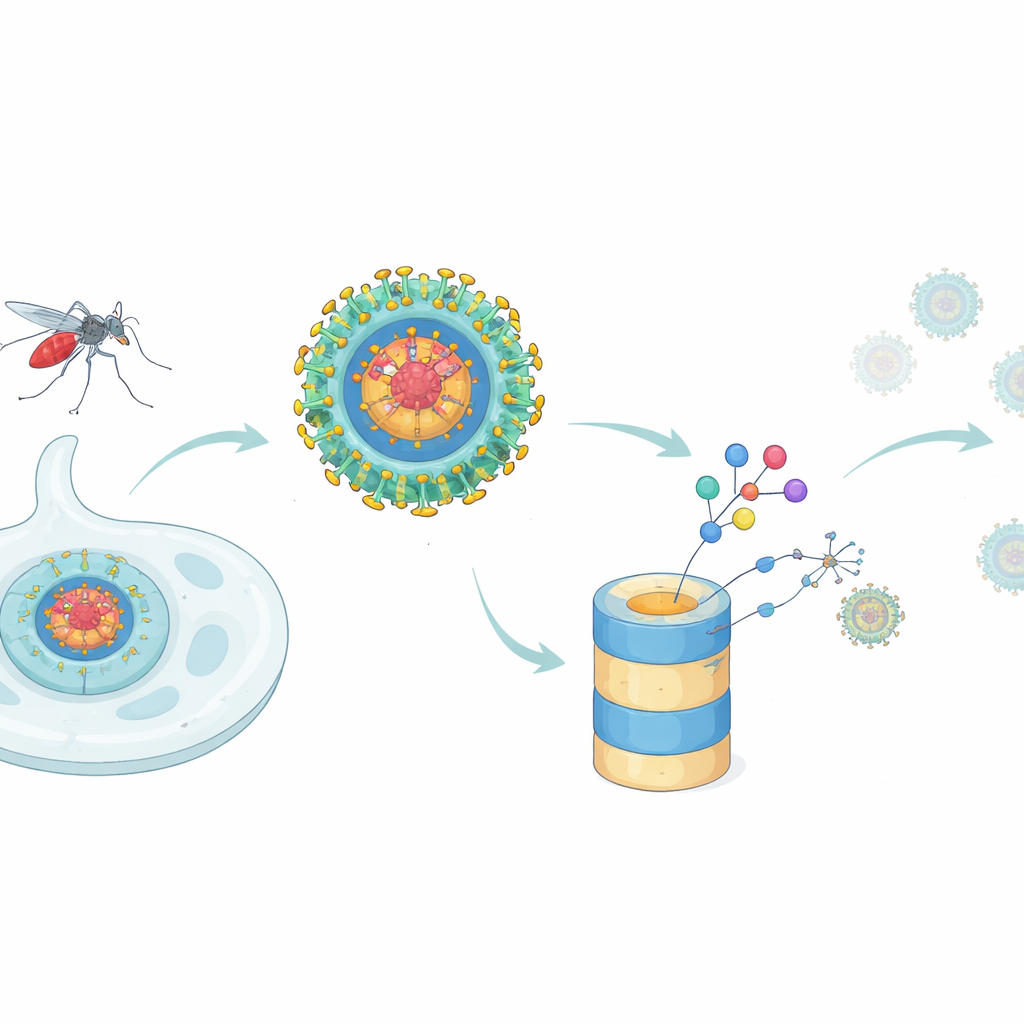
阻止登革热的新策略
大多数抗病毒药物的作用类似于机器里的塞子:它们占据病毒蛋白的一个功能位点并试图阻断其作用。当单个病毒蛋白承担多种任务,或当微小突变削弱药物结合力时,这种方法就会遇到困难。登革热的衣壳蛋白就是一个典型例子。它构成包裹病毒遗传物质的新颗粒的核心外壳,但也通过与多种人类蛋白相互作用并抑制机体的干扰素反应(先天抗病毒警报)来干扰宿主细胞。作者们提出,较新的药物概念——靶向蛋白降解——是否能够超越经典抑制剂,通过将衣壳蛋白从受感染细胞中实际移除来发挥作用。
设计一种分子“赏金猎人”
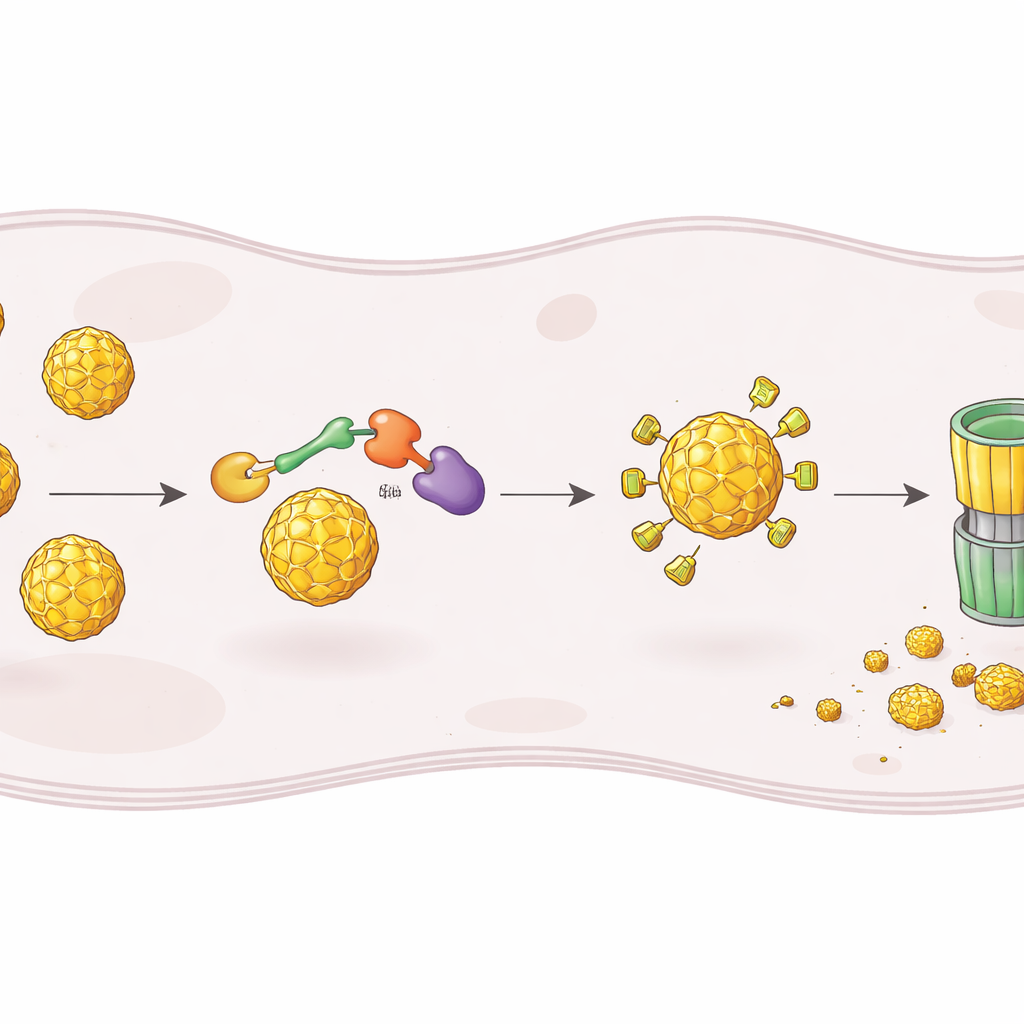
为构建这样的降解剂,研究人员从已知的小分子ST148入手,该分子能与登革热衣壳结合并干扰新病毒颗粒的装配。他们将ST148化学连接到第二个模组,该模组能够招募负责标记蛋白质以便降解的人体酶复合体。由此产生的嵌合分子称为PROTACs,其结构使一端抓住衣壳,另一端招募E3连接酶复合体,将二者拉到一起,使衣壳被泛素标记并送入细胞的蛋白酶体——主要的蛋白质粉碎机。通过测试多种连接子长度和招募不同E3配体,他们鉴定出一款表现突出的化合物,命名为RPG‑01‑132,在受感染细胞中能可靠地降低衣壳水平,其作用依赖于CRBN形式的E3连接酶和正常的蛋白酶体功能。
关闭病毒产生与免疫逃逸
在获得有效降解剂后,团队评估了它对登革热感染的实际影响。在感染登革热病毒的肝源性细胞中,RPG‑01‑132在能够仅部分降低总体衣壳水平的浓度下,就引起了释放的具感染性病毒数量显著下降。重要的是,其他病毒蛋白和病毒RNA保持不变,表明该化合物并非简单地毒害整体复制,而是通过导致衣壳丧失而发挥特异性作用。电子显微镜提供了直观证据:用原始抑制剂ST148处理的细胞在内质网中积累了部分形成的病毒颗粒堆积,符合装配受阻的情况;而用降解剂处理的细胞几乎看不到可见的病毒颗粒。降解剂还在报告系统中缓解了衣壳抑制干扰素‑β信号的能力,提示通过降解衣壳可以逆转其在削弱先天免疫中的非结构性作用。
应对病毒多样性与耐药性
登革热病毒有四个主要血清型,它们对针对衣壳的抑制剂的敏感性各不相同,且单个突变就能产生耐药性。作者将降解剂与ST148在代表性四个血清型的菌株以及携带已知使ST148失效突变(衣壳S34L)的病毒上进行了比较。如预期,ST148在某一血清型上效果最佳,并且在耐药突变上失去活性。相比之下,RPG‑01‑132在所有血清型上表现出相似的抗病毒效力,并在S34L突变体上保留活性,同时仍通过相同的CRBN依赖性降解途径发挥作用。这说明了“事件驱动”药理学的关键优势:降解剂不需要始终紧紧结合每一个衣壳分子,只要能触发足够多的降解事件以改变平衡即可。
这对未来登革热治疗意味着什么
这项研究表明,登革热的衣壳蛋白不仅可以作为病毒的结构成分被攻击,亦可以作为支持感染多个步骤和免疫逃逸的可移除枢纽来处理。通过将传统抑制剂转化为降解剂,研究人员创造了一种能阻断病毒产生、解除部分病毒对先天免疫的抑制并在不同病毒株和已知耐药突变中保持有效的化合物。RPG‑01‑132本身仍需优化——改进细胞进入能力、在动物模型中增强活性并进行严格的安全性检测——但它提供了一个有说服力的概念验证。更广泛地说,本工作表明劫持细胞自身的处置机制可能为抗病毒药物开辟新途径,使其更难被病毒规避,并能够中和在受感染细胞内承担多种角色的蛋白质。
引用: Chakravarty, A., Wang, LN., Golden, R.P. et al. Degraders of the dengue virus capsid protein exhibit differentiated pharmacology relative to capsid inhibitors. Nat Commun 17, 2594 (2026). https://doi.org/10.1038/s41467-026-69263-w
关键词: 登革热病毒, 衣壳蛋白, 靶向蛋白降解, 抗病毒药物设计, PROTACs