Clear Sky Science · zh
将相分离与成纤维化分离可保留生物分子凝聚体的活性
为何这与大脑健康相关
许多脑部疾病,包括阿尔茨海默症,涉及蛋白质随时间聚集成坚硬的纤维缠结。这些相同的蛋白质也能在细胞内形成较软、类似液滴的结构,帮助组织化学反应,有点像微小的液态工作站。本研究提出了一个关键问题:我们能否在不破坏这些液滴有益日常功能的前提下,阻止它们有害地硬化为纤维?作者展示了一种常见的细胞代谢物——氨基酸L-精氨酸,能对一种与阿尔茨海默相关的关键蛋白Tau做到这一点。
从游离蛋白到微小液滴
在细胞内,某些蛋白并非总与细胞流体均匀混合。相反,它们可以聚集成称为生物分子凝聚体的液滴,表现得像非常软的凝胶或粘稠液体。研究团队关注Tau,这是一种通常帮助构建和稳定微管的蛋白——微管是神经细胞内部像道路一样的中空丝状结构。Tau也以形成淀粉样纤维而臭名昭著,后者是许多神经退行性疾病标志性缠结中的坚硬纤维。为研究Tau液滴随时间的演化,研究者构建了一种改造版本的蛋白,称为SynTag-Tau,它能在实验可操作的时间尺度上形成活性的凝聚体并逐渐老化为淀粉样纤维,且不需使用强烈的助剂。
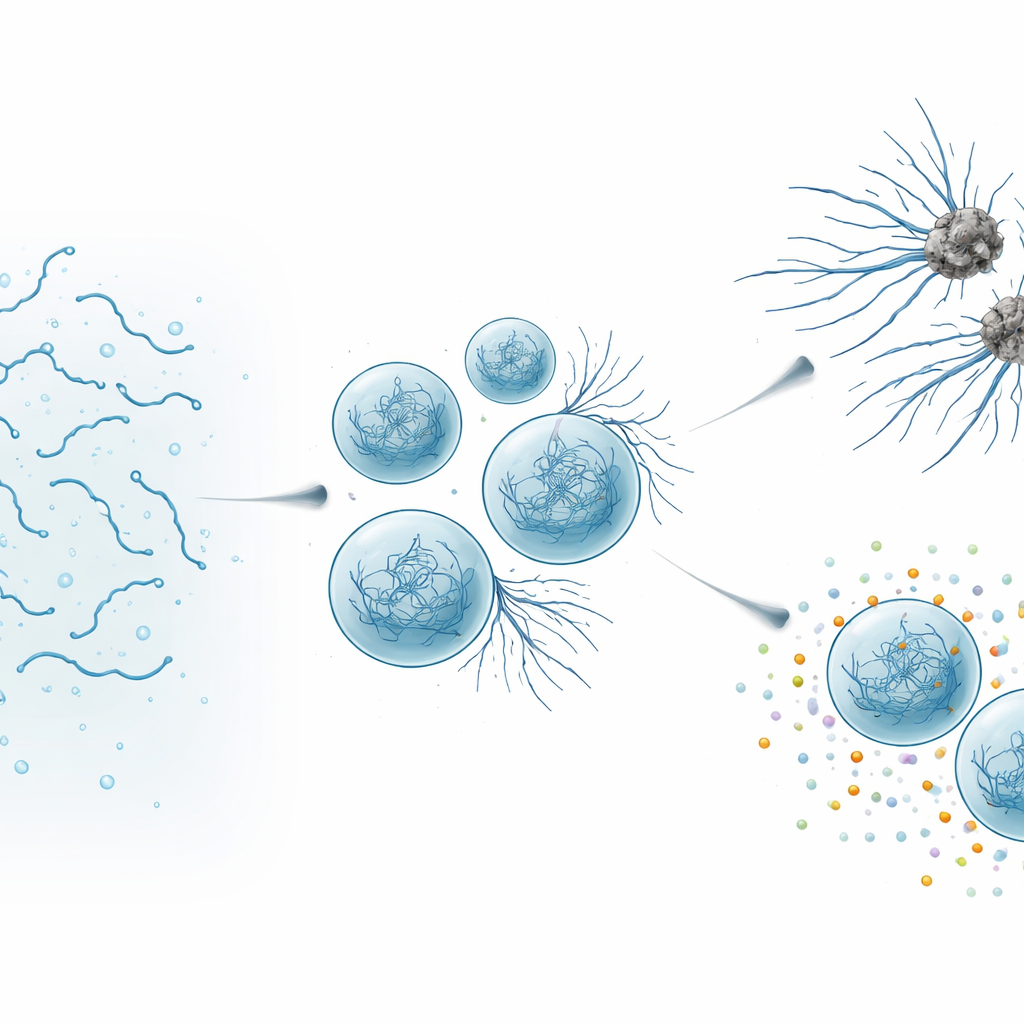
当有益液滴变为有害
通过高分辨率显微镜和生物物理测量,作者们观察到SynTag-Tau液滴在数小时内的变化。新形成的液滴表现得像液体:它们容易融合,分子移动迅速,且没有有序结构的迹象。随时间推移,液滴变得迟缓并变硬,细薄纤维开始从其表面伸展到周围溶液中。敏感的光学方法显示,这些纤维含有典型淀粉样的紧密“交叉-β”构象。重要的是,界面——致密液滴与周围流体之间的边界——成为纤维最先出现的热点。随着液滴老化并长出更多纤维,Tau的正常功能受损:凝聚体吸引微管构建模块管蛋白的能力下降,最终完全失去支持微管组装的能力。
倾斜平衡的小分子
研究者接着探问,是否有简单的代谢物能在不破坏液滴本身的情况下,减缓或阻止这种从液态到纤维的转变。筛选多种天然存在的小分子后,他们发现带正电的氨基酸L-精氨酸和L-赖氨酸在延缓或阻断SynTag-Tau液滴形成淀粉样纤维方面效果显著,且在现实的低毫摩尔浓度下并不抑制液滴形成。相反,带负电的氨基酸如谷氨酸和天冬氨酸则加速了纤维形成,而通常破坏蛋白结构的化学物质要么无效,要么干扰了液滴结构。L-精氨酸的荧光类似物显示,该分子更倾向于停留在Tau凝聚体内部而非外部,提示它在最需要的地方发挥作用。
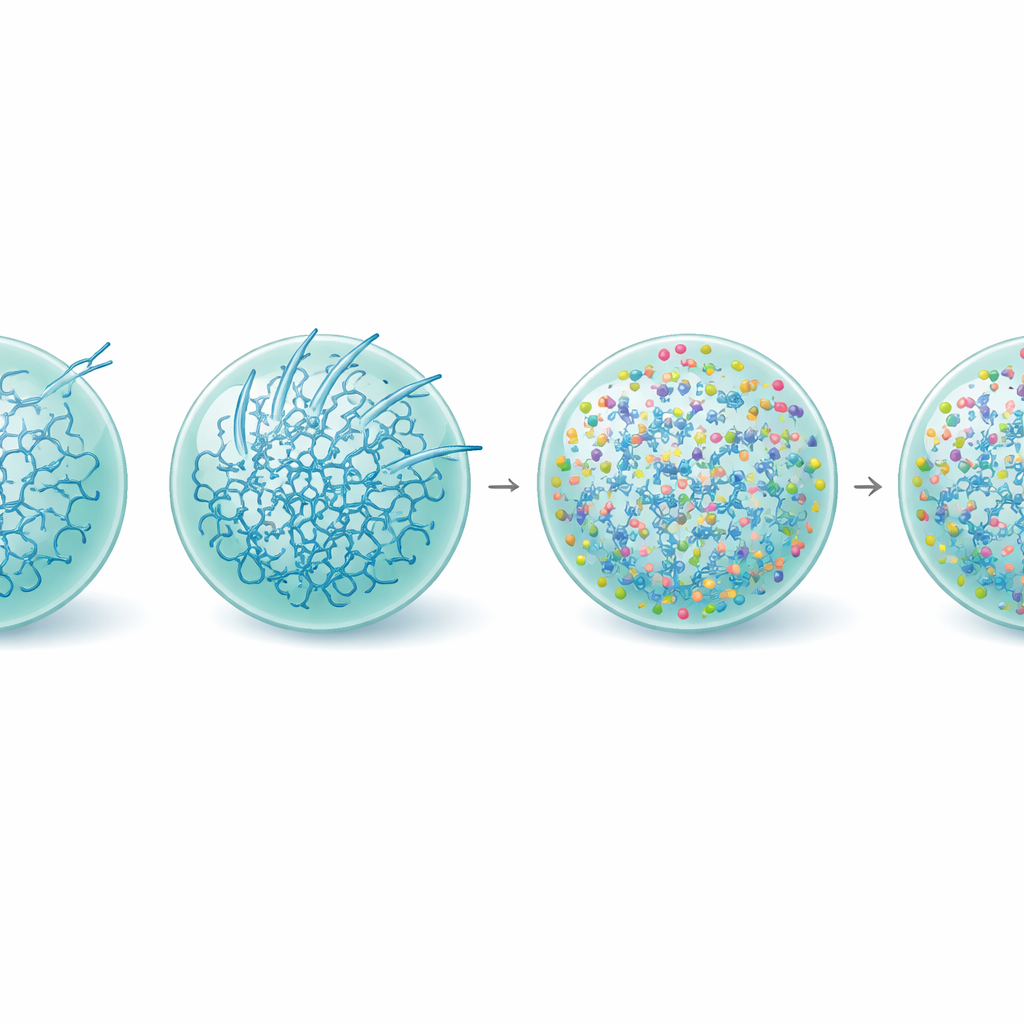
使液滴变刚,保住功能
进一步深入研究表明,L-精氨酸如何重塑Tau液滴内部的状态。蛋白构象测量显示,加入L-精氨酸后,即便在较老的液滴中,采用与淀粉样相关的刚性富β构象的Tau分子比例也减少了。基于视频的纳米流变学——追踪凝聚体内微小颗粒运动——揭示L-精氨酸实际上使Tau液滴更具粘弹性,意味着其内部网络变得更强、更互联,同时仍保持类流体性质。这种增强似乎将系统维持在一种亚稳、功能性的状态,提高了在液滴表面形成纤维的能量障碍。与此一致的是,接受L-精氨酸处理的凝聚体在未经处理的液滴失活很久之后,仍能均匀地招募管蛋白并支持微管生长。
对未来疗法的意义
这项工作表明,驱动蛋白液滴形成的力与驱动有害纤维形成的力相关但可以分离。通过用像L-精氨酸这样的代谢物调整凝聚体内部的化学环境,可以在保留有利的、液态的状态的同时,延缓或阻止向与疾病相关的淀粉样纤维的转变。尽管本研究在体外使用的是一种经特殊设计的Tau体系,但它提供了一个原理性证明:选择性强化凝聚体稳定性的小分子有朝一日可能帮助保护细胞免受有毒蛋白聚集逐渐累积的伤害,同时不阻断生物分子凝聚体的正常组织作用。
引用: Mahendran, T.S., Singh, A., Srinivasan, S. et al. Decoupling phase separation and fibrillization preserves activity of biomolecular condensates. Nat Commun 17, 2841 (2026). https://doi.org/10.1038/s41467-026-69244-z
关键词: Tau 蛋白, 生物分子凝聚体, 淀粉样纤维, L-精氨酸, 神经退行性疾病