Clear Sky Science · zh
人类脆性X病理生理的电生理特征在Fmr1-/y小鼠V1中也存在
为什么脆性X中的脑节律很重要
脆性X综合征是导致智力障碍和自闭症的主要遗传原因之一。家庭和临床医生长期希望,在小鼠中显示出希望的治疗方法能惠及人类,但许多在动物模型中有效的药物在临床试验中未能成功。这项研究提出了一个简单但至关重要的问题:我们能否在人体和小鼠中找到一个共享且可测量的大脑信号,该信号既能反映脆性X的病理变化,又能在治疗作用于大脑时发生改变?
作为大脑窗口的缓慢“怠速”节律
我们的大脑从未真正静止。即便在静息状态下,数十亿神经元也会产生节律性电活动,这些活动可以用放置于头皮的传感器记录为脑电图(EEG)。其中最强的节律之一称为α节律,是一种温和的8–13次/秒的摆动,特别在头后部强烈存在,帮助调节我们处理视觉和听觉的方式。在许多脑部疾病中,包括脆性X、自闭症、精神分裂症等,这种节律都会发生改变。在本研究中,研究者聚焦于脆性X男性患者的α节律与典型发育同龄人有何不同,以及小鼠脆性X模型的视觉皮层中是否存在类似的节律。
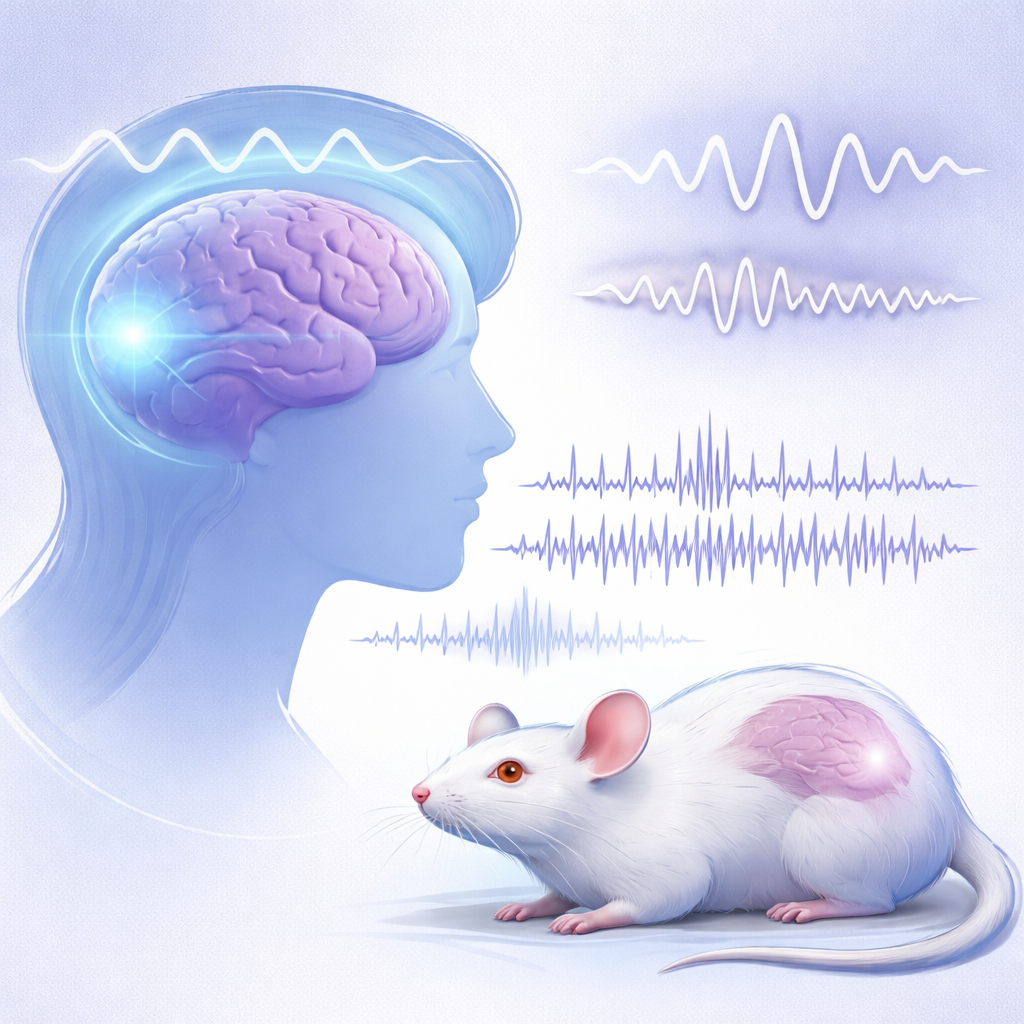
研究者在人类身上观察到的情况
研究团队对患脆性X的男童和男性以及年龄匹配的对照组进行了静息态EEG记录,使用了遍布头皮的大量小电极。研究者没有只看传统的频段,而是将每个人的信号分解为平滑的背景“噪底”和代表真实节律振荡的明显峰值。跨越各个年龄段,脆性X人群的主要低频峰(与α有关)一致地向更慢的频率移动。在儿童群体中,这个类α峰不仅频率更慢,而且幅度也较弱;而在成人中,它明显更慢,但强度大致与对照组相当。追踪显示,这种异常节律最强的来源位于大脑后方的视觉区域,这表明这是与动物模型进行比较的良好靶点。
小鼠视觉皮层中匹配的特征
研究者使用相同的分析方法,随后测量了雄性脆性X小鼠及其健康同窝鼠的视觉皮层活动。小鼠没有典型的人类α频段,但在安静观看灰屏或处于黑暗中时,视觉皮层会出现一个3–6次/秒范围的显著节律。在脆性X小鼠中,这一节律也变慢了,呼应了人类中观察到的改变。当微电极直接置入视觉皮层时,出现了更丰富的细节:主要的低频节律实际上包含两个次峰。较低的次峰表现出脆性X中的减速,而较高的次峰变化仅出现在幼年期,与人类儿童中特定的功率变化相呼应。
节律背后的细胞与化学机制
由于小鼠实验可以直接探测细胞类型和药物作用,研究团队接着探究了哪些神经元和化学信号塑造了这些类α节律。他们发现,特异性地从皮层兴奋性神经元及邻近的支持细胞中去除脆性X蛋白就足以再现异常节律,即便抑制性细胞在遗传上仍然完好无损。通过选择性抑制两大类抑制性细胞——含钙结合蛋白parvalbumin(PV)阳性和含生长抑素somatostatin(SST)阳性中间神经元,研究者表明每一类细胞各自影响节律的不同次峰。随后他们测试了一种药物Arbaclofen,该药增强一种特定类型的抑制性信号(GABAB受体)。在典型小鼠中,该药使低频节律更强且略微变慢,证实了该振荡对药理干预的敏感性。然而在脆性X小鼠中,相同剂量对节律的影响较弱,尽管它们仍能降低过高的高频活动。
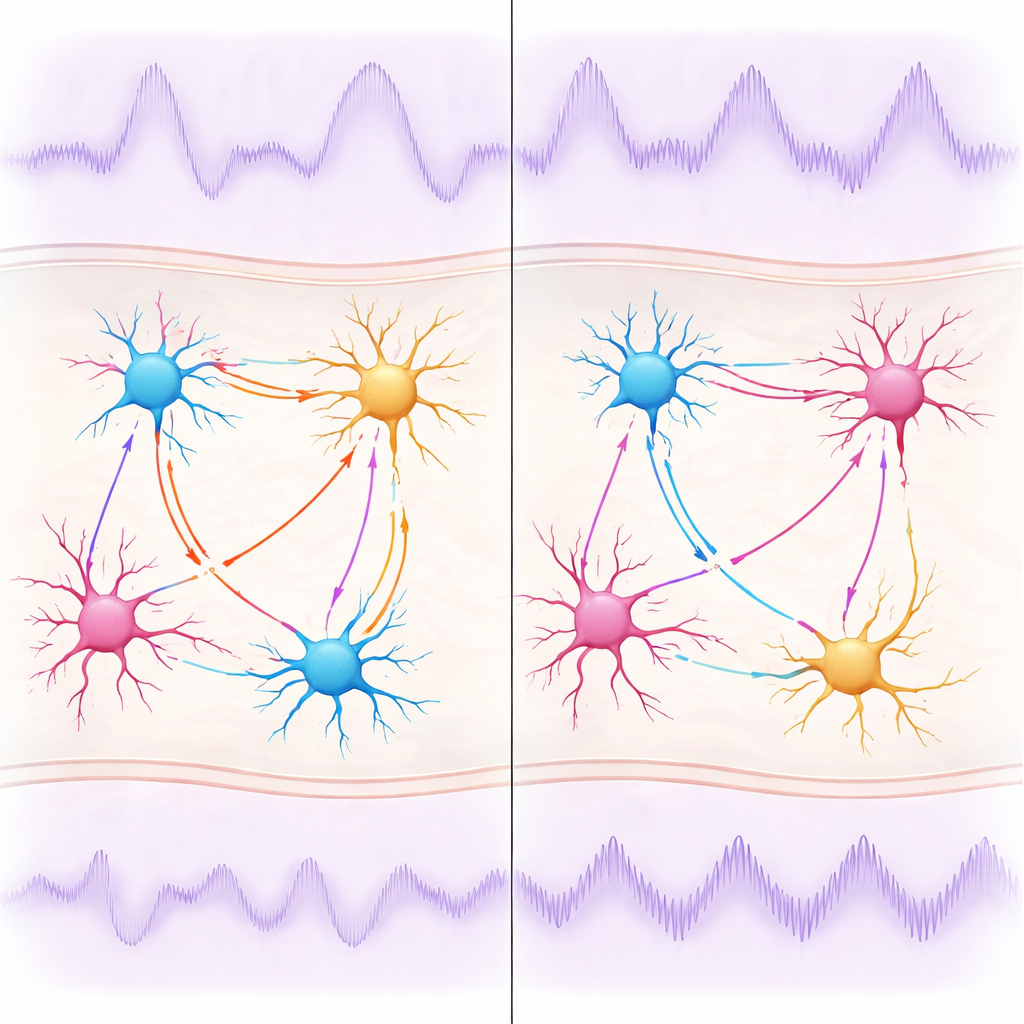
连接实验室小鼠与人类治疗
对非专业读者而言,关键信息是:这项研究识别出一个在脆性X患者和小鼠模型中共同存在的特定脑节律异常,并表明这一信号可以被药物以依赖年龄和基因型的方式改变。放慢的类α节律提供了一个实用的“大脑功能温度计”,可以用相同的方法在人体和小鼠中测量,可能比先前使用的快速脑波更能反映治疗效果。通过将该节律与特定细胞类型和抑制性通路联系起来,这项工作还指向了更有针对性的未来治疗策略,同时有助于解释为何一些早期的药物试验未能从小鼠平移到人类。
引用: Kornfeld-Sylla, S.S., Gelegen, C., Norris, J.E. et al. A human electrophysiological signature of Fragile X pathophysiology is shared in V1 of Fmr1-/y mice. Nat Commun 17, 1497 (2026). https://doi.org/10.1038/s41467-026-69243-0
关键词: 脆性X综合征, 脑节律, α振荡, 视觉皮层, GABA 抑制