Clear Sky Science · zh
GLT25D1 对胶原糖基化的分子基础
微小糖基如何帮助构建坚固组织
胶原是人体中最常见的蛋白质,为皮肤、骨骼、血管及许多其他组织提供支架。但胶原并非孤立发挥作用:它需要在精确的位置被带有小型糖分子的修饰,才能获得合适的强度和柔韧性。本研究以原子级细节揭示了一个关键酶 GLT25D1 如何将特定糖分子附着到胶原上,以及该过程出现故障如何导致血管脆弱、肌肉问题,甚至可能促成癌症。
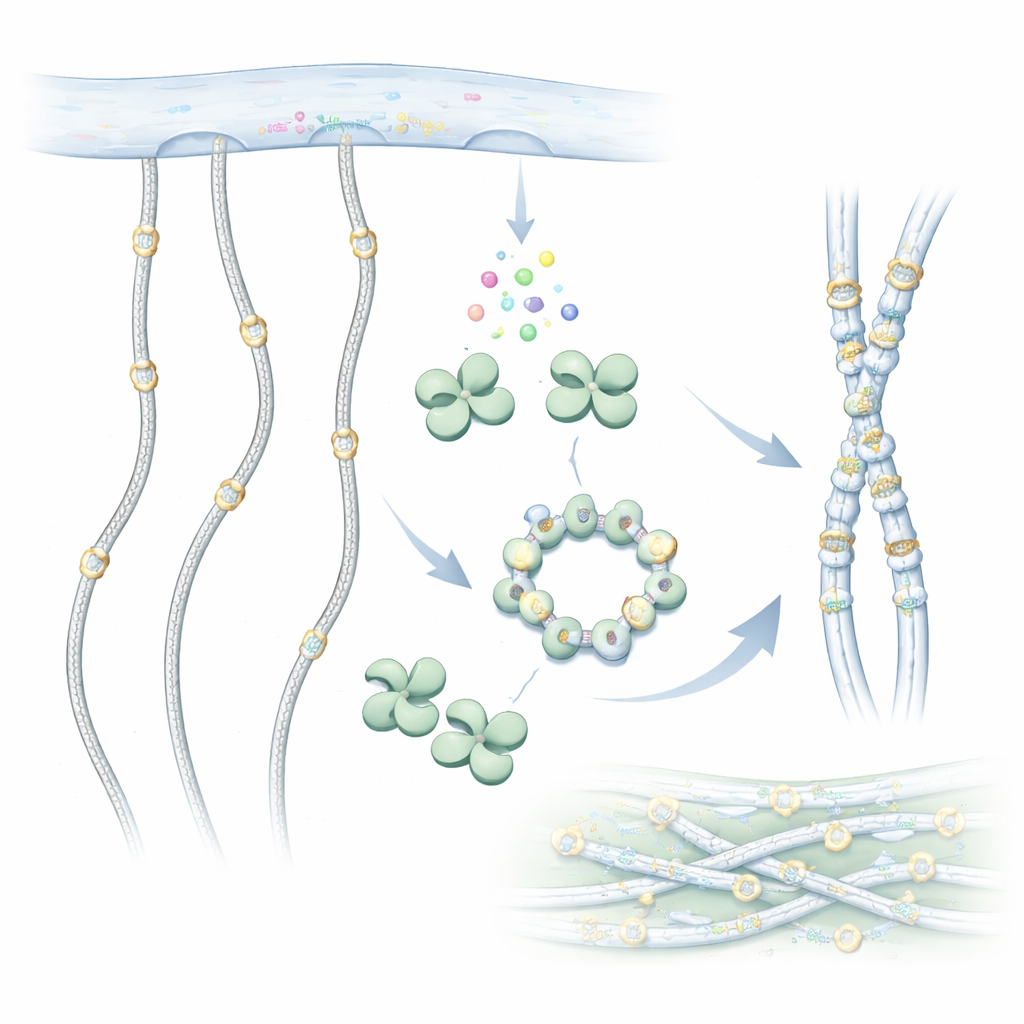
更近距离观察胶原的隐蔽改造
胶原分子是长而如绳索的链条,组装成细胞外的坚固纤维。然而在离开细胞之前,它们会被化学修饰。其中一项重要的修饰是在称为羟赖氨酸的特殊残基上添加糖基。GLT25D1 执行糖标记的第一步——将一个半乳糖从供体分子转移到羟赖氨酸上。该糖修饰在从简单动物到人类的物种中保守存在,帮助胶原正确折叠、与细胞相互作用并抵抗磨损。
揭示胶原“装饰者”的形态
为了解 GLT25D1 的工作机制,研究者使用低温电子显微镜对人源酶进行了近原子分辨率成像。他们发现每个 GLT25D1 分子由两个相似的叶片构成,均与糖转移酶常见的酶折叠相关。这些叶片配对形成延长的二聚体,三个二聚体进一步组装成一个环状的六聚体。在这些构象中,真正执行催化功能的中心彼此相距较远,这种布局可能允许沿一条拉伸的胶原链上同时运作多个加糖位点。
工作部件:糖转移真正发生的地方
团队解析了与糖供体和包含羟赖氨酸的短胶原样肽结合的 GLT25D1 结构。该三元复合物显示,只有第二个叶片,即 C 端结构域,实际进行化学反应。在这里,供体分子嵌入由金属离子稳定的口袋中,而肽位于一条狭窄槽沟中,强制形成特定的局部模式:羟赖氨酸后紧接着一个体积极小的甘氨酸。一个天冬氨酸残基作为化学碱,活化羟赖氨酸的羟基,使其能进攻糖分子并完成转移。对这些关键氨基酸的改变会显著降低或消除活性,从而证实它们的必要作用。
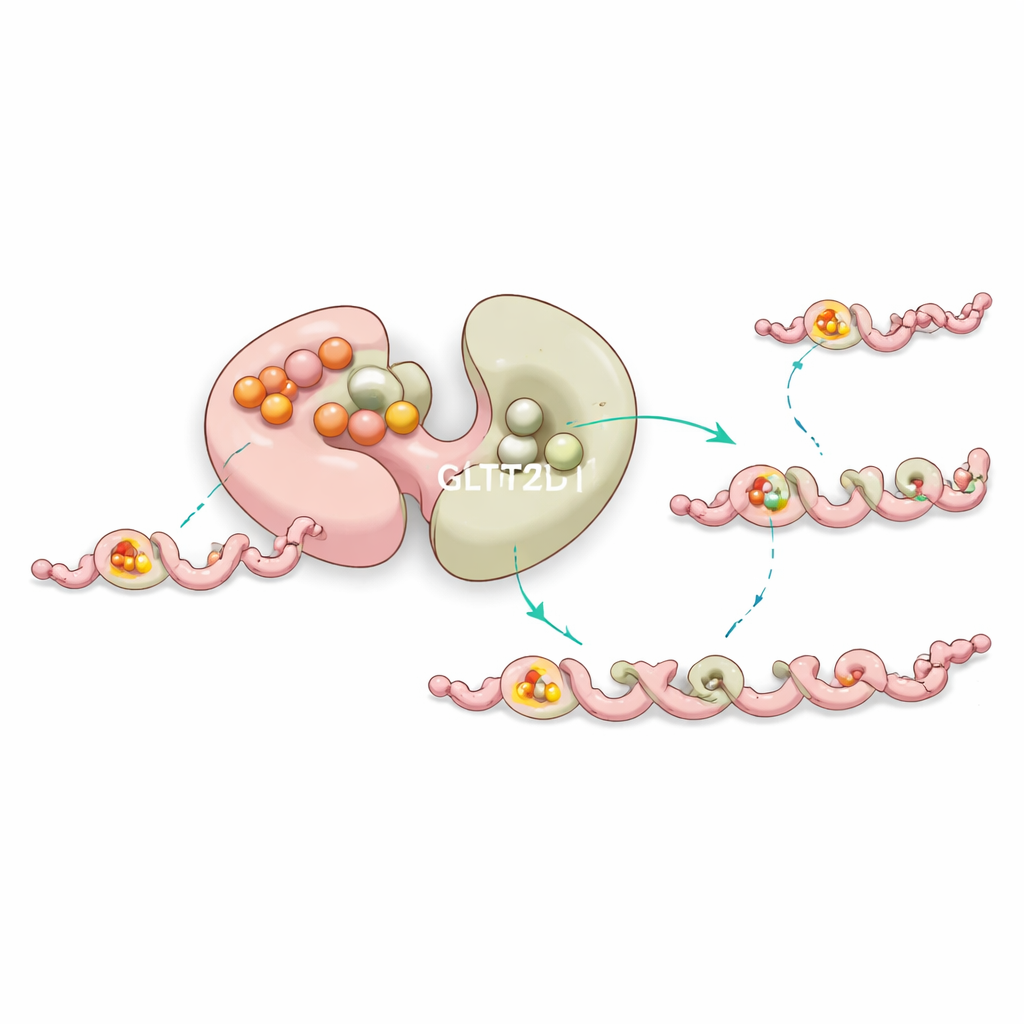
内建的稳定剂与远程调控
有趣的是,GLT25D1 的第一个叶片与糖供体结合得非常紧密,但并不执行转移反应。相反,实验和计算模拟表明这个“沉默”位点有助于稳定酶,并通过蛋白内部的长程通讯微妙地调节催化叶片的行为。靠近该非催化口袋的突变常常使酶失稳或改变其效率,这暗示自然选择利用这个额外的结合位点作为一种内部质量控制机制,以保持胶原修饰过程顺畅进行。
当“装饰者”失灵:与疾病的关联
通过将患者来源的突变映射到其结构模型上,作者能够解释 GLT25D1 出错如何导致人类疾病。有些突变直接切除催化叶片,有些使蛋白核心失稳,另外一些则直接攻击糖结合或胶原结合位点。这些缺陷降低或消除胶原的加糖,并已与小血管性脑病、认知障碍以及肌肉和骨骼缺陷相关联。与癌症相关的突变也集中在关键区域,这提示改变的胶原修饰可能影响肿瘤的生长与转移。
这对健康与未来治疗意味着什么
通过绘制出 GLT25D1 工作的详细三维蓝图,这项工作解释了胶原上如何添加精确的糖标签,以及这一步骤为何对组织完整性至关重要。对非专业读者而言,关键信息是:胶原上的微小化学变化可能对血管、骨骼甚至癌症风险产生重大影响。GLT25D1 的结构图现在为诊断有害变异和设计治疗策略提供了指引——无论是稳定受损酶的小分子,还是基于基因的手段——这些方法有朝一日可能从根本上纠正胶原加糖缺陷。
引用: Sun, H., Zhang, M., Shi, Y. et al. Molecular basis of collagen galactosylation by GLT25D1. Nat Commun 17, 2426 (2026). https://doi.org/10.1038/s41467-026-69234-1
关键词: 胶原糖基化, GLT25D1, 细胞外基质, 血管疾病, 低温电子显微结构