Clear Sky Science · zh
骨源性抑制蛋白缺失使白色脂肪细胞对诱导小褐化的小鼠产热信号更为敏感
为何让脂肪“变暖”能帮助遏制疾病
我们大多数人认为骨骼和体脂是两个不同的领域:一者提供支架,另一者储存能量。这项小鼠研究显示,骨与脂肪之间存在持续的化学对话,骨细胞产生的一种蛋白质能够决定我们的“白色”脂肪是单纯储存热量,还是转变为更为活跃、燃烧热量的“米色”脂肪。了解这种隐秘的对话可能为同时应对肥胖、糖尿病和骨质流失打开新的思路。
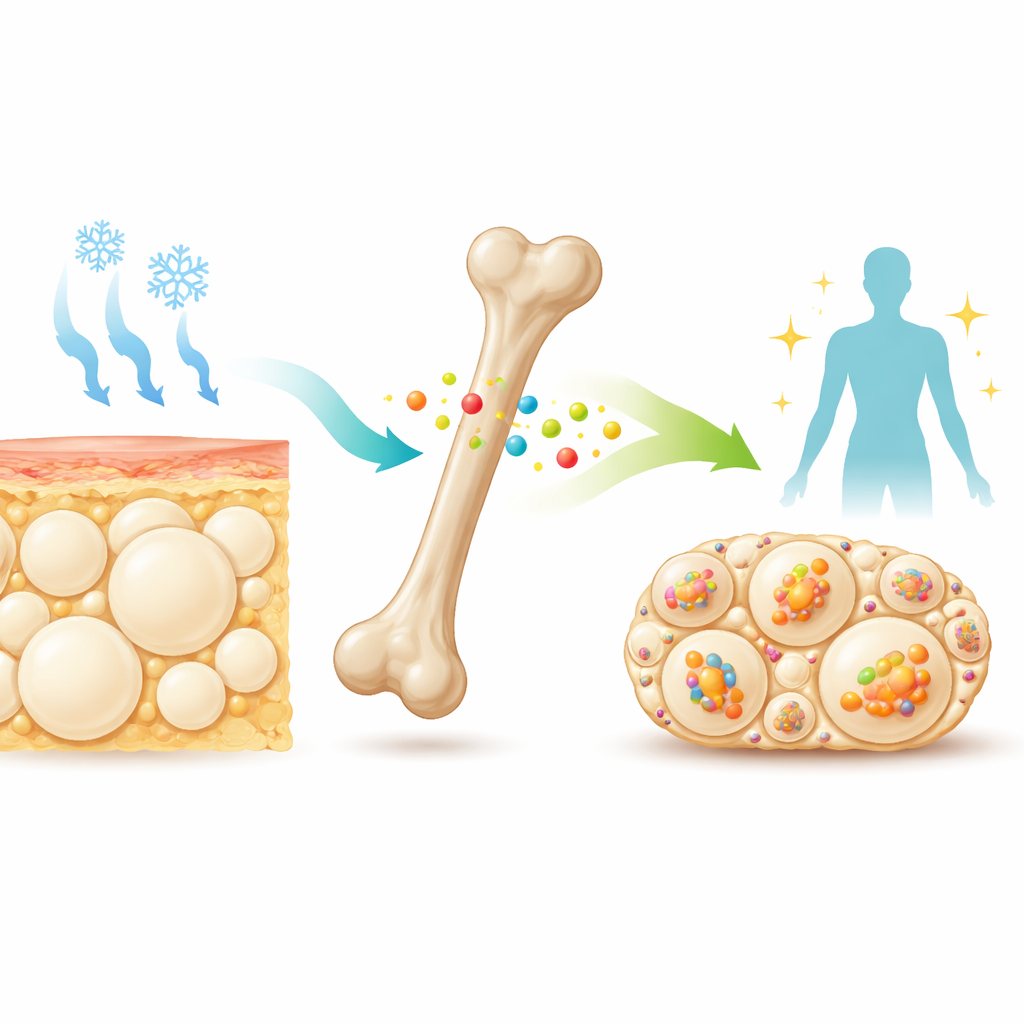
来自骨骼的低调信使
在骨骼深处,专门的细胞将一种名为骨源性抑制蛋白(sclerostin)的小蛋白释放到血液中。临床上已有针对该蛋白的药物用于增强骨强度,降低骨折风险。早期研究表明,缺乏骨源性抑制蛋白的小鼠不仅骨骼更强壮,而且较瘦、对胰岛素更敏感。它们的皮下脂肪,尤其是髂窝周围的皮下白色脂肪(inguinal white fat),含有类似“米色”脂肪的多室小脂肪细胞,这类细胞可以燃烧底物产热。这些线索促使研究者提出:在暴露于寒冷或模拟神经信号的药物时,骨源性抑制蛋白是否通常充当将白色脂肪转换为米色脂肪的制动器。
冷信号、骨信号与脂肪点火
研究组将正常小鼠和缺乏骨源性抑制蛋白基因(Sost-/-)的小鼠暴露于一种激活脂肪细胞特异性受体(β3-肾上腺素能受体)的药物,或置于轻度寒冷环境中。在正常动物中,这些产热信号增加了骨骼中骨源性抑制蛋白的生成并提升其血液水平。该上升与松质骨的丧失相关,但对皮下脂肪改变有限。相比之下,缺乏骨源性抑制蛋白的小鼠反应更强:它们的腹股沟脂肪摄取更多葡萄糖,释放更多脂肪酸,体积缩小,并充满了富含线粒体的米色风格细胞。关键产热基因在这些小鼠中被更强烈地激活,尤其在皮下脂肪中,而经典的棕色脂肪则大体保持不变。
通过共同开关微调脂肪燃烧
为探明骨源性抑制蛋白如何施加这种控制,研究者将注意力集中在β-连环蛋白(β-catenin)上——一种参与Wnt信号通路的蛋白,骨源性抑制蛋白在骨骼中通常抑制该通路。在脂肪组织中,出生后激活β-连环蛋白会促使白色细胞向米色样状态转变,并增强其对β3-肾上腺素能信号的反应,但当小鼠被安置于温暖的热中性环境(此时机体不再需要额外产热)时,该效应会消失。相反,在缺乏骨源性抑制蛋白的小鼠中,若特异性删除脂肪细胞中的β-连环蛋白,则其米色脂肪被消除,白色脂肪细胞恢复变大,胰岛素和脂肪酸水平的改善也被逆转。这些实验表明,当骨源性抑制蛋白水平较低时,脂肪细胞内的β-连环蛋白成为一个重要的内在杠杆,使白色脂肪对产热信号更为敏感。
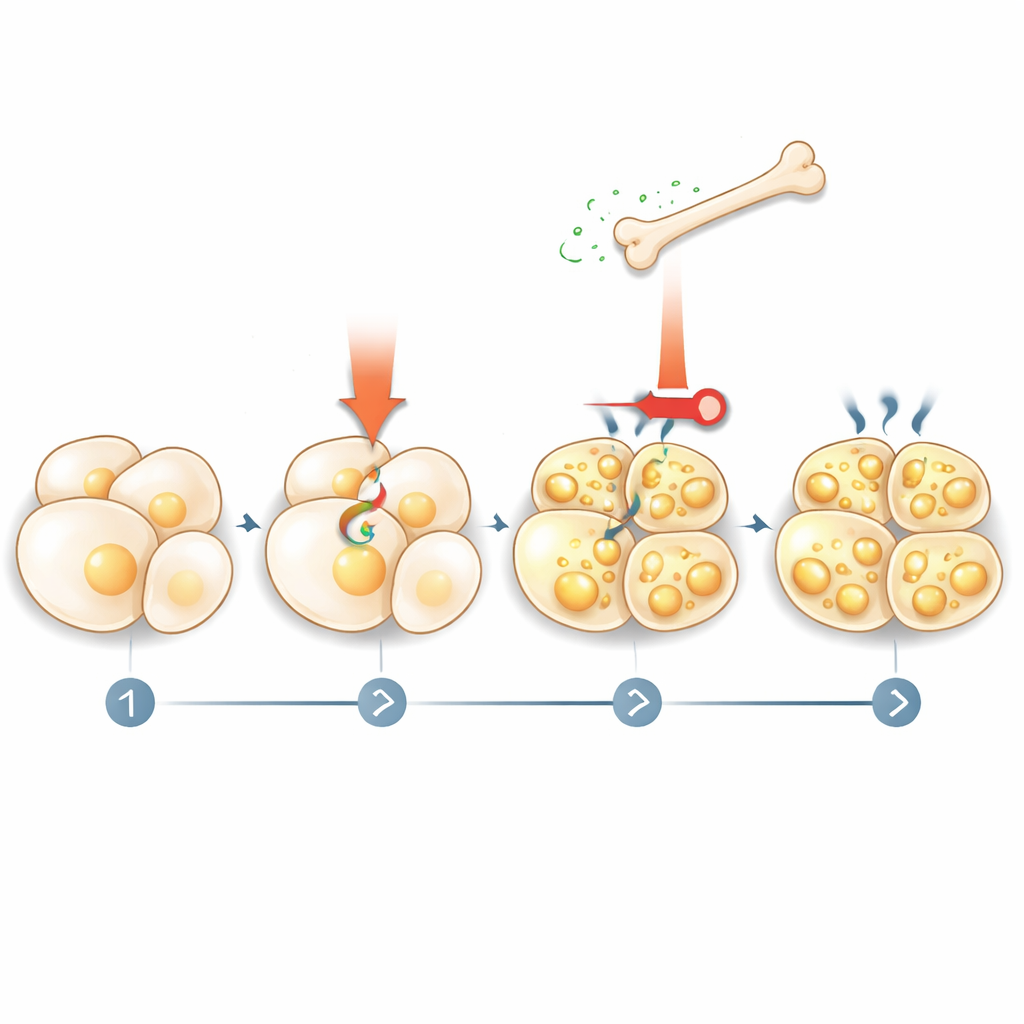
脂肪如何向骨骼回话
故事并未止于骨骼指挥脂肪。研究组发现,产热刺激激活脂肪分解(脂解),向血液释放脂肪酸。这些脂肪酸反过来通过名为PPARγ的核受体作用于骨细胞,促进骨源性抑制蛋白的生成。当研究者在脂肪细胞中阻断脂解或在骨细胞中移除PPARγ时,模拟寒冷的药物便无法再提升骨源性抑制蛋白水平。这揭示了一个反馈回路:产热信号促使脂肪释放燃料,该燃料指令骨骼分泌更多骨源性抑制蛋白,而骨源性抑制蛋白又反馈抑制进一步的脂肪激活与米色化。
将骨药与脂药配对以改善代谢健康
最后,研究者测试了中断该回路是否可在疾病样模型中带来益处。以高脂饮食致肥的小鼠接受低剂量米拉贝隆(mirabegron,一种已用于膀胱问题的β3-肾上腺素能药物)、一种中和骨源性抑制蛋白的抗体(romosozumab,已获批用于骨质疏松),或两者联合。单用任一药物的效果有限,而联合用药减少了关键脂肪库的脂肪量,使脂肪偏向更小、更活跃的细胞,降低了胰岛素、甘油三酯和胆固醇,并保留了骨强度。温暖环境(降低机体对产热的需求)在很大程度上抹除了骨源性抑制蛋白缺失带来的代谢益处,强调该通路在存在产热信号时尤为重要。
这对未来治疗意味着什么
简而言之,这项工作显示骨骼不仅是被动的支架,而是积极调节脂肪细胞燃烧能量多少的器官。骨源性抑制蛋白像一个音量旋钮,控制产热脂肪的活性以及燃料的使用量。通过基因或药物将该旋钮调低,会使特定的白色脂肪库在受到寒冷或特定药物刺激时更容易转换为产热模式。由于同一干预在小鼠中既能增强骨骼又能改善代谢健康,经精心设计的骨-脂联合治疗有朝一日可能帮助同时治疗肥胖、糖尿病和骨质疏松,而非各自单独应对这些疾病。
引用: Choquette, G.M., Kim, S.P., Wilkinson, K.J. et al. Sclerostin deficiency sensitizes white adipocytes to thermogenic signals that induce beiging in mice. Nat Commun 17, 2394 (2026). https://doi.org/10.1038/s41467-026-69227-0
关键词: 骨源性抑制蛋白, 米色脂肪, 骨-脂交流, 产热, 代谢性疾病