Clear Sky Science · zh
由septin相关的PIPKIγ亚型在中期体处局部合成PI(4,5)P2以控制centralspindlin在细胞质分裂期间与中期体的关联
细胞如何完成分裂
胞质分裂——将一个细胞拧成两个的最后收拢——常被视为理所当然,但当这一过程出错时会助长癌症和其他疾病的发展。本研究揭示了一组特定分子如何像施工领班一样在连接两个新生细胞的狭窄桥梁处发挥作用,确保分裂顺利完成,而不是回弹或停滞。
子细胞之间的最终桥梁
在细胞复制遗传物质并分离染色体后,必须在物理上完成分裂。由蛋白丝构成的收缩环在细胞中部收缩,形成称为裂沟的深槽。随着裂沟向内牵拉,两个人工细胞通过包含致密核心—中期体的细胞间细桥相连。中期体是由成束微管、支架蛋白和信号脂质组成的微小但复杂结构,既作为系索又作为调控中心,协调分裂的最后步骤和细胞之间的最终切断。 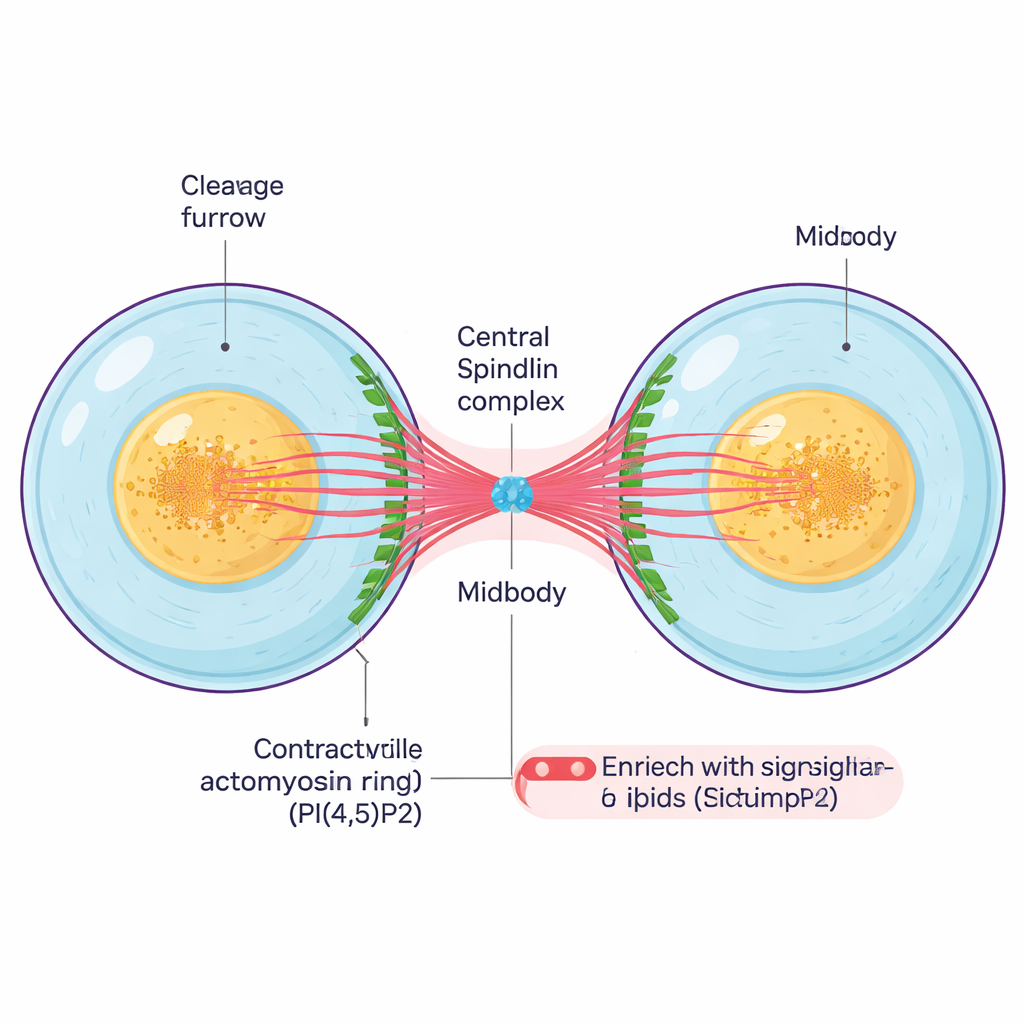
必须出现在正确位置的脂质信号
这一过程中一个关键参与者是存在于细胞膜上的信号脂分子PI(4,5)P2。这种脂质有助于锚定许多构建并收缩收缩环以及稳定桥梁的蛋白质。问题在于,鉴于它可以在膜中扩散,细胞如何控制PI(4,5)P2出现的时空位置。作者关注产生PI(4,5)P2的I型PIP激酶,特别是一种基因PIPKIγ,其存在若干细微不同的剪接变体。通过在人体细胞中选择性下调每种激酶并用先进显微镜观察效应,他们发现PIPKIγ在胞质分裂晚期——桥梁和中期体形成时——发挥特殊作用,尽管它并未显著改变细胞表面整体PI(4,5)P2水平。
septin支架招募一种专门酶
研究团队发现PIPKIγ的两个剪接变体,称为i3和i5,像精密工具一样被称为septins的结构蛋白带到正确位置。septins形成丝状和环状结构,帮助塑造桥梁并组织其他组分。生化拉下实验和细胞成像显示,PIPKIγ-i3和PIPKIγ-i5可以与septin复合物物理结合并装饰septin丝,而其他PIPKIγ变体则不能。当研究者在这些剪接插入区突变两种特定氨基酸时,这些酶便无法再结合septins。在分裂细胞中,正常的PIPKIγ-i3/i5从弥散的膜分布移动并在裂沟处富集,随后与septins和另一种支架蛋白anillin一起勾勒出细胞间桥梁和中期体。仅去除i3和i5变体会使anillin和septins从中期体沿桥梁散开,许多细胞因此胞质分裂失败,最终出现多核现象。
局部脂质生成锁定分裂机器
为了检验这些效应是否依赖局部PI(4,5)P2的生成,作者测量了中期体周围的PI(4,5)P2并操作添加或移除该脂质的酶。耗减PIPKIγ-i3/i5会降低中期体处的PI(4,5)P2,而抑制PI(4,5)P2降解酶则产生相反效果。重要的是,恢复一种能与septin结合且具有催化活性的正常PIPKIγ剪接形式可以挽救anillin和septins在桥梁处的正确聚集,但激酶失活或无法结合septin的突变体则不能。利用活细胞成像和一种通过物理扩张样本以显现细微结构的扩展显微术,团队显示缺失PIPKIγ-i3/i5时,septins不再转移到桥梁微管上,桥梁变短且成束程度降低,一个关键复合体centralspindlin也无法紧密地维持在中期体上。 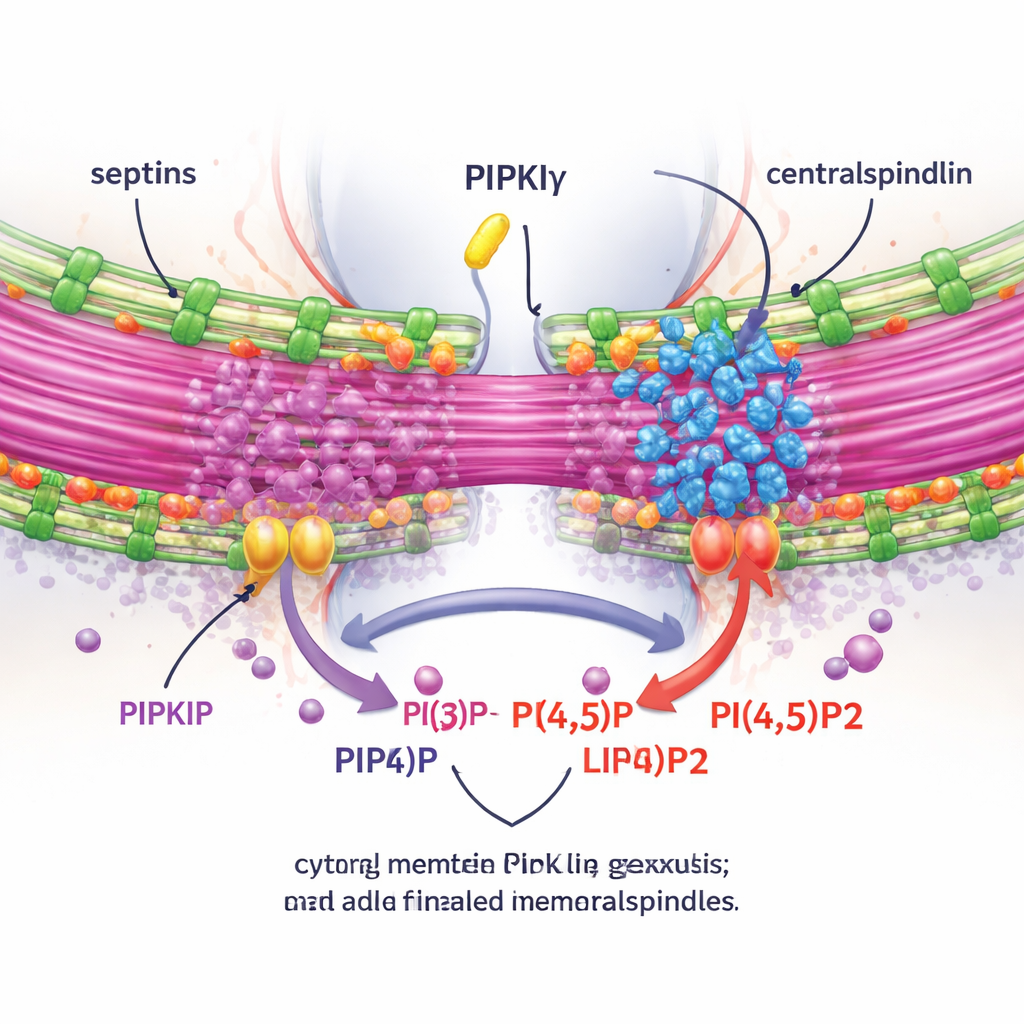
为干净切割建立一个检查点
centralspindlin有助于将中期体的微管与周围膜连接,并调控控制细胞形状的小分子开关。研究发现centralspindlin同时与septins和PIPKIγ相关联,失去任一伙伴都会类似地削弱其在中期体的存在。作者提出,septins将PIPKIγ-i3/i5招募到内陷的裂沟处,这些酶在该处产生一小块高浓度的PI(4,5)P2。这个局部脂质池反过来稳定了靠近中期体的anillin、centralspindlin和septins,促进桥梁微管的成束和稳定,使细胞间桥梁得以成熟直到最终的切断发生。如果该系统被破坏,PI(4,5)P2会出现在错误位置,支架蛋白分散,微管成束差,胞质分裂常常失败。
这一发现对于基础细胞生物学之外的意义
通过明确特定PIPKIγ剪接变体与septins如何协同在中期体产生局部脂质信号,这项工作解释了细胞如何为高度可动的信号分子提供时空精确性。这种精确性对安全完成细胞分裂至关重要,有助于防止染色体错误分离和异常细胞数目,从而降低有利于肿瘤发生的风险。同样的中期体结构在分裂后也影响细胞命运和增殖,因此理解它们如何组装为探索这些纳米级支架出错如何促成癌症以及可能操纵干细胞打开了新途径。
引用: Russo, G., Hümpfer, N., Jaensch, N. et al. Local PI(4,5)P2 synthesis by septin-associated PIPKIγ isoforms controls centralspindlin association with the midbody during cytokinesis. Nat Commun 17, 1482 (2026). https://doi.org/10.1038/s41467-026-69224-3
关键词: 细胞分裂, 胞质分裂, 信号脂质, septins(隔丝蛋白), 癌症生物学