Clear Sky Science · zh
通过氢原子转移介导的动态消旋光催化立体选择性编辑烷炔,构建三维分子
为何将平面分子转为三维形状至关重要
许多现代药物起始于易于合成但在体内表现并不总是理想的平面、片状分子片段。药物设计者已经认识到,紧凑的三维框架往往具有更好的性质:它们可以更贴合生物靶点,在体内的分布和迁移不同,有时还能减少副作用。本文介绍了一种新的光驱动方法,能够在一步反应中将简单的平面“线状”分子扭转为复杂的三维笼状结构,可能加速下一代药物和功能材料的探索。
从直线到微小笼状结构
构建这些笼状结构(称为桥环)的传统方法多走迂回路线:化学家先合成相对平面的环系,然后在第二步将其拼接在一起。这种两步策略可行但耗时,并限制可达的形状。作者改为从非常简单的一维原料出发:线性烷炔(碳—碳三键)和醛(小的碳—氧单元)。他们的目标是直接从这些直链一步跳跃到紧凑的三维框架,避开常规的迂回路径,从而打开对药物设计有价值的新的“化学空间”。
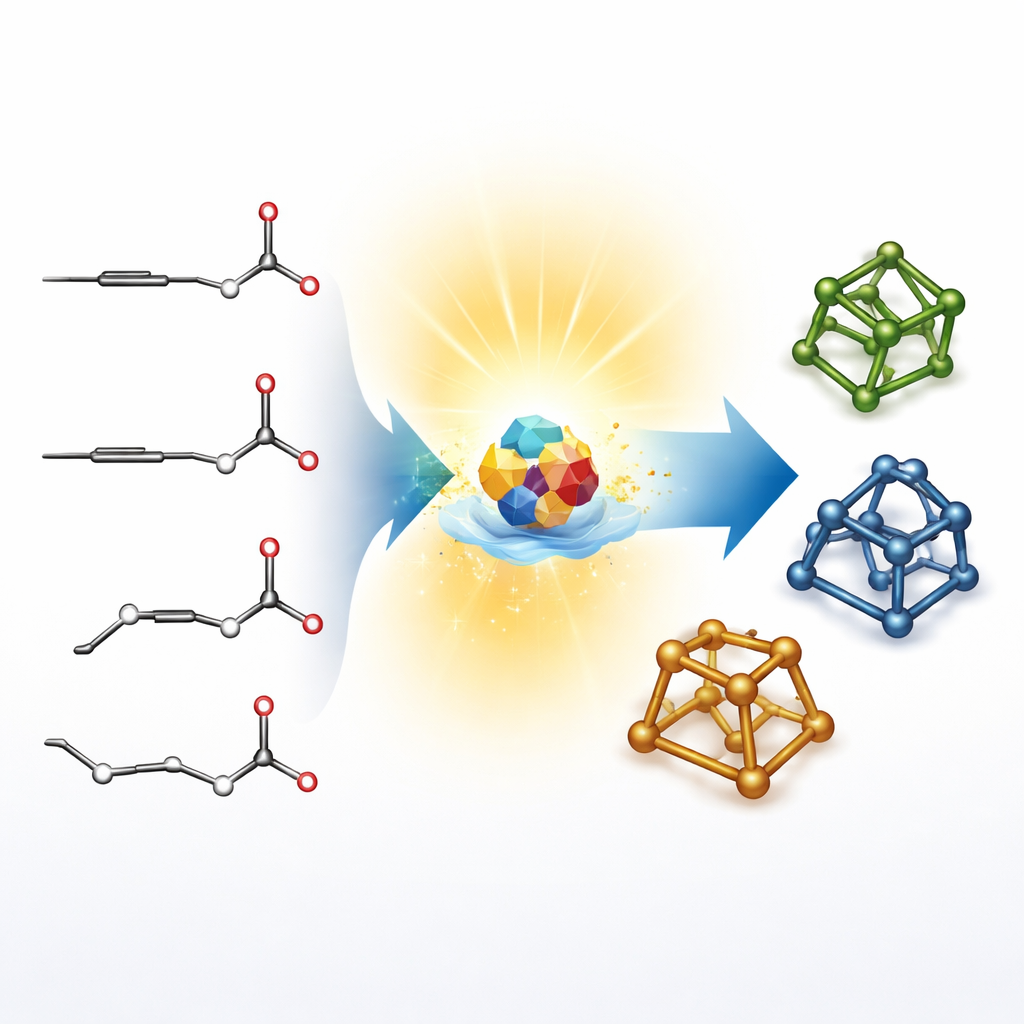
让光来完成艰巨工作
研究团队利用了一种基于多氧酸盐——十钨酸盐的特殊光敏催化剂。在紫光照射下,该催化剂可以从醛底物上抽取一个氢原子,短暂生成一个高活性片段。该片段加成到烷炔上,自身折返并闭合成一个五元环。单凭第一步环合会在关键碳位产生混杂的三维构象混合物。巧妙之处在于,同一光驱动体系还能通过反复抽取和归还氢原子实时重排这些构象,使混合物朝更稳定的形态演化。
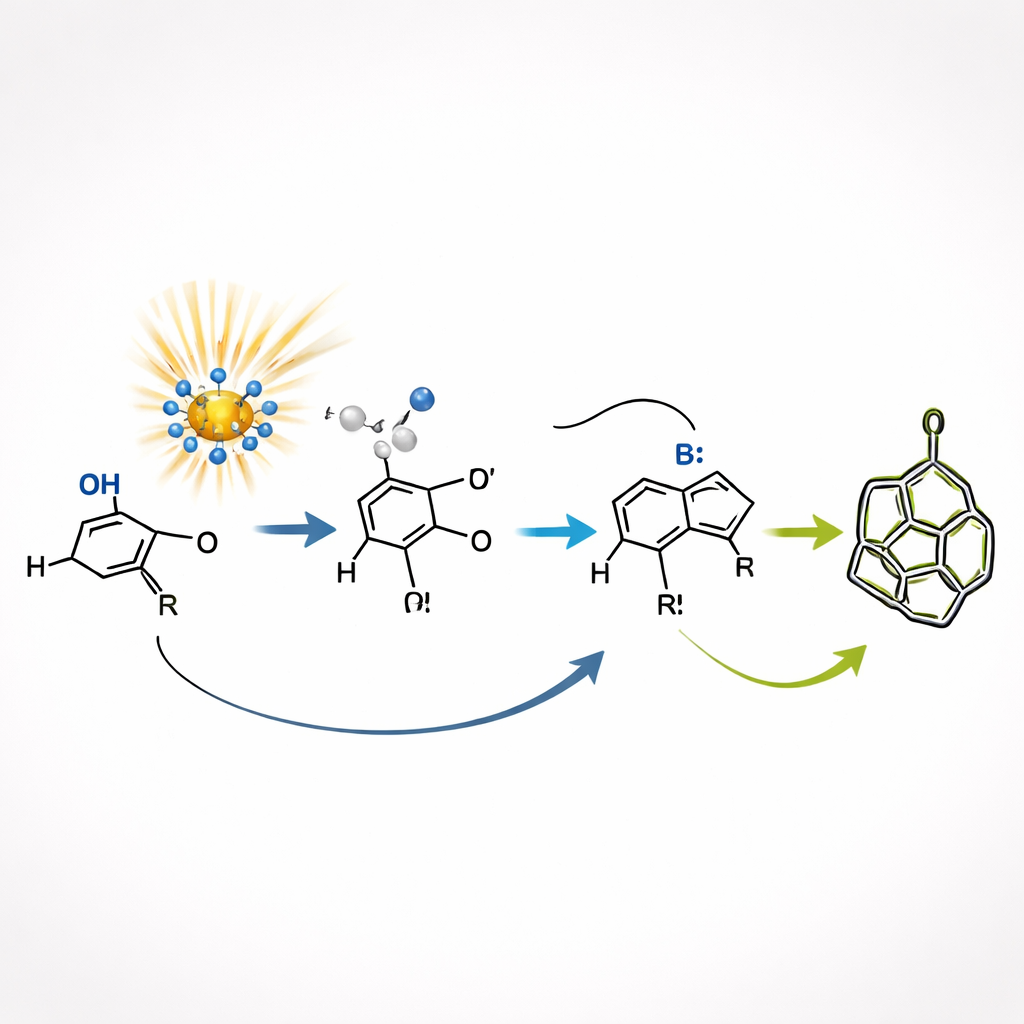
自我修正的三维编辑
该发现的核心是内在的自我修正机制,称为动态动力学解析。初始的环中间体以两种密切相关的三维构象存在,仅在原子空间取向上有所不同。光激活的氢传递能快速在这些构象间互变,而一个额外的碱促进的闭合步骤则只偏好其中一种构象进行最终笼状形成。因此,“优先”的中间体不断被耗竭并转化为单一、界定明确的双环产物,而较不利的构象则持续被转换为其同伴。这种可逆的构象翻转与选择性捕获之间的相互作用,使得即便第一步很不选择,最终产物在多个位点仍能获得优异的立体控制。
构建多样且有用的三维骨架
作者展示了该光驱动方法适用于多种起始材料,并能在生成的笼体上引入多种化学基团,作为化学手柄进行进一步改造。他们合成了两类框架:bicyclo[2.2.1]heptanone 和 bicyclo[3.2.1]octanone,这两类都是药物化学中受青睐的构件。这些结构出现在天然产物、催化剂和材料中。团队还演示了如何将这些三维笼体转化为更复杂的化合物,包括用于电致发光材料的关键中间体以及已知脑受体拮抗剂的刚性化改良体。在一个实例中,用新构建的三维笼替换药物中一个柔性环,甚至在一定程度上提高了其生物效力。
通向更丰富分子形状的捷径
通俗地说,这项工作展示了如何把简单直线的分子“棍子”,借助光和智能催化剂在一步之内折叠成精确的三维“雕塑”。该过程同时完成两个任务:构建基础骨架并微调原子的空间排列,且条件温和。由于烷炔是常见且廉价的原料,该策略有望成为将廉价原料直接转化为复杂、类药结构的通用捷径。随着化学家进一步深入三维分子的领域,这类工具可能在按设计构建更高效的药物和材料方面发挥关键作用。
引用: Gu, Z., Zeng, T., Yuan, Z. et al. Photocatalytic Stereoselective Editing of Alkynes to 3D Molecules via Hydrogen Atom Transfer-Mediated Dynamic Epimerization. Nat Commun 17, 2518 (2026). https://doi.org/10.1038/s41467-026-69219-0
关键词: 光催化, 氢原子转移, 三维分子骨架, 动态动力学解析, 药物化学