Clear Sky Science · zh
全RAF抑制剂 exarafenib 靶向 BRAF II/III 类非小细胞肺癌,揭示 ARAF–KSR1 抵抗机制与组合策略
这项研究对肺癌患者的重要性
大多数人听说过能针对特定基因改变的靶向抗癌药。但对许多肺癌患者,尤其是那些肿瘤携带 BRAF 基因中不常见突变的人,目前的靶向药往往无效。本研究介绍了一种新型候选药物 exarafenib,旨在覆盖更广泛的 BRAF 驱动肿瘤,并阐明癌细胞如何试图逃逸这种抑制——从而揭示可能使这些肿瘤更长时间受控的联合治疗策略。
被忽视的一大类突变
研究人员首先提出一个基本问题:不同类型的 BRAF 突变在晚期癌症中,尤其是在非小细胞肺癌(NSCLC)中有多常见?他们利用包含超过 16 万名患者的超大规模液体活检数据库,分析循环血液中的肿瘤 DNA 片段。结果显示,在肺癌中约有 4–5% 的患者存在 BRAF 突变,这在全球范围内仍意味着数以千计的患者。关键是,大约三分之二的肺肿瘤携带所谓的 II 类和 III 类 BRAF 突变——这是当前获批的 BRAF 药物难以有效靶向的类型。携带这些类别突变的患者,尤其是 II 类,整体生存时间往往短于携带更常见的 I 类突变的患者,这很可能是因为 I 类患者可获得已有的靶向疗法,而 II/III 类患者大多仍接受标准化疗或免疫治疗。
靶向全通路的下一代药物
BRAF 是一组蛋白(MAPK 通路)中的一环,将细胞表面的生长信号传入细胞核。许多现有的 BRAF 药物只针对一种突变形式设计,甚至可能在正常细胞中意外激活相关蛋白。exarafenib 的设计则不同:它是一种“全 RAF”抑制剂,旨在抑制多个 RAF 家族成员(ARAF、BRAF 和 CRAF),无论是单体还是二聚体形式,同时尽量不影响大多数其他细胞酶。在对数百种人类激酶进行的生化测试中,exarafenib 有力地抑制了所有三种 RAF 蛋白且离靶效应很少,提示其安全性谱可能比早期的全 RAF 化合物更为清晰。
在难治肿瘤模型中的显著效果
团队在携带不同 BRAF 和 RAS 突变的一系列细胞系和小鼠模型中测试了 exarafenib,包括真实来源的患者肿瘤。在细胞培养中,exarafenib 抑制了细胞生长并关闭了 MAPK 信号,不仅对经典的 BRAF V600E 癌细胞有效,也对携带 II 类和 III 类突变的细胞以及许多目前缺乏有效靶向选择的 RAS 突变细胞有效。在携带这些改变的肺肿瘤小鼠中,exarafenib 以剂量相关的方式使肿瘤缩小或生长减慢,并显示出药物水平、通路抑制与肿瘤反应之间的明确关联。来自两例晚期 BRAF 突变肺癌患者的早期临床数据——一例为罕见的 BRAF 融合,另一例为 II 类点突变——显示部分缓解和明显的症状缓解,支持了临床前工作的相关性。
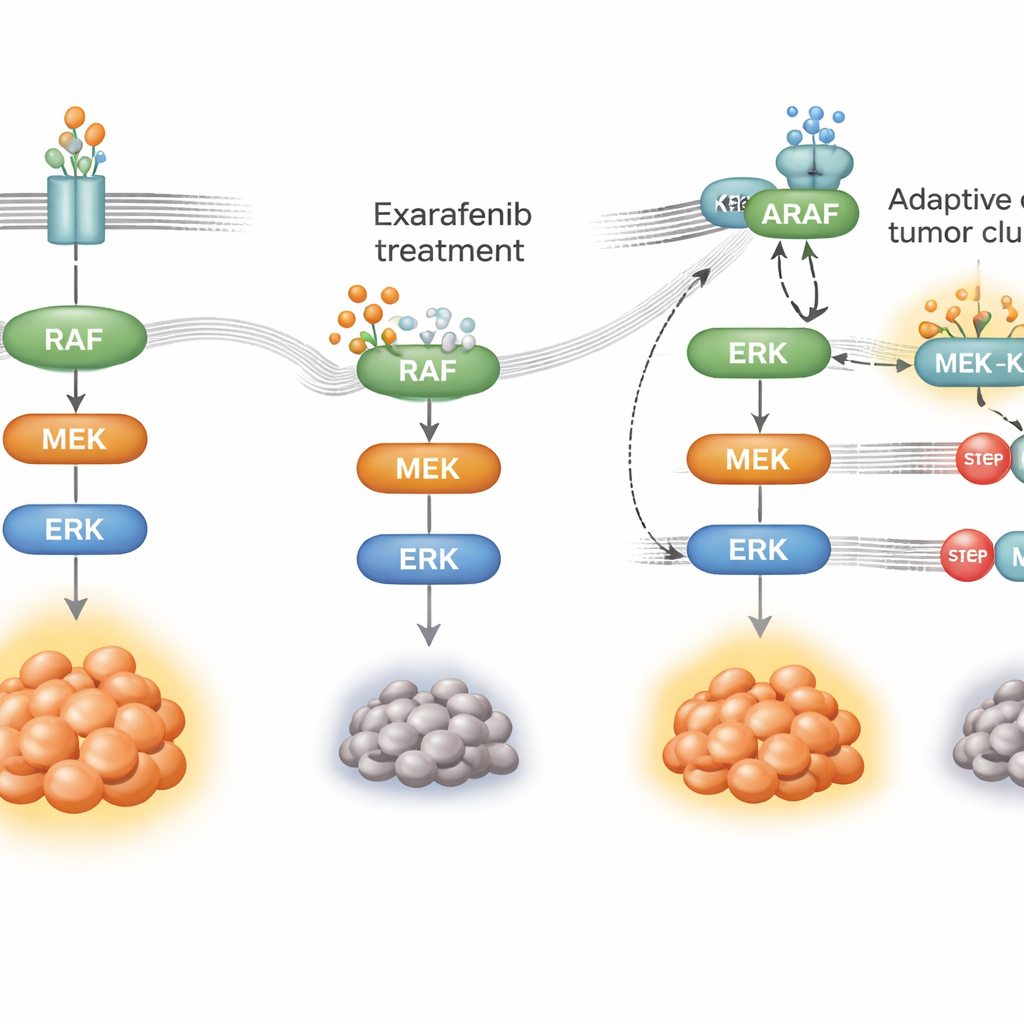
癌细胞如何学会绕过药物
没有任何靶向疗法能永远有效;癌细胞会适应。为了解肿瘤可能如何对 exarafenib 产生耐药性,研究人员将 BRAF 突变的肺癌细胞持续暴露于药物数月,直到出现耐药群体。这些细胞仍然依赖相同的生长通路,但在使用方式上发生了重接线。它们不再主要依赖突变的 BRAF,而是提高了名为 RAS 的上游开关活性,并转而使用另一位家族成员 ARAF,联合一个称为 KSR1 的支架蛋白。在药物压力下,ARAF 与 KSR1 形成紧密复合体,帮助在 exarafenib 结合时仍维持 MAPK 级联的运行。当科学家有选择性地敲低 ARAF 或 KSR1,或降低 RAS 活性时,耐药细胞再次对 exarafenib 变得敏感,生存信号崩溃。
领先耐药的组合策略
基于这一机制图谱,团队寻找能够在原始路径与旁路共有的关键节点封锁该通路的伙伴药物。他们发现,将 exarafenib 与抑制 MEK 或 ERK 的药物联合——这两者是 MAPK 级联的关键下游步骤——在多种细胞和小鼠模型中产生显著协同效应,包括那些本质上对 exarafenib 敏感性较低或已获得耐药的肿瘤。这些组合更长时间地关闭通路,诱导更多细胞死亡,并且在动物实验中常常与单用更高剂量 exarafenib 同样或更优,而未见明显额外毒性。在那些由 RAS 明显驱动耐药的模型中,直接靶向 RAS 的药物也增强了 exarafenib 的效果,提示另一种临床上有前景的策略。
对患者意味着什么
对于携带 II 类或 III 类 BRAF 突变、或复杂 BRAF 融合并伴有 RAS 共突变的 NSCLC 患者,目前尚无获批的靶向疗法,且其结局落后于携带更常见改变的患者。本研究提供了强有力的科学证据,表明 exarafenib 有望通过广泛关闭 RAF 驱动的信号来填补这一空白。研究还解释了肿瘤可能通过 ARAF–KSR1 旁路进行适应,并显示在多个层面上联合抑制该通路,特别是联合 RAF 与 MEK 抑制剂或加用 RAS 抑制剂,可能带来更深更持久的肿瘤控制。综上,这些见解为推进临床试验铺路,旨在为一大群此前缺乏治疗选择的肺癌患者提供更为个体化的组合靶向治疗路径。
引用: Manabe, T., Bergo, H.C., Li, Q. et al. Pan-RAF inhibitor exarafenib targets BRAF class II/III NSCLC and reveals ARAF-KSR1 resistance and combination strategies. Nat Commun 17, 2484 (2026). https://doi.org/10.1038/s41467-026-69216-3
关键词: BRAF 突变型肺癌, 全 RAF 抑制剂, MAPK 信号通路, 药物耐受性, 靶向治疗组合