Clear Sky Science · zh
组织驻留巨噬细胞的存活依赖由SerpinB2调控的线粒体功能,在慢性炎症中尤为重要
为什么脂肪里的免疫细胞重要
大多数人把体脂视为被动的储存,但它实际上是一个活跃的组织,充满了帮助控制炎症和血糖的免疫细胞。这项研究揭示了深层腹部脂肪中一类寿命较长的免疫细胞如何作为防止2型糖尿病的守护者——以及肥胖导致的慢性炎症如何通过损伤它们的能量工厂线粒体,悄然使其死亡。
两类脂肪守护者
内脏脂肪——缠绕在内脏周围的脂肪组织——含有两类主要的免疫细胞,称为巨噬细胞。一类寿命较短,持续由血液中的单核细胞补充;这些“炎症性”巨噬细胞倾向于促进炎症和胰岛素抵抗。另一类是长期驻留的组织巨噬细胞,早期发育形成,通常有助于维持组织的平静、支持健康的脂肪储存并促进全身的胰岛素敏感性。通过在小鼠中追踪这些细胞并比较基因活性,研究者表明驻留型巨噬细胞富含抗炎和促进胰岛素敏感性的基因,而来自单核细胞的入侵型巨噬细胞则表达会恶化血糖控制的基因。
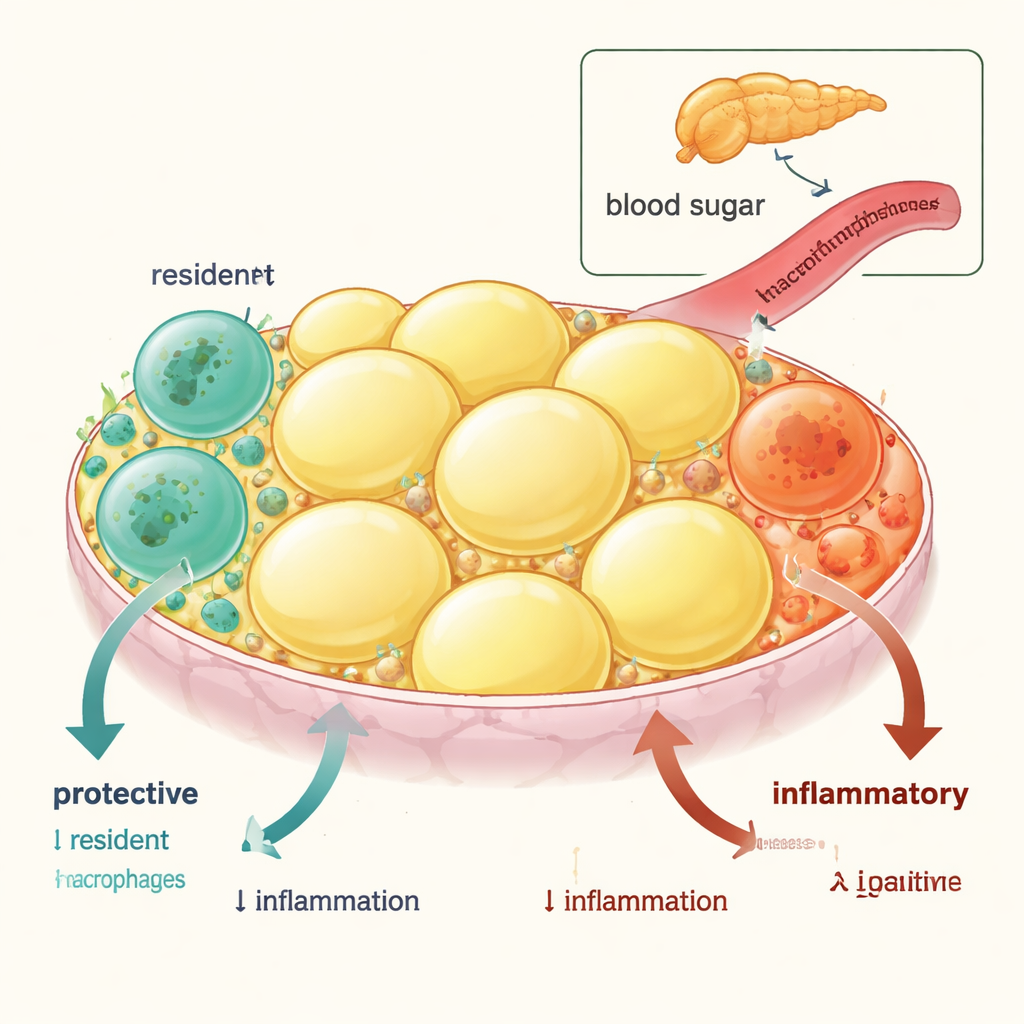
当炎症消灭好细胞
在肥胖时,这种保护性的平衡会发生改变。研究团队发现,在肥胖的小鼠以及肥胖或糖尿病患者中,内脏脂肪中驻留巨噬细胞的数量下降,而炎症性巨噬细胞增加。精细的成像和细胞死亡标记揭示了原因:驻留巨噬细胞经历更多的程序性细胞死亡(凋亡),而炎症性细胞则不是。值得注意的是,当将肥胖小鼠从高脂饮食中撤回时,驻留细胞群通过局部增殖缓慢恢复,代谢健康得到改善——显示这种丧失是由炎症状态驱动并且可逆的。
单一蛋白将线粒体与存活联系起来
一个关键线索是名为SerpinB2的蛋白,最为人知的是在血液凝固中的作用。研究者发现SerpinB2在驻留巨噬细胞内表达非常高,而在炎症性细胞中表达要少得多。在肥胖的人和小鼠中,驻留巨噬细胞显著降低了SerpinB2的表达,且较高的体质量指数与较少的SerpinB2阳性细胞相关。在缺失SerpinB2的细胞实验中,观察到细胞色素c——一种关键的线粒体蛋白——更多地从线粒体泄漏到细胞质中,这是触发凋亡的经典信号。这些缺乏SerpinB2的巨噬细胞显示抗氧化防御能力降低、线粒体活性氧(ROS)增加和耗氧量上升,都是线粒体承受压力、过度运转并推动细胞走向炎症性行为和死亡的迹象。
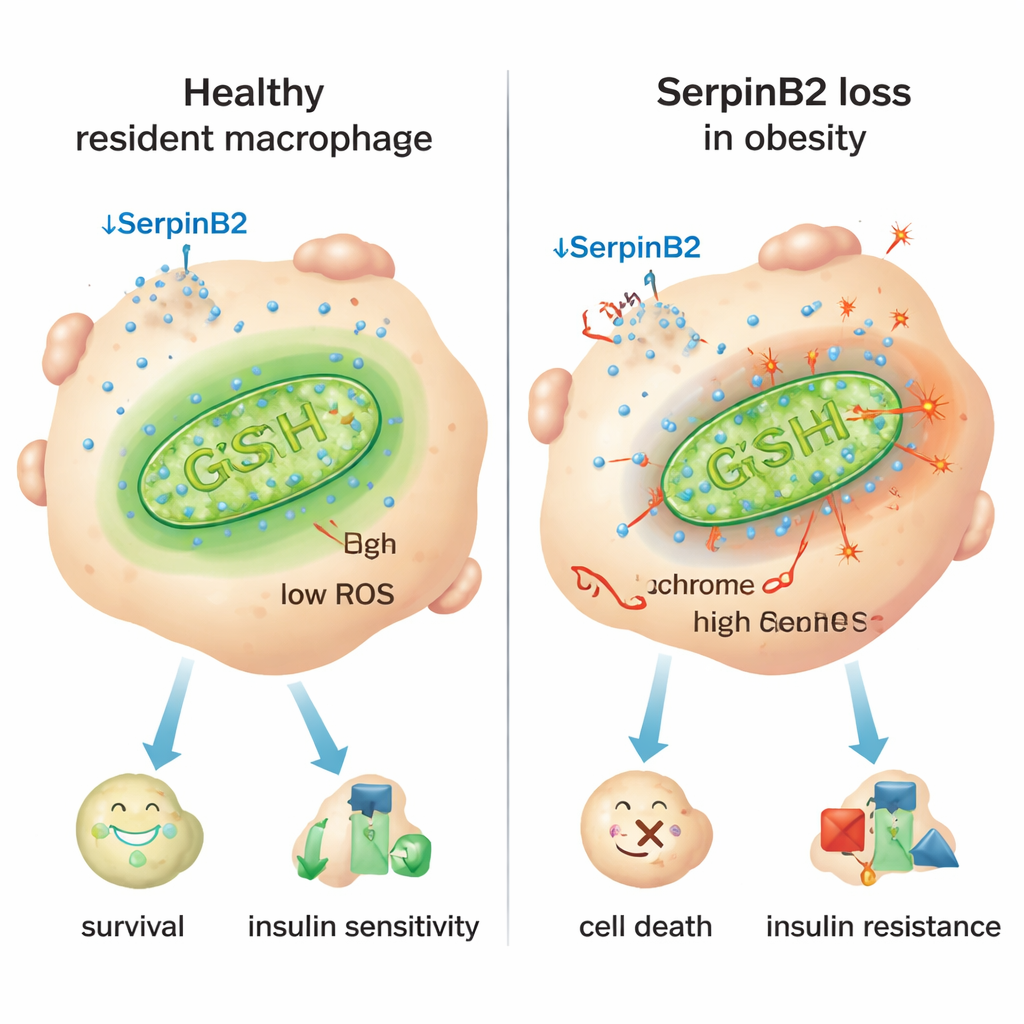
炎症开关及潜在修复方式
该研究将这种线粒体压力追溯到肥胖中持续存在的炎症信号,特别是脂肪组织中过度产生的免疫信使干扰素‑γ(IFN‑γ)。IFN‑γ激活一种名为Ikaros的转录抑制子,该抑制子结合SerpinB2基因的调控区并将其下调。在工程化使髓系细胞无法响应IFN‑γ的小鼠中,驻留巨噬细胞维持了SerpinB2、存活状况更好,动物表现出更低的血糖、更好的胰岛素敏感性以及更小的脂肪细胞。相反,在巨噬细胞中特异性删除SerpinB2会加剧葡萄糖耐受不良和胰岛素抵抗,部分原因是脂肪组织更加炎症化并发生扩张。通过补充N‑乙酰半胱氨酸(NAC)提高抗氧化剂谷胱甘肽水平可以恢复线粒体保护,挽救驻留巨噬细胞的存活,缩小脂肪细胞体积,并在缺失SerpinB2的情况下仍改善代谢指标。
这对代谢健康意味着什么
对普通读者而言,核心信息是并非所有脂肪或脂肪内的免疫细胞都是有害的。内脏脂肪中一类专门的长期驻留巨噬细胞通过SerpinB2驱动的抗氧化防御维持线粒体健康,从而保护我们免受失控炎症和血糖升高的影响。在肥胖中,慢性炎症信号关闭了SerpinB2,线粒体受到压力,这些保护性细胞死亡,更多有害的巨噬细胞接管,促成胰岛素抵抗。该研究表明,旨在保护驻留巨噬细胞的疗法——通过阻断IFN‑γ/Ikaros对SerpinB2的抑制或通过支持基于谷胱甘肽的抗氧化防御——可能有助于预防或治疗与肥胖相关的代谢疾病。
引用: Vasamsetti, S.B., Sadaf, S., Uddin, M.A. et al. Tissue-resident macrophage survival depends on mitochondrial function regulated by SerpinB2 in chronic inflammation. Nat Commun 17, 1493 (2026). https://doi.org/10.1038/s41467-026-69196-4
关键词: 内脏脂肪, 巨噬细胞, 线粒体, 胰岛素抵抗, SerpinB2