Clear Sky Science · zh
非典型蛋白激酶C的激活驱动糖尿病患者肠道排糖
将肠道变成糖分阀门
糖尿病患者体内循环着过多的血糖。像胃旁路这样的减重手术能在令人惊讶的短时间内将血糖恢复正常,甚至在体重明显下降之前就见效,但其机制长期不明。本研究揭示了一种基于肠道的“糖分阀”——肠道可以从血液中抽取葡萄糖并将部分排回肠腔——提示了一个新的药物靶点,或有望在不做手术的情况下模拟手术带来的益处。
为什么手术能如此快速地改变血糖
医生早已注意到 Roux-en-Y 胃旁路术不仅是有效的减重手段,也是治疗 2 型糖尿病的强有力方法之一。手术后不久,患者的血糖常常显著改善,即便体重尚未大幅下降。该团队先前的研究显示,胃旁路后小肠的部分区域开始表现得像海绵一样,从血液中吸收葡萄糖并将一部分释放到肠腔内。这种异常的行为被称为肠道排糖,似乎依赖于一种名为 GLUT1 的转运蛋白。关键问题是:哪一个分子开关使肠道翻入这种清除糖分的状态?
用大数据寻找分子开关
为了寻找该开关,研究者使用了基于 Connectivity Map 的大规模计算药物发现系统,该数据库记录了数千种化学物质在细胞中如何改变基因表达。他们将五种表现出高肠道排糖的情形(包括经胃旁路的鼠类组织和经肠道生长信号处理的细胞)的基因表达模式,与已知药物产生的模式进行比对。一个化合物类别持续突出:蛋白激酶 C(PKC)的激活剂,PKC 是一类在细胞内传递信号的酶。当他们进一步深入分析时,团队锁定了 PKC 的“非典型”亚群,尤其是称为 PKCζ 的一种,其在肠道细胞中的活性与胃旁路样的排糖状态最为吻合。
肠道细胞中的糖泵在工作
通过单细胞 RNA 测序放大观察个体肠上皮细胞,作者发现胃旁路手术会在远端小肠特定的营养吸收细胞中同时增强 PKCζ 和 GLUT1。在细胞培养和人源肠类器官中,人工提高 PKCζ 水平或用普罗斯塔丁(一种安全激活这些非典型 PKC 酶的植物来源化合物)处理,会促使 GLUT1 转运蛋白移至细胞表面。在那里,GLUT1 表现出类似双向泵的功能:它从朝向血液的一侧抽取更多葡萄糖,并允许多余葡萄糖排出到肠腔。值得注意的是,这一路径并未显著加速细胞自身的糖酵解,表明其主要作用是将葡萄糖排弃,而非产生额外能量。
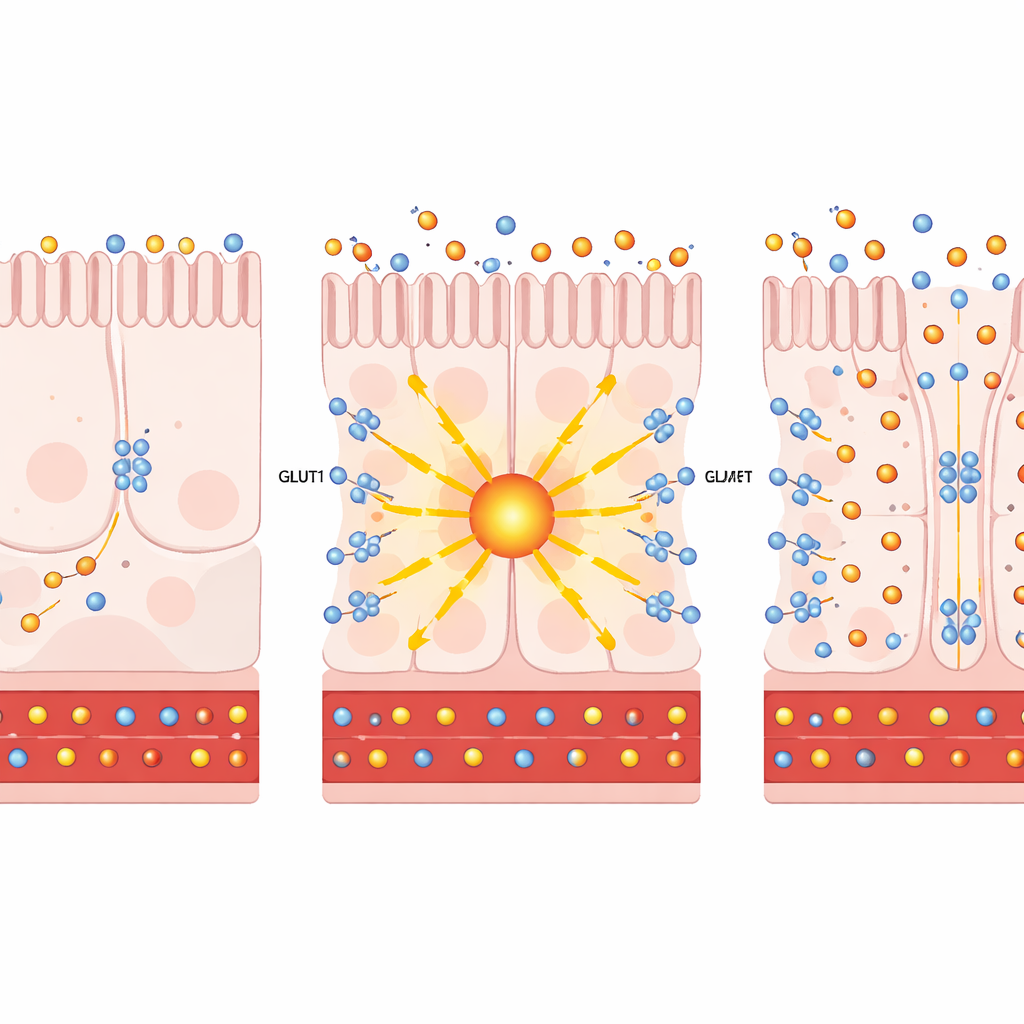
从细胞到小鼠:在无手术的情况下模拟手术效果
接着,研究团队测试在活体动物中激活该通路是否能改善糖尿病。在肥胖、胰岛素抵抗的小鼠中,向肠道特异性递送额外的 PKCζ 可减缓体重增加、降低空腹血糖并改善耐糖能力。放射性糖示踪显示更多糖被远端肠道摄取并冲洗入肠腔。在用普罗斯塔丁处理的糖尿病小鼠模型中也观察到类似结果:体重增加较少,对糖负荷的处理更好,且将更多葡萄糖导入肠道,且这些变化并未伴随胰岛素水平、食物摄入或肠道屏障完整性的改变。在组织切片中,GLUT1 出现在既面向血液也面向肠腔的细胞表面,处于从循环中拉取葡萄糖并将其推入肠腔的理想位置。
这对未来糖尿病治疗意味着什么
对非专业读者来说,关键信息是肠道可以被转换为一个可控的过剩血糖排放通道。通过激活肠上皮细胞内的特定酶——非典型 PKC——研究者能够促使细胞将更多 GLUT1 转运到表面,使其表现得像一个可逆的排水口,从血液中抽取糖并将部分排回肠腔。在小鼠中,这种由肠道驱动的葡萄糖处置改善了血糖并限制了体重增加,而没有过度刺激胰岛素、改变食欲或损伤肠道。尽管普罗斯塔丁及相关化合物尚未获批作为糖尿病药物,这项工作将 aPKC–GLUT1 通路指向了一个有前景的靶点,未来有望开发出部分复制胃旁路手术代谢益处的药物,而无需手术介入。
引用: Kang, C.W., Hong, ZY., Oh, J.H. et al. Atypical protein kinase C activation drives intestinal glucose excretion in diabetes mellitus. Nat Commun 17, 2417 (2026). https://doi.org/10.1038/s41467-026-69193-7
关键词: 肠道排糖, 2 型糖尿病, GLUT1 转运蛋白, 非典型蛋白激酶 C, 普罗斯塔丁