Clear Sky Science · zh
MerTK 触发的 TGFβ1 自分泌信号调控小胶质细胞对神经退行性变的反应
大脑清道夫如何塑造疾病进程
当大脑和视神经中的神经元死亡时,会留下大量碎片。被称为小胶质细胞的专职免疫细胞充当大脑的清道夫,吞噬这些残骸。但小胶质细胞的作用不仅限于清理:它们的反应方式既可能保护神经回路,也可能加剧像阿尔茨海默病这样的疾病。该研究揭示了小胶质细胞内一个被掩藏的自我通信回路,该回路由退化神经纤维的碎片触发,并帮助决定这些细胞对损伤的响应强度。
隐匿于退化神经纤维中的触发信号
为探究这一过程,研究者使用了一个小鼠模型,对视神经进行挤压性损伤,使眼部神经元的长突起发生退化而不致死于细胞体,从而清晰地隔离了轴突分解的后果。在这些退化纤维的表面,一种脂类分子翻转朝外,作为对附近小胶质细胞的“吃我”信号。这些信号由小胶质细胞表面的一种受体 MerTK 感知,MerTK 属于识别碎片的少数蛋白家族之一。通过选择性删除小胶质细胞中的 MerTK,研究团队证明:缺失该受体时,小胶质细胞无法发起其通常的损伤反应——它们的增殖减少、迁移减弱,并且与损伤控制和炎症相关的基因激活减少。
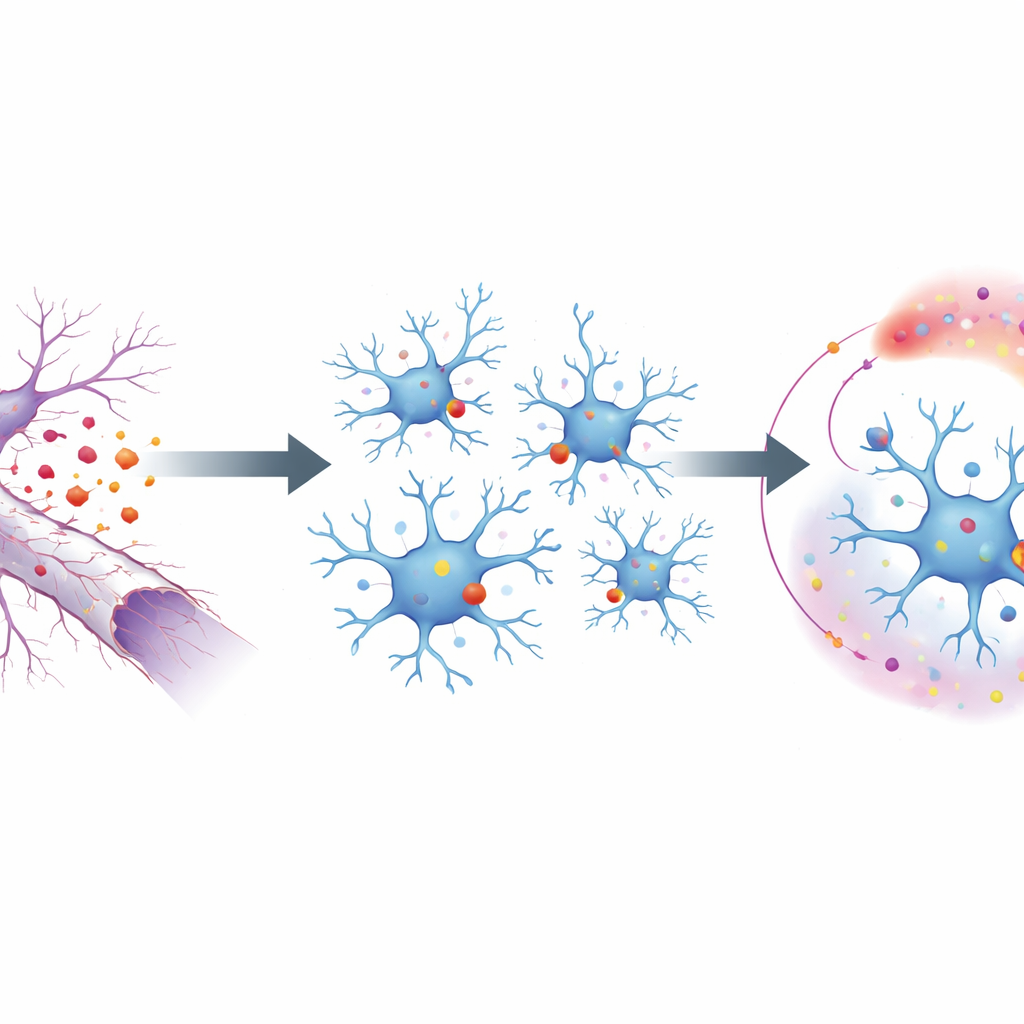
从表面信号到基因重编程
通过追踪小胶质细胞内部,科学家们阐明了 MerTK 的表面信号如何转化为基因活性的改变。他们发现 MerTK 激活了一条称为磷脂酶 C 的分子中继,进而增强了两个位于细胞核内的主控蛋白 PU.1 和 IRF8。这些因子如同小胶质细胞装配线的工头,开启许多所需的激活态基因。通过 DNA 结合图谱,研究团队发现 PU.1 和 IRF8 直接结合于编码 TGFβ1 的基因中的特定位点。当该结合位点发生突变,使得这些“工头”无法停靠时,受损神经中的小胶质细胞便无法增加 TGFβ1 的产生,而其它基线功能仍然保持完整。
小胶质细胞内的自我反馈回路
接下来的问题是 TGFβ1 在这一情境中究竟有何作用。研究表明,小胶质细胞既产生 TGFβ1 又对其作出响应,形成一种自分泌(autocrine)或自我反馈回路。当仅在小胶质细胞中基因性删除 TGFβ1 或其受体时,损伤仍会导致轴突退化,但小胶质细胞不再表现出完整的激活程式。它们的增殖减少,损伤反应和炎症相关基因的表达下降,尽管许多维持细胞稳态的身份标志仍被其他信号抑制。TGF 信号的一个关键下游分子——磷酸化的 SMAD2,在损伤后特异性出现在小胶质细胞核中;而当 TGFβ1 或其受体被敲除时,该标记大部分消失,证实了自我反馈回路被破坏。
从小鼠视神经到阿尔茨海默病大脑
为检验该通路在人工损伤模型之外是否重要,作者们考查了一个广泛使用的阿尔茨海默病小鼠模型。在这些动物中,簇集于淀粉样斑块周围的小胶质细胞表现出高水平的 PU.1、IRF8、TGFβ1 以及激活的 TGFβ 信号,呼应了视神经的发现。研究团队随后分析了来自阿尔茨海默病患者脑组织的单核 RNA 测序人类数据。在这些数据中,小胶质细胞突显为表达 MerTK、PU.1、IRF8 和 TGFB1 人类对应基因的主要细胞类型。在患者的尸检脑切片中,小胶质细胞也显示出强烈的 TGFβ 信号激活迹象,而对照供体组织中则较少。综合这些观察结果,支持了同一自我通信回路在人类疾病中也在起作用的观点。
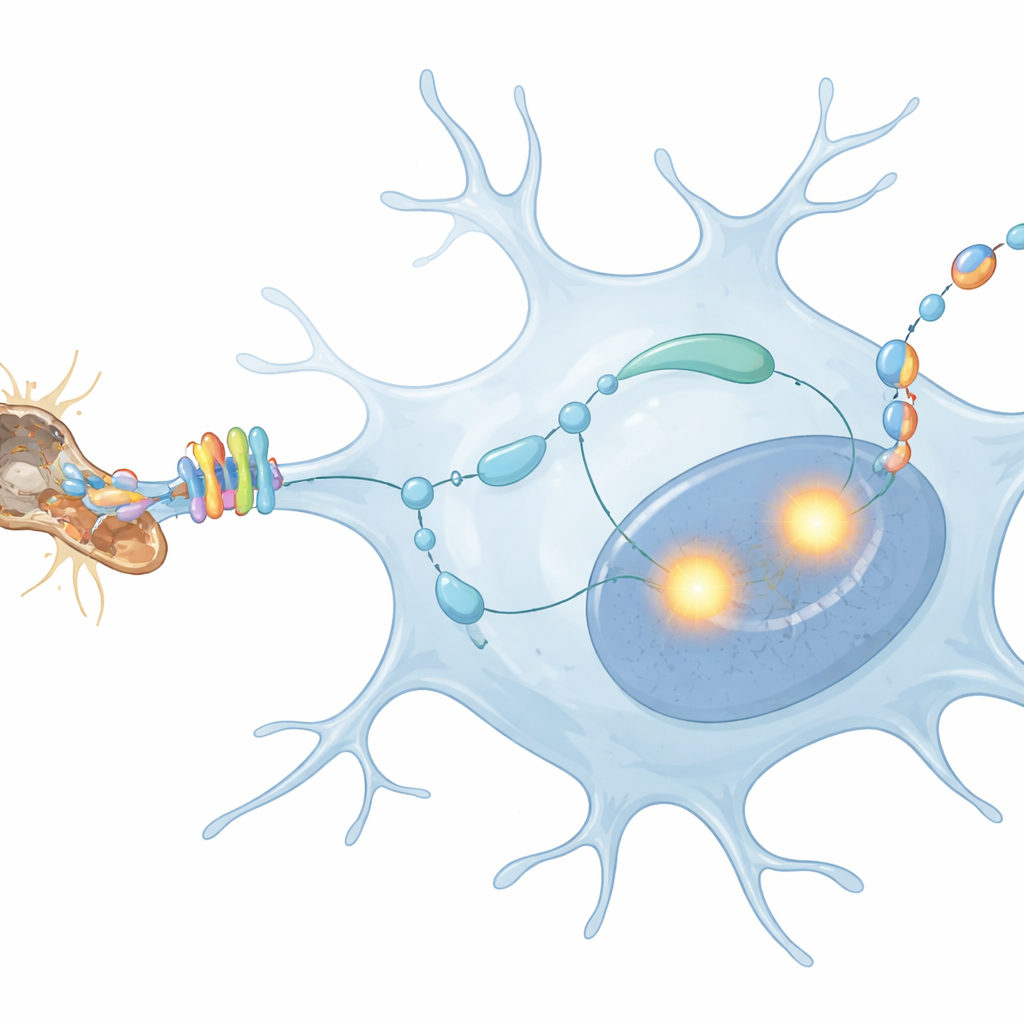
为何这种自我对话对大脑健康至关重要
这项工作揭示了一个事件链:来自退化神经纤维的碎片激活小胶质细胞表面的 MerTK,MerTK 随后增强 PU.1 和 IRF8,而它们又驱动小胶质细胞产生可反馈自身的 TGFβ1。此类自我对话使它们对神经退行性变的反应更为敏锐且可持续。对非专业读者而言,核心信息是:大脑的清洁细胞并非被动的打扫者;它们会积极倾听自身的信号,这一反馈回路可能决定它们的举动是保护神经元还是推动像阿尔茨海默病这样的疾病进展。理解并有选择地调节这一回路,或可开辟新的途径,以在保留小胶质细胞有益清理功能的同时,抑制有害的炎症反应。
引用: Huang, Y., Deng, Z., Zhou, Z. et al. MerTK-triggered TGFβ1 autocrine signal regulates microglial response to neurodegeneration. Nat Commun 17, 2312 (2026). https://doi.org/10.1038/s41467-026-69189-3
关键词: 小胶质细胞, 神经退行性变, 阿尔茨海默病, 脑炎症, TGF-β 信号传导