Clear Sky Science · zh
通过效能选择性Nav1.7抑制剂揭示人类Nav1.7失活低电压依赖性的分子决定因素
将疼痛信号的音量调低
为什么有些人轻触就会感到剧烈疼痛,而另一些人几乎感觉不到痛楚?答案很大程度上取决于神经细胞中那些控制电信号的微小蛋白质闸门。本研究揭示了其中一种闸门——Nav1.7——因其细微的结构特性而在触发疼痛中尤为重要,并说明一种天然化合物Uvarigranol D如何选择性地将其关闭。该工作指向一种新的止痛剂设计策略:在不减慢心脏或影响大脑的情况下,抑制过度活跃的疼痛神经。 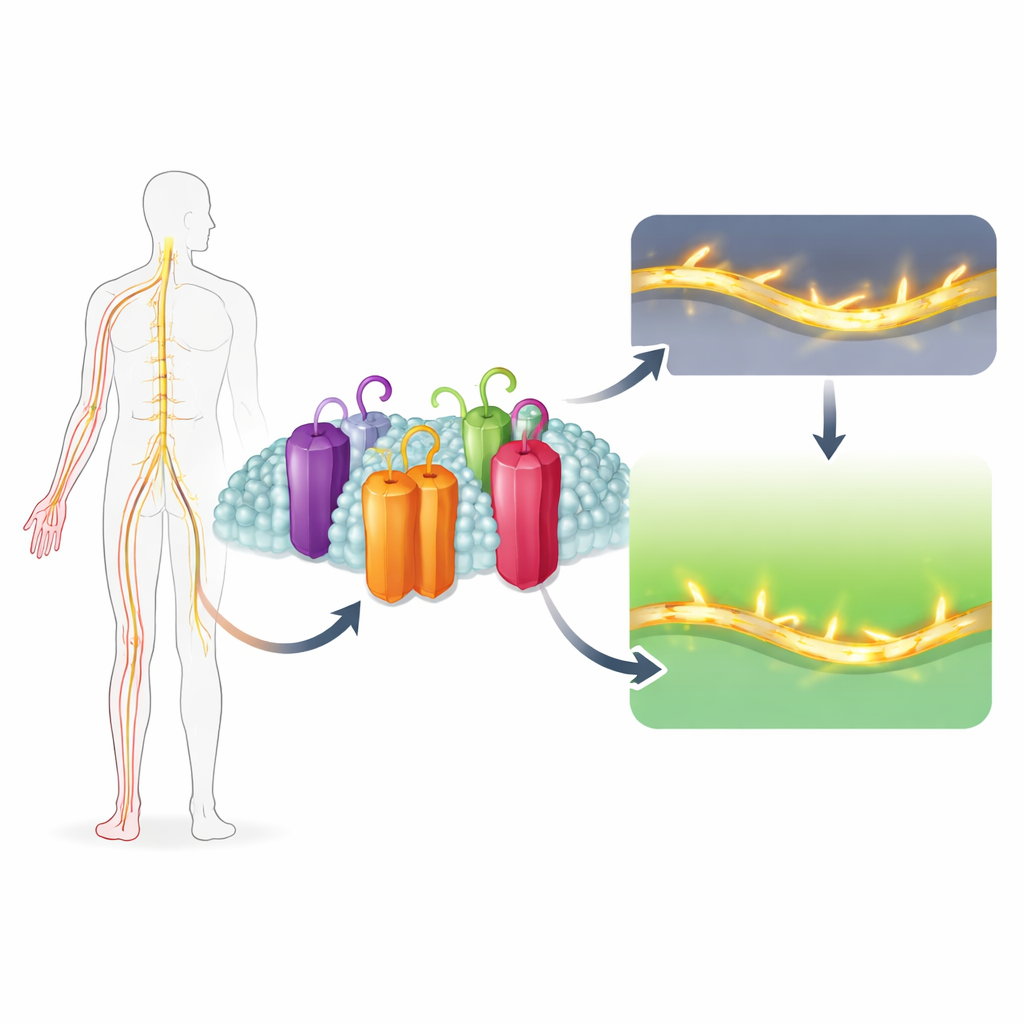
疼痛的特殊守门员
我们的神经通过钠通道产生电冲动,这些微观孔道短时间打开,让带正电的钠离子涌入细胞。人类有九种主要类型的这类通道,每种在脑、肌肉、心脏或感受疼痛的神经等不同组织中发挥作用。Nav1.7是分布在外周疼痛纤维中的那种。它不同寻常之处在于可以在比其他同类更低的电压下开关,使其能对极细微的电压变化做出反应。这使Nav1.7成为放大微弱疼痛触发信号的强大装置。遗传学研究表明,Nav1.7过度活跃会导致严重的遗传性疼痛综合征,而完全丧失功能的Nav1.7则会让人感觉不到任何疼痛。
寻找选择性阻断剂
药物开发者长期以来一直希望以Nav1.7为靶点治疗慢性疼痛,但它与对心跳和大脑功能至关重要的其他钠通道非常相似。大多数实验性药物会同时结合多种通道,导致副作用或在临床试验中失败。研究人员用一种检测膜电位变化的细胞测定筛选了1500多种天然化合物,发现了一类来自植物Uvaria grandiflora的分子,重点研究了一种称为Uvarigranol D(UGD)的化合物。UGD在多种通道上都会减弱钠电流,但它几乎完全抑制了Nav1.7,而即使在高剂量下对其他钠通道也只约半数阻断。这表明其选择性并非来自更强的结合力,而是在结合后产生了更强的功能效应。 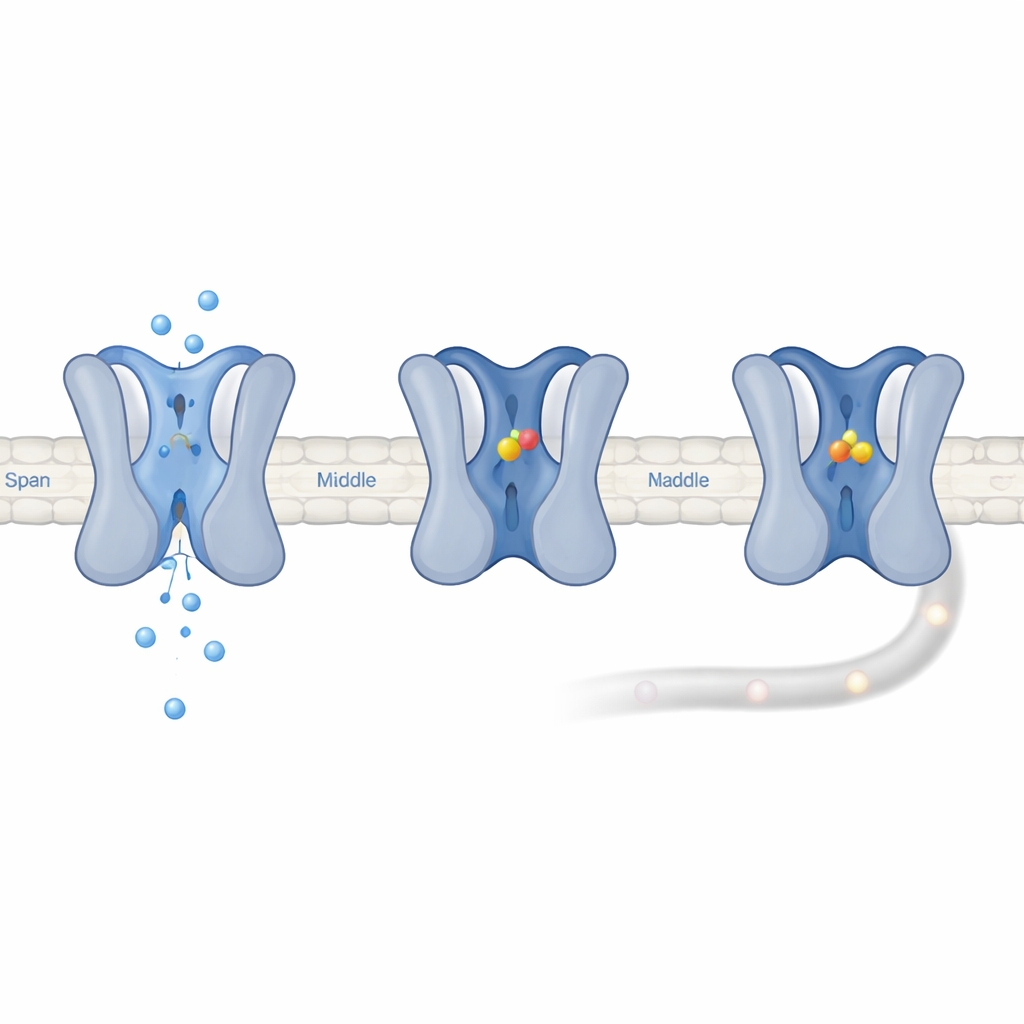
单个原子级变化使Nav1.7与众不同
为了解UGD为何对Nav1.7如此有效,研究团队构建了将Nav1.7与密切相关的大脑通道Nav1.2之间片段互换的嵌合通道。这定位到位于孔外侧开口附近、III结构域中称为S5和S6的两个结构段之间的一小段区域,是UGD完全阻断能力的关键决定因子。比对氨基酸序列发现,只有Nav1.7在1398位携带苏氨酸(threonine),而其他所有人类钠通道在该位点都含有体积更大的蛋氨酸(methionine)。当研究者将Nav1.7的苏氨酸替换为蛋氨酸时,UGD不再能完全关闭该通道;而在Nav1.2中以蛋氨酸换成苏氨酸,则使该通道表现得像Nav1.7。这一单个替换还改变了通道的电压开关行为:苏氨酸使通道在更负的电压下激活和失活,并加速这些过程,这些特性使得Nav1.7即便在疼痛神经的正常静息电位附近也更倾向于处于非静息态。
将通道锁定在“下位”静息模式
电生理记录显示,UGD并不粘附于关闭或短暂打开的Nav1.7。相反,它更偏好那些进入了长持续时间的“慢失活”状态的通道——在该状态下孔被关闭,并需数百毫秒或更长时间才能恢复。当存在UGD时,通道从该状态中恢复所需的时间大约延长了十倍,说明UGD稳定了这一状态。计算机模拟表明,UGD嵌入在III结构域的一段环与IV结构域的一个螺旋相遇处形成的一个口袋中,并与五个氨基酸发生关键接触。对这些残基的任何突变都会削弱UGD的效应,证实了该口袋的重要性。由于Nav1.7富含苏氨酸的结构使其在更低电压下更容易进入失活状态,因此其更大比例的通道处于UGD偏好的结合状态,这解释了尽管结合强度相似,Nav1.7在功能上却比其它同类通道受到更强抑制的原因。
从离子孔到缓解疼痛
最终重要的是这些分子事件如何影响真实细胞。在大鼠背根神经节的感痛神经元中,UGD显著减少了动作电位的数量——携带疼痛信息的快速电压尖峰——并在低微摩尔到亚微摩尔浓度下最终完全阻断它们。相比之下,主要使用另一种钠通道(Nav1.5)并在略低电位下静息的类人心肌细胞来自干细胞分化的模型,对UGD的敏感性约低60倍。这表明像UGD这样的“效能选择性”阻断剂可以仅因为Nav1.7更频繁地处于其易被药物结合的失活状态,而在抑制疼痛通路方面远强于对心脏或其他兴奋组织的影响。
这对未来止痛疗法的意义
该研究揭示了一个小的结构细节——单个苏氨酸——是Nav1.7特殊低电压行为及其产生“阈值电流”(决定疼痛神经是否发放的微弱信号)的基础。通过结合并稳定该通道的失活形式,UGD利用了这一内在倾向,使Nav1.7受到的抑制远强于其他钠通道。对于非专业读者而言,结论是作者已经绘制出这个体内“疼痛守门员”的精确薄弱点,并展示了一种在不严重干扰心脏或脑通道的情况下按压它的方法。这一见解为设计新型止痛药开辟了道路,这类药物通过针对电压行为和通道状态来抑制过度活跃的疼痛神经,而不是仅仅追求对Nav1.7更紧的结合。
引用: Zhao, F., Xi, C., Li, J. et al. Molecular determinant of low-voltage dependence of human Nav1.7 inactivation revealed by efficacy-based Nav1.7 selective inhibitor. Nat Commun 17, 2559 (2026). https://doi.org/10.1038/s41467-026-69184-8
关键词: Nav1.7 钠通道, 慢性疼痛, Uvarigranol D, 状态依赖性抑制, 电压门控钠通道