Clear Sky Science · zh
细菌PstSCAB转运蛋白对磷酸盐摄入的分子机制
微小营养为什么对我们至关重要
从人类神经元到土壤细菌,每一个活细胞都依赖磷。该元素参与能量储存、构建DNA并维持细胞膜完整性。然而在环境中,可被细胞实际摄取的可用磷酸盐常常匮乏。许多致病细菌在磷酸盐不足时依赖一种超高效的分子机器——PstSCAB转运蛋白——来搜寻磷酸盐。弄清这台机器的运作方式不仅是基础科学问题;它还有可能为通过掐断细菌这一重要营养来源来削弱感染提供新思路。
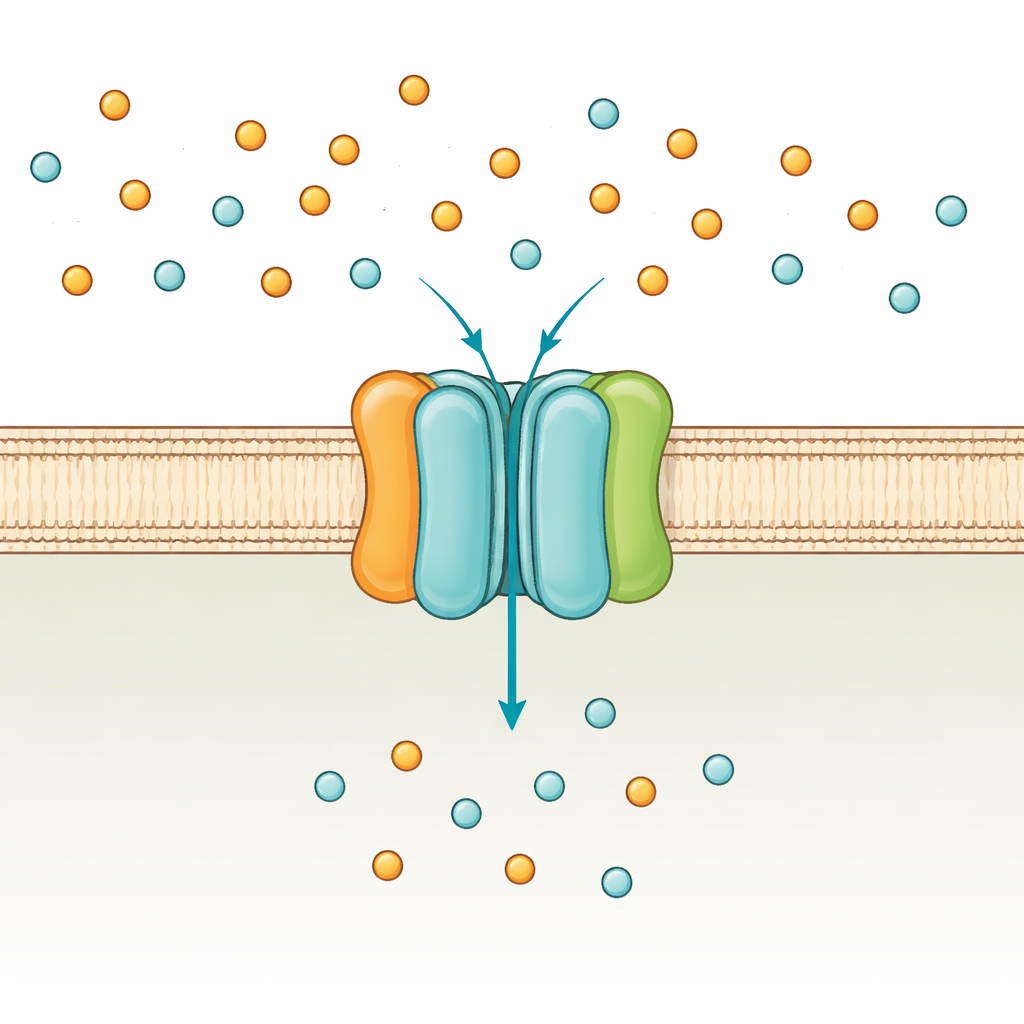
细胞的磷酸盐看门人
像大肠杆菌这样的细菌使用两条主要途径来摄取磷酸盐:一种在磷酸盐充足时起作用的低亲和力系统,以及在缺乏时开启的高亲和力PstSCAB系统。PstSCAB嵌入细胞膜,由细胞的通用能量货币ATP提供动力。它由五个部分构成:两条形成通道的膜内亚基(PstA和PstC)、位于膜外负责抓取磷酸盐的可溶性“捕手”蛋白(PstS),以及一对在细胞内部燃烧ATP以驱动转运的PstB亚基。由于该系统还参与控制多种与细菌毒力相关的基因,PstSCAB的突变会削弱引起尿路感染、农畜败血症及结核等疾病的病原体。
捕捉机器运作瞬间
此前,科学家对PstSCAB的认识多为片段式,主要是对捕手蛋白PstS的单独观察。本研究中,研究人员使用高分辨率冷冻电镜来可视化整个转运蛋白在其工作周期的若干关键步骤。他们将细菌蛋白重建入人工膜“纳米盘”并快速冷冻,使分子在运转中被捕获。通过对蛋白进行精细调控并有选择地添加或不添加ATP,他们获得了三种主要构象的结构:一个未结合捕手的静止向内构象、一个携带磷酸盐的PstS停靠到膜复合体的前易位态,以及一个结合ATP的催化中间体,在该状态下磷酸盐被夹持在转运体内。
构象变化如何移动磷酸盐
这些图像展示了协调的构象变化如何把磷酸盐从外部运到细胞内部。在静止态,由PstA和PstC形成的通道仅朝向细胞内开放;外侧被一组“闸门”残基封闭,导致磷酸盐尚无法从外部进入。当携磷酸盐的PstS在前易位态停靠时,它嵌入PstA和PstC的柔性环之间,但显著的是膜亚基几乎没有发生形变。真正的转折发生在PstS开始打开其两叶以释放磷酸盐时,同时两枚PstB亚基合拢以结合ATP。ATP结合将PstB夹成二聚体,并拉动PstA与PstC中的连接螺旋,翻转整个通道为向外构象,从而将一个特定的磷酸结合口袋暴露到外侧。
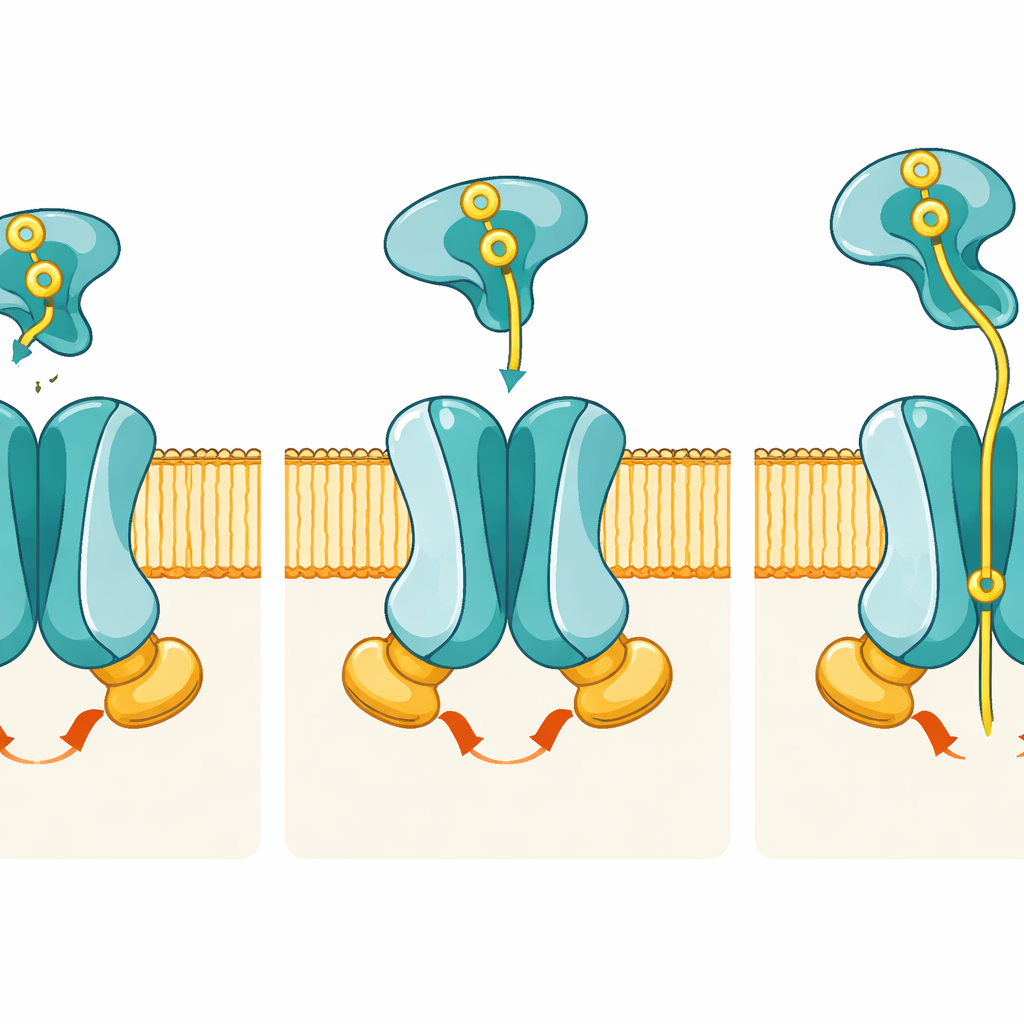
为磷酸量身定做的口袋
在向外、结合ATP的构象中,作者在膜区中部发现了与磷酸离子相符的电子密度。该离子被带正电的氨基酸——尤其是来自PstA和PstC的两处精氨酸——像分子指尖一样托住,握住带负电的磷酸盐。计算机模拟表明磷酸在这个口袋中能在微秒尺度上稳定结合,遗传学实验也证实了其重要性:当这些关键残基被突变时,转运蛋白仍会耗ATP但磷酸盐摄入显著下降。这种“能量消耗位置”与“货物识别位置”的分离凸显了该机器对磷酸盐识别的高度精细调节。
从结构快照到医学前景
综合这些结构与生化验证,研究描绘出一个完整循环:PstS在外侧捕获磷酸盐,停靠到向内的转运体,然后在PstB结合并水解ATP的耦合下,引发一次翻转,使磷酸盐进入膜内的结合口袋并最终进入细胞内部。ATP水解后,机器恢复到静止态,准备下一轮运作。对非专业读者来说,关键信息是:我们现在拥有了许多细菌如何在低磷环境中生存并调控毒力的原子级蓝图。这个详尽的地图可以指导设计阻塞转运蛋白或其捕手蛋白的药物、抗体或肽,将这一必需营养通道变成一个易受攻击的治疗靶点。
引用: Xiao, H., Li, S., Qi, R. et al. Molecular mechanism of phosphate import by the bacterial PstSCAB transporter. Nat Commun 17, 2294 (2026). https://doi.org/10.1038/s41467-026-69153-1
关键词: 磷酸盐运输, 细菌营养摄取, ABC转运蛋白, PstSCAB, 抗菌靶点