Clear Sky Science · zh
囊膜多糖转运蛋白Wza-Wzc复合体的分子见解
细菌如何穿上看不见的盔甲
致病细菌常用富含糖的外衣——囊膜,来保护自己,帮助它们躲避免疫系统并抵抗恶劣环境。本研究以原子级细节揭示了常见肠道细菌中一台关键装置如何合成并输出这种糖状盔甲。理解这一过程可能为开发新型抗生素和疫苗提供思路,这类策略通过剥夺病原体的保护屏障而不仅仅试图直接杀死它们。
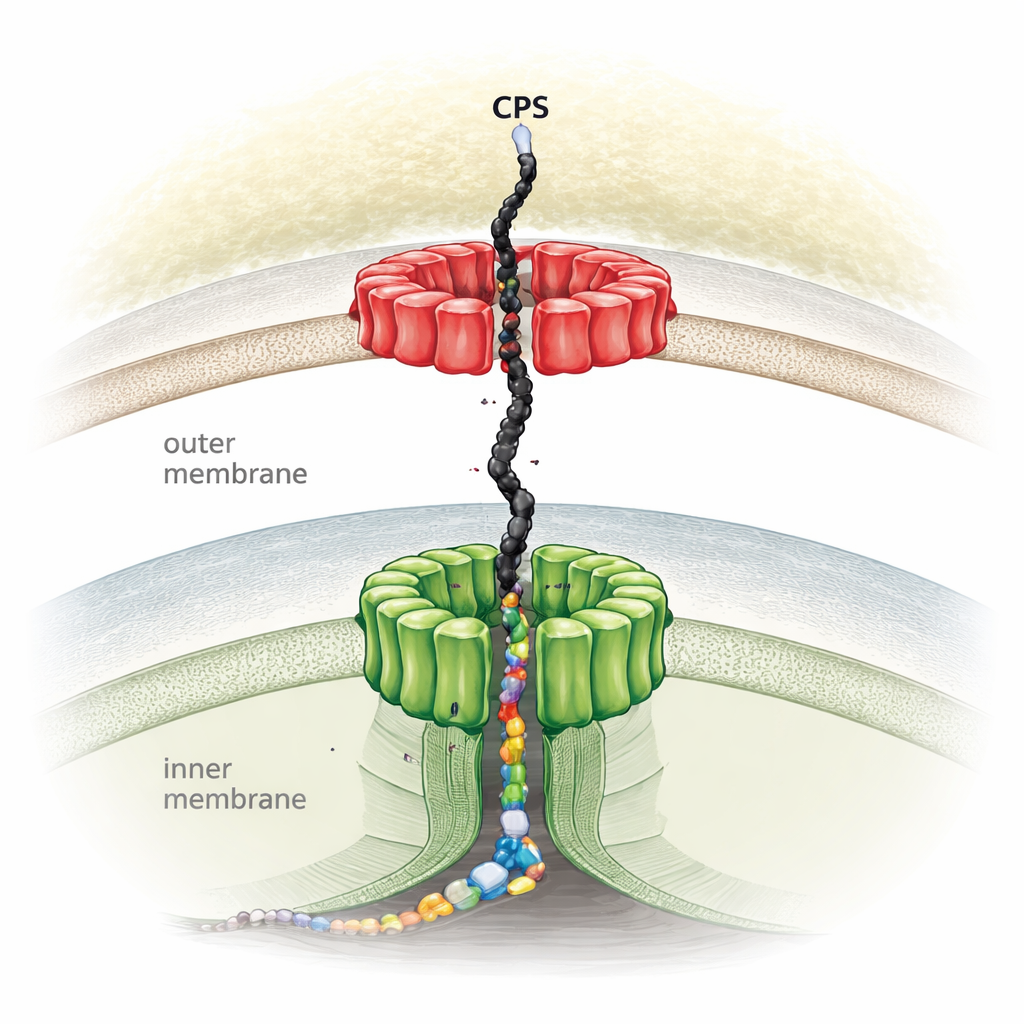
包围危险菌的糖盾
许多有害细菌用囊膜多糖包裹自己——这些由长而分支的糖链构成的厚外层能帮助它们躲避免疫攻击、抵抗抗生素并形成抗损伤的生物膜。该研究聚焦于大肠杆菌,这是一个研究透彻的模式生物,使用一种广泛存在的途径(称为Wzx/Wzy依赖通路)来组装这些糖链。在此通路中,糖的重复单元先在细胞内合成,翻转穿过内膜,连接成长聚合物,最终被推出去形成囊膜。尽管研究者已知主要蛋白组分的名字,但尚未完整了解它们如何组装成跨越整个细菌包膜的单一机器。
揭示一条全长的分子通道
研究者使用高分辨率冷冻电子显微镜解析了Wza-Wzc复合体的完整三维结构——这是大肠杆菌K12中囊膜多糖的核心输出机械。他们发现每种蛋白各由八个拷贝组装成一条高耸的连续通道,从内膜延伸至外膜,跨越两膜之间的潮湿间隙。Wza位于外膜,形成一个刚性的环形出口端口,而Wzc则在内膜锚定,构成一座柔性的塔状结构。二者共同形成一条约250–360埃长的通道,通道足够宽以引导一条大型、柔性的糖聚合物从内膜合成处一直输送到细胞表面,防止其扩散或泄漏。对Wza和Wzc关键接触点的突变会完全阻止囊膜生成,证实该联合复合体对输出至关重要。
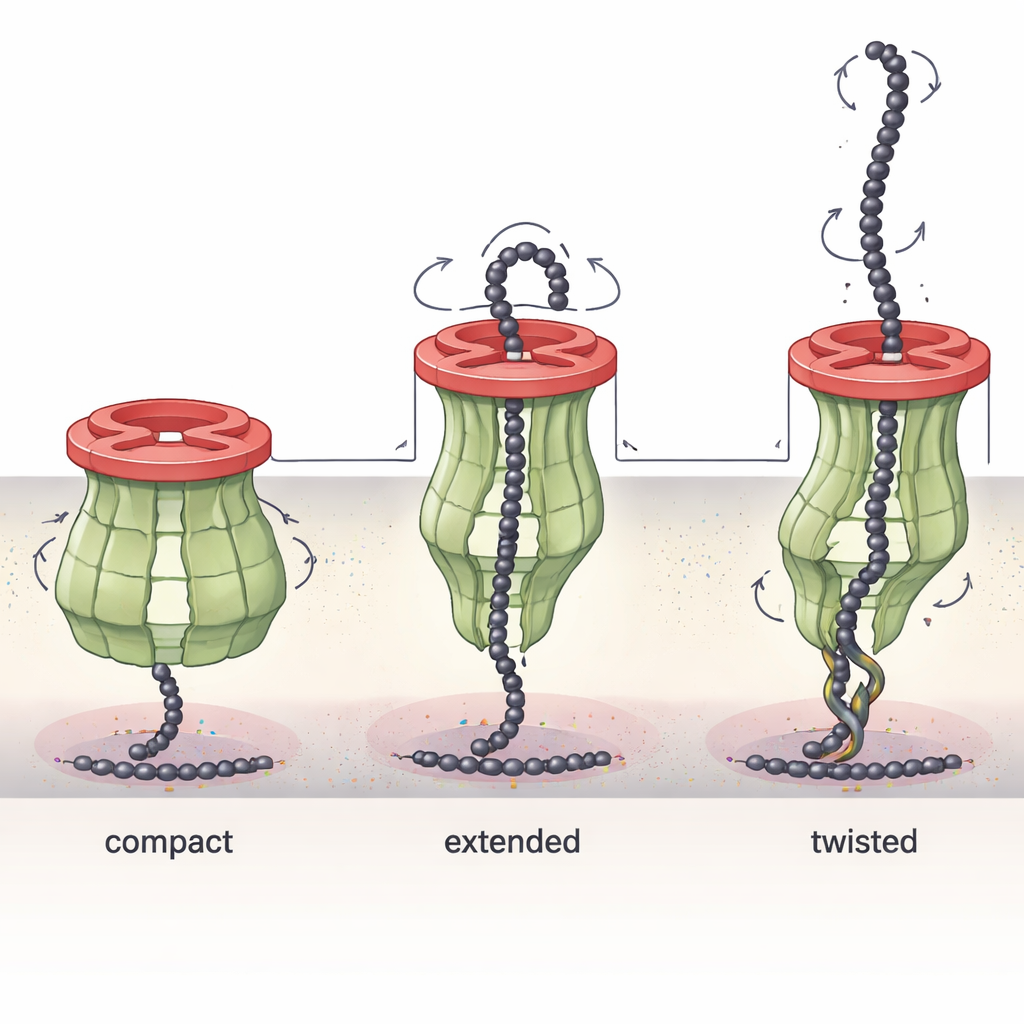
能变形的引擎将糖拉出
Wzc部分被发现具有显著的动态特性。通过在不同化学条件下获取若干结构“快照”,研究者表明Wzc那长长的周质臂可以像机械杠杆一样弯曲、扭转和伸展。在一种构象下,通道紧凑且密封;在其他构象中,Wzc发生旋转和伸长,微调通道的宽度与形状。在某些构象中,这些臂部部分阻塞通道或与Wza的接触变松,极端情况下一个Wzc环甚至可以同时与两个Wza环相互作用。这些观察支持这样一个模型:Wzc有点像分子绞盘——它的扭转与伸长运动帮助把不断延长的糖链从内膜处拉出并送入外膜的孔道,同时协调整台机器的装配与拆解。
识别糖基的停靠台
另一个谜题是该机器如何在细胞内外众多碳水化合物中识别出正确的糖构件。Wzc包含一个位于内膜正上方的“果冻卷”(jellyroll)结构域,其功能此前不明。将该结构与已知的糖结合蛋白做结构比较,并结合对纯化碳水化合物阵列的生化测试,揭示该结构域可以识别与大肠杆菌囊膜中发现的类似的特定糖基序列。去除果冻卷区域会明显降低但不会完全消除囊膜生成,表明它充当着一个停靠台,捕获新翻转过来的糖单元并将其引导到由Wzc与酶Wzy共同形成的聚合平台,Wzy负责将这些单元缝合成长链。
协调生长、输出与复位
最后,研究将这些结构特征与一个基于磷酸化的生化调控系统联系起来——即可逆地向Wzc的富酪氨酸尾部添加或移除磷酸基团。当Wzc高度磷酸化时,它主要以松散的单体形式存在;当伴侣酶移除磷酸后,Wzc的激酶结构域组装成一个八聚体,重排其臂部以便与Wza结合并包围聚合酶Wzy。随着囊膜链的生长并被拉过通道,Wzc的进一步扭转与伸展可能有助于将完成的聚合物释放到Wza以便输出。分泌完成后,Wzc重新自我磷酸化,促使复合体解体并为下一轮囊膜合成重置系统。
为何这对抗感染很重要
通俗地说,这项工作几乎逐个螺栓地展示了细菌如何构建一条分子管道,将长糖链从细胞内部穿到外部,在那里形成保护性的披风。通过绘制Wza-Wzc复合体的结构与运动,并指出糖识别与调控元件,研究强调了若干潜在薄弱点,未来的药物或疫苗可能针对这些部位。破坏这一输出机器不一定会直接杀死细菌,但可以剥夺它们的盔甲,使其对免疫防御和现有抗生素更为脆弱。
引用: Yuan, B., Sieben, C., Raj, P. et al. Molecular insights into the capsular polysaccharide transporter Wza-Wzc complex. Nat Commun 17, 1436 (2026). https://doi.org/10.1038/s41467-026-69136-2
关键词: 细菌囊膜, 多糖分泌, Wza-Wzc复合体, 冷冻电镜结构, 抗菌靶点