Clear Sky Science · zh
使用光氧化还原催化对药物及未活化叔胺进行晚期N-Me选择性烯基化与炔基化
为何改造已有药物仍然重要
当今许多药物疗效良好,但在安全性、副作用或靶向精确性方面仍有提升空间。化学家越来越倾向于在开发后期对现有药物进行温和的“微调”,而不是从头发明全新的分子。该研究展示了如何利用可见光束在常见药物构件上接入新片段,从而产生改良的抗抑郁候选物,并为更快地完善疗法打开了一条捷径。
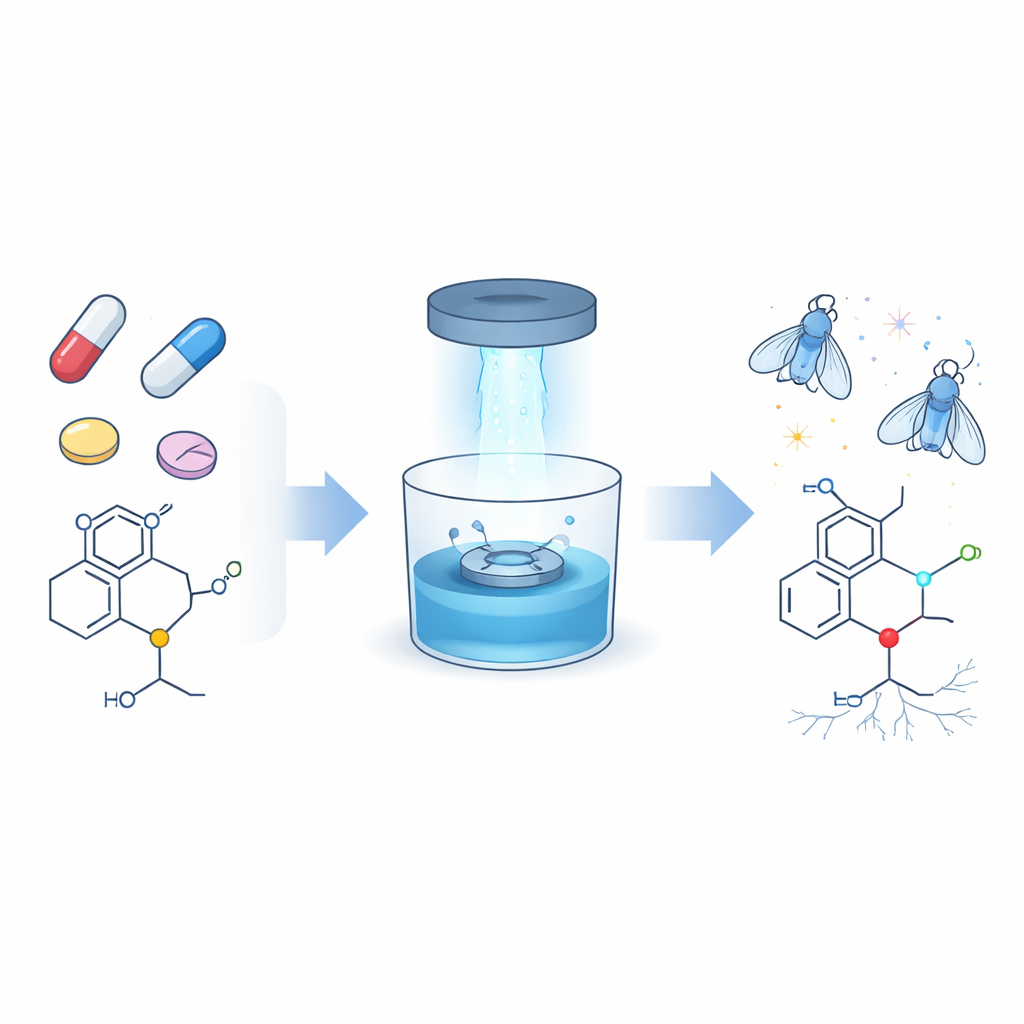
升级许多药物中的常见特征
令人惊讶的是,当代药物中有很大一部分——超过五分之二——包含富含氮的片段称为胺,而其中大多数是称为叔胺的亚型。它们出现在抗生素、抗癌药、抗过敏药、止痛药和抗抑郁药中。到目前为止,化学家一直难以在这些基团中选择性地只修改一个微小部分,即N-甲基单元,尤其当它周围有多处几乎相同的碳–氢键时。作者旨在开发一种温和、可靠的方法,在不干扰药物其余部分的情况下,将新的“把手”——特指碳–碳双键(烯烃)和三键(炔烃)——连接到该N-甲基位置。
用光逐一改写化学键
研究团队转向光氧化还原催化,这是一种利用可见光和光敏催化剂在温和条件下移动单电子并触发反应的技术。在他们的体系中,蓝光激发有机催化剂,催化剂暂时从叔胺上抽取一个电子。这一步在N-甲基位点产生短寿命自由基,该自由基可以与携带乙烯基或炔基的精心选择的反应伙伴结合。通过调节反应条件——溶剂、碱和添加剂的选择——研究者获得了高产率和优良的控制,使得新基团几乎专一地落在N-甲基位置,即便存在多个相似位点。他们在一组简单胺和实际药物(包括抗组胺药、心血管药、抗感染药和若干抗抑郁药)上展示了这一方法。
从化学微调到更强的抗抑郁作用
为检验这些结构修改是否具有医学意义,作者将注意力集中在伊米普明(imipramine)上,这是一种长期使用的三环类抗抑郁药。他们设计并建模了20多种伊米普明变体,在这些变体中,新的烯基或炔基延伸上携带芳环,可以紧密嵌入人体血清素转运体的疏水口袋——该蛋白调控与情绪相关的神经递质血清素的水平。计算对接表明,这些改造分子中许多应与母体药物具有相当或更好的结合能力。随后,研究者使用新的光驱动方法合成了最有希望的候选分子,并在生物体系中进行测试:基于社会隔离的果蝇抑郁模型,以及对其中两种最优化合物在活跃运输血清素的小鼠神经细胞中的测试。
果蝇与细胞如何揭示更强效的药物
在被隔离的雄性果蝇中,类抑郁行为表现为攻击性增加。喂食伊米普明可降低这种攻击性,反映其在人的抗抑郁作用。值得注意的是,几种通过新方法合成的伊米普明衍生物同样能降低攻击性,有四个候选物的效果甚至优于伊米普明本身。在培养的小鼠海马细胞中,两种领先化合物在阻断血清素再摄取方面比伊米普明更强,这一点通过直接化学测定血清素以及通过进入细胞后发光的荧光染料两种方法得到证实。这些测试表明,在N-甲基位点进行的细微晚期改动不仅在分子层面上发生改变,而且确实能增强抗抑郁效力。
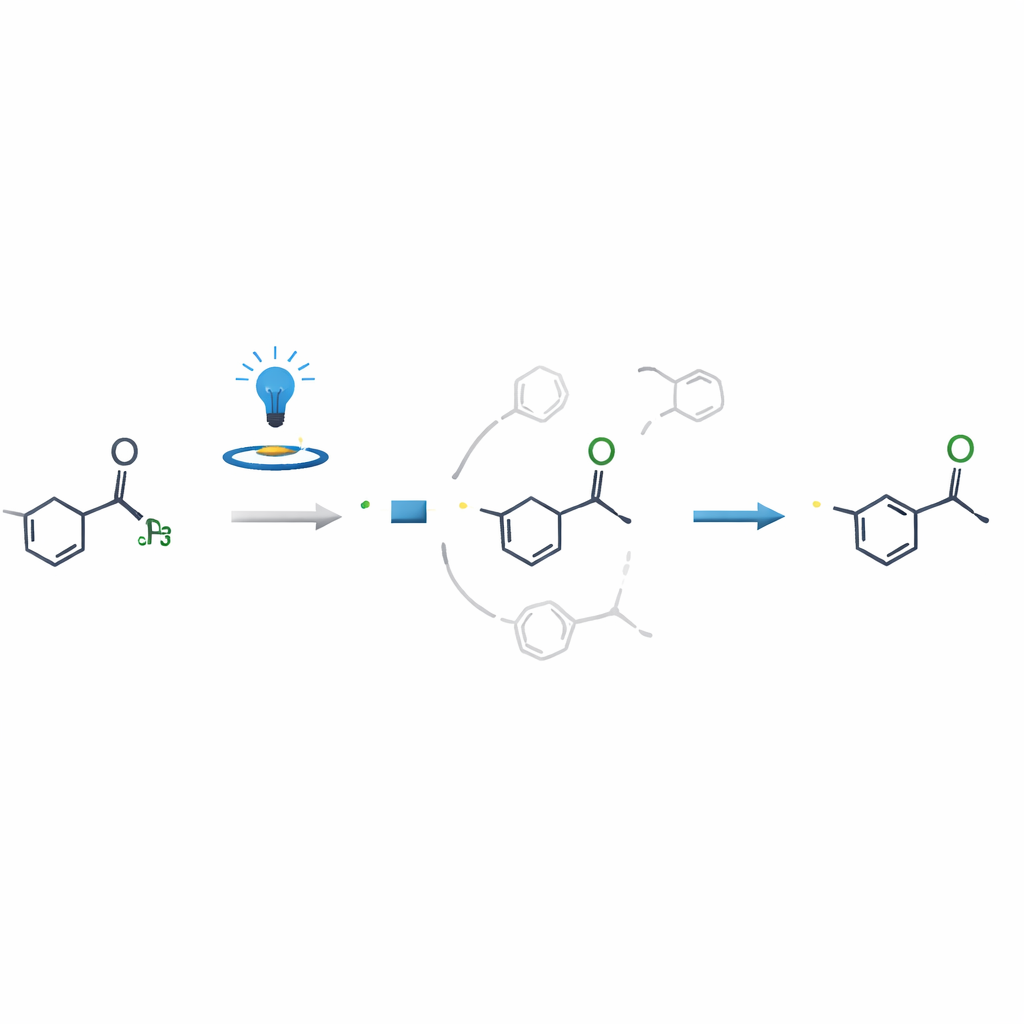
为何该反应如此具有选择性
一个关键科学问题是,为什么当其他邻近位点看起来同样活泼时,反应还能如此干净地只修饰N-甲基基团。通过对照实验、电子自旋测量和详尽的计算,作者表明决定性步骤并不是自由基首次形成的时刻,而是该自由基加成到烯基或炔基伙伴的那一步。从N-甲基自由基通向最终产物的途径在能量上更容易且速度更快,从而有效地将反应导向单一产物。这个认识有助于解释高选择性,也可为其他复杂分子上的类似策略提供指导。
这项工作对未来药物意味着什么
总体而言,该研究引入了一种可行的方法,可对含叔胺的现有药物进行外科式升级,添加紧凑的化学“把手”来调节它们与生物靶点的相互作用或与其他组件的连接。通过证明这种晚期修改能在简单的动物与细胞模型中将一种已确立的抗抑郁药转变为更有效的变体,该工作指向了现代合成化学、计算与生物学的强大结合。随着该方法推广到其他药物,它可能加快候选药物的改良,并帮助以更佳的性能与安全性刷新既有疗法。
引用: Paul, S., Mahato, S., Mahapatra, S.K. et al. Late-stage N-Me selective alkenylation and alkynylation of drugs and unactivated tertiary amines using photoredox catalysis. Nat Commun 17, 2695 (2026). https://doi.org/10.1038/s41467-026-69131-7
关键词: 光氧化还原催化, 晚期功能化, 叔胺, 抗抑郁药设计, 血清素转运体