Clear Sky Science · zh
通过代谢竞争与毒性沉默的工程细菌疗法抑制出血性大肠杆菌
作为活体药物的友好细菌
某些大肠杆菌株引起的食物中毒远不止胃肠不适。所谓的肠出血性大肠杆菌(EHEC)会释放强效毒素,尤其在儿童中可诱发肾功能衰竭,而常规抗生素有时反而会加剧毒素释放。本研究探讨了一种不同的治疗思路:使用经工程改造的益生菌和一种存在于人乳中的糖,封装在智能微囊中,以在不扰动肠道生态的前提下,通过竞争代谢和抑制毒性来击退危险细菌并压制其有害行为。
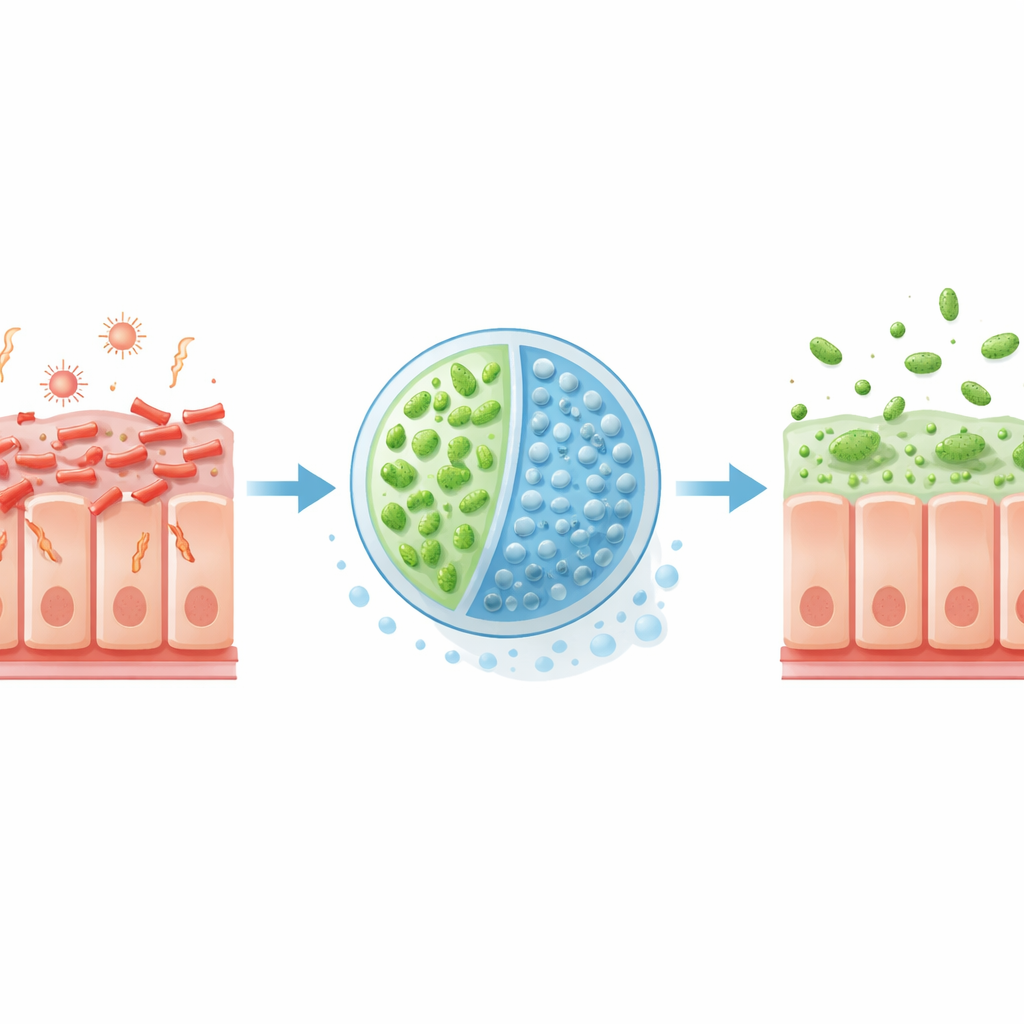
为什么有些大肠杆菌如此危险
EHEC是一种常经食物传播的病原体,常从半熟肉类或受污染的蔬果获得。进入肠道后,它能紧密附着于肠上皮细胞并注入蛋白,重塑细胞表面,形成有利于细菌附着和扩散的“着陆点”。与此同时,EHEC产生志贺毒素(Shiga toxin),这些毒素进入血流可损伤血管,有时导致危及生命的溶血尿毒综合征。许多抗生素会使这些细菌产生应激并触发更多毒素释放,因而临床上能用的安全选择有限,这使得靶向的新方法尤其受到期待。
对益生菌重新编程以饿死并解除EHEC武装
研究人员选择了长期使用的益生菌株大肠杆菌Nissle 1917,并将其改造为一种治疗性微生物EcN3。他们为EcN3引入了额外基因,使其能更高效地分解一种大肠内EHEC偏好的糖酸——葡糖醛酸。同时,他们赋予EcN3一种酶,可将母乳糖2′‑岩藻糖乳糖(2′‑fucosyllactose)裂解为乳糖和岩藻糖两部分。乳糖在细菌内部充当“开关”,启动EcN3增强的营养利用系统,帮助其大量摄取葡糖醛酸,从而剥夺EHEC的食物来源;而释放出的岩藻糖则作为信号,促使EHEC下调关键毒力基因,降低其形成紧密附着和造成损伤的能力。
在合适部位释放疗法的智能囊
单纯将工程细菌和糖喂入肠道并不足够:胃酸可能杀死益生菌,其他微生物也可能在糖到达结肠前就将其消耗掉。为此,团队构建了多腔微球——由海藻酸盐凝胶制成的微小颗粒,内含两个独立腔室。一个腔室装载EcN3,另一个装载2′‑岩藻糖乳糖,使二者在到达大肠前保持隔离。这些微胶囊可抵抗模拟胃液的降解,但在类似结肠的环境中溶解,准确释放工程细菌和糖。在小鼠中,与直接给药相比,封装系统提高了EcN3的存活率并更强烈地激活了其工程化基因。
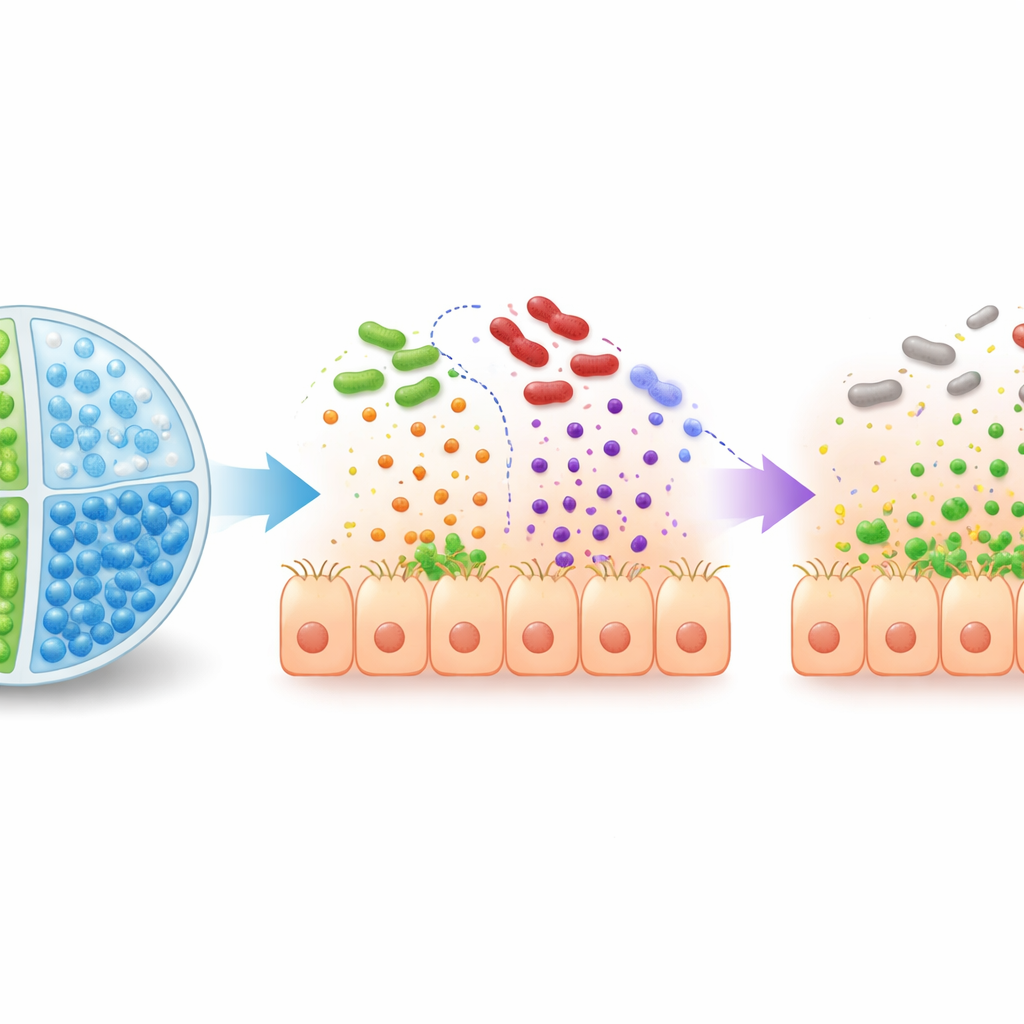
在动物模型中测试保护效果
团队在感染EHEC的幼年兔和感染与人类疾病类似的近缘病原体鼠伤寒志贺菌(Citrobacter rodentium)的小鼠中测试了该策略。感染后用EcN3加2′‑岩藻糖乳糖治疗时,动物肠道中的致病菌数量减少,细菌附着相关基因的表达降低,肠组织损伤减轻——且没有增加志贺毒素的产生。作为预防措施,游离(未封装)组合效果欠佳,因为糖被现有微生物群快速消耗。相比之下,当EcN3和2′‑岩藻糖乳糖在双腔微球中共同递送时,兔和小鼠的致病菌定殖显著减少,疾病程度减轻,存活率提高。
帮助有益微生物与肠屏障恢复
通过DNA测序分析肠道菌群,科学家发现感染扰乱了正常微生物平衡,促使有害的Citrobacter增多而有益群体减弱。使用工程微囊的治疗不仅降低了病原体水平,还将群落恢复到更健康的状态,特别是增加了已知有益的乳酸杆菌属(Lactobacillus)。肠道屏障功能的多项指标也呈现类似结果:接受封装疗法的动物显示出更多与黏液和紧密连接相关的基因、更厚的保护性黏液层以及更少的荧光示踪物从肠道漏入血流,表明肠壁更紧密、炎症更轻。
对未来无抗生素感染疗法的一瞥
总体而言,这项工作展示了一种针对一种难治食源性感染的双重靶向策略。通过将在营养竞争中占先并能感知良性糖信号的工程益生菌,与将两者递送到结肠的微囊相结合,该疗法削弱EHEC、降低其数量并保护肠道,而无需依赖传统抗生素。尽管还需更多安全性和临床研究,但这一方法展示了活体药物与智能材料未来可能为管理严重肠道感染并减少对常规药物依赖提供的精确且有利于微生物组的途径。
引用: Ma, G., Liu, R., Li, X. et al. Engineered bacterial therapy suppresses Enterohemorrhagic Escherichia coli through metabolic competition and virulence silencing. Nat Commun 17, 2307 (2026). https://doi.org/10.1038/s41467-026-69126-4
关键词: 工程益生菌, 肠道感染疗法, EHEC, 微生物组, 药物输送微球