Clear Sky Science · zh
三萜类抗真菌药物抑制真菌β−1,3-葡聚糖合酶的机制
为何遏制真菌感染很重要
真菌感染每年悄然导致超过一百万人死亡,并威胁全球农作物与生态系统。临床可用的抗真菌药物种类有限,且一些危险的真菌正在进化以逃避它们。此研究在分子层面揭示了一类新型抗真菌药物如何结合并使真菌用于构建保护性细胞壁的关键酶失活。理解这一过程为设计能克服耐药真菌的更佳治疗策略提供了路线图。
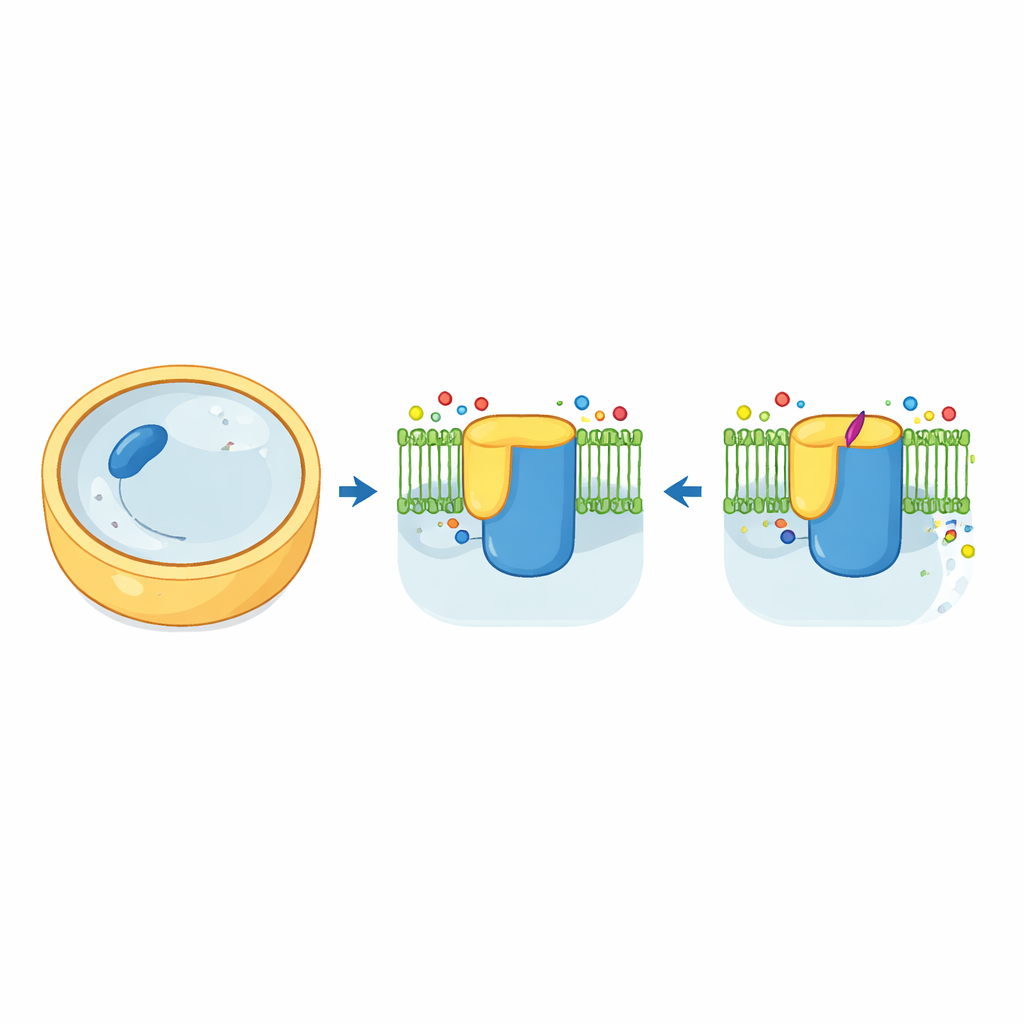
真菌细胞壁的“造砖机”
真菌细胞包裹在由一种称为β-1,3-葡聚糖的糖基聚合物构成的坚韧细胞壁中。制造并输出这种聚合物的酶,称为β-1,3-葡聚糖合酶,既像造砖机又像传送带。在面包酵母中,该机器由两种高度相似的亚型构成,Fks1与Fks2,均嵌插在细胞膜中并受一个名为Rho1的小型辅助蛋白控制。作者利用冷冻电子显微镜获取了Fks1与Fks2在天然状态下的高分辨率三维构象。结构显示了一个大的胞质“工作台”连接着一片跨膜螺旋丛,中间有一个腔体,很可能作为新生葡聚糖链穿出细胞的通道。
天然产物药物如何抓住该酶
临床重要的三萜类药物,包括口服药物ibrexafungerp,其源于一种天然化合物enfumafungin。此前人们并不清楚这些药物究竟在葡聚糖合酶的何处结合。研究者解析了Fks1与Fks2与enfumafungin结合的结构。令人意外的是,药物并未楔入催化位点(糖单位连接处)。相反,它嵌在名为TM5的一根膜螺旋的外侧部分,位于距催化中心约三纳米的膜内,靠近推测的葡聚糖出口通道。该斑块中的关键氨基酸包裹药物的疏水核心并接触其酸性尾部,而药物的糖基附属部分几乎不与蛋白接触——这解释了化学家为何能改造该糖基部分而不丧失效力。
能冻结运动机器的药物
乍看之下,酶在有无enfumafungin时的整体形状几乎没有改变。关键差别在于周围脂质的组织方式及某些螺旋的柔性。药物结合时,邻近的一个芳香族侧链旋转以夹住enfumafungin,并与另一残基一道稳定与药物并置的有序脂质。额外的类固醇状脂质在一组水平螺旋周围整齐排列,这些螺旋有助于界定葡聚糖的输出路径。这些脂质像楔子和支柱一样,将螺旋和通道入口锁定为特定的“基态”构象。遗传学实验表明,改变许多药物或这些类固醇的接触点会削弱药物结合或破坏酶功能,并且这些位点的突变与人类和植物病原体中已知的耐药突变相符。
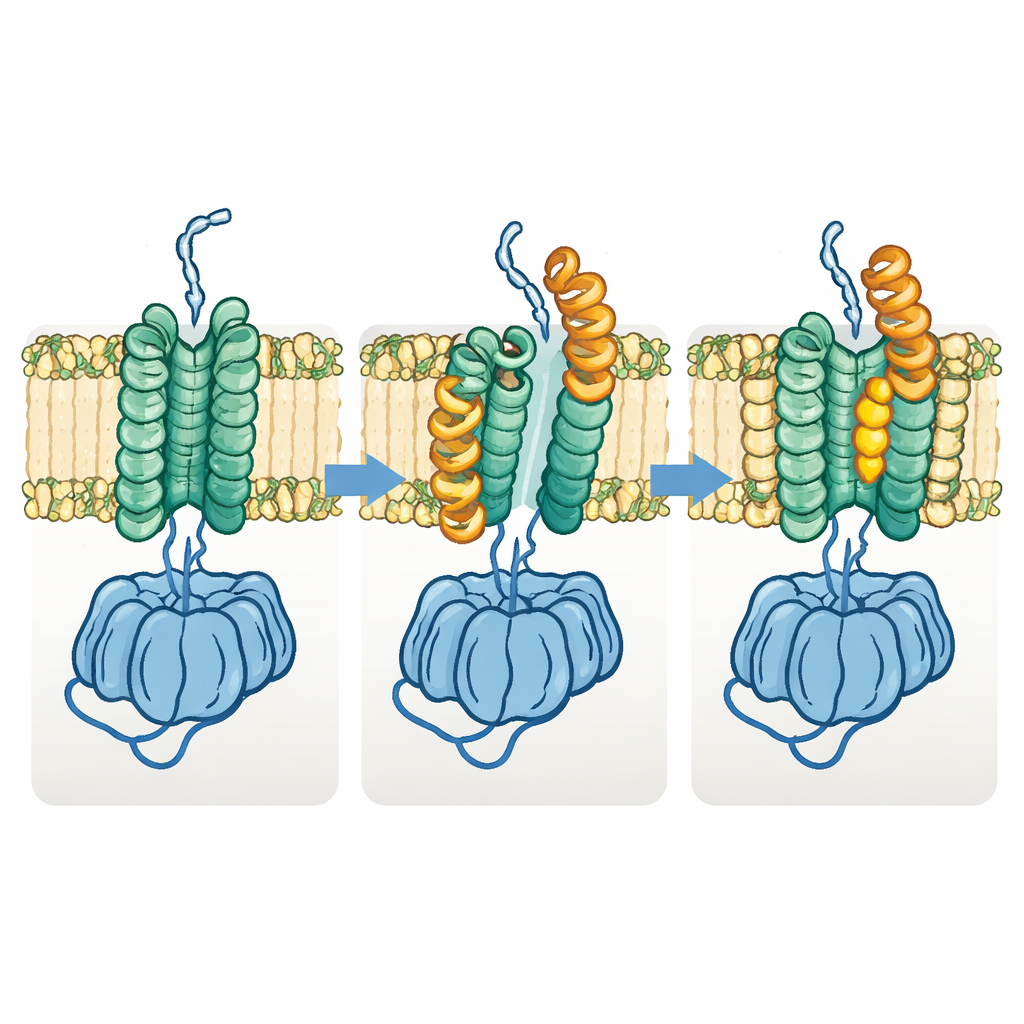
聚合物运输必需的构象转换
研究团队还发现了Fks1的另一种“开放”构象。在该状态中,膜区的一半侧向移动,关键的水平螺旋向外摆动,撬开两簇膜束之间的空间并扩大了表观的葡聚糖通道。对多种结构的比较表明,酶在正常工作过程中在基态与开放态之间循环:基态用于准备并启动聚合物形成,而开放态允许生长的链横向穿过膜向外移动。当作者设计二硫键以期将酶永久锁定在任一状态时,两个变体的活性均大幅丧失,支持了这种构象转换对功能至关重要的观点。
对未来抗真菌药物的启示
该研究表明,enfumafungin及其相关药物并非通过阻断催化口袋起作用,而是通过重塑局部膜环境并将葡聚糖合酶锁定在基态来发挥作用,揭示了一种非常规的药物作用模式。研究还证明Fks1与Fks2具有几乎相同的结构和药物响应,这解释了在应对耐药问题时两者都必须被考虑。更广泛地说,这项工作强调了小分子如何通过结合浅表位点并招募脂质来控制“难以成药”的膜蛋白,为设计下一代即便在真菌进化下仍然有效的抗真菌药物提供了概念蓝图。
引用: You, ZL., Sun, L., Wang, LX. et al. Inhibition mechanism of the fungal β−1,3-glucan synthases by triterpenoid antifungal drugs. Nat Commun 17, 2347 (2026). https://doi.org/10.1038/s41467-026-69114-8
关键词: 抗真菌药物, 真菌细胞壁, 葡聚糖合酶, 药物耐药性, 冷冻电子显微镜