Clear Sky Science · zh
结核分枝杆菌转录起始时停顿的结构基础
病菌的基因开关如何被卡住
引起结核病的细菌结核分枝杆菌必须不断开关基因,以在人体的严酷环境中生存。本文所述工作窥见了这种基因控制的最早步骤之一,捕捉到了细胞刚开始将 DNA 转录为 RNA 时出现的一种短暂“停顿”。理解这一停顿有助于解释微生物如何决定是完成基因的开启还是放弃尝试——并可能最终揭示新的抗生素靶点。
从 DNA 开始的信息传递
在细菌中,一个巨大的蛋白机器称为 RNA 聚合酶沿着 DNA 移动以合成 RNA,这是生成蛋白质的第一步。启动时,它与被称为 σ 因子的辅助蛋白结合,σ 因子引导聚合酶到 DNA 上的特定起始位点并帮助打开双螺旋中的一个小“气泡”。对于结核分枝杆菌,其中一种称为 σE 的因子在细胞内膜外受应激时尤为重要。另一个因子 CarD 有助于稳定打开的 DNA 气泡。它们共同形成起始复合体,在合成出最初几段 RNA 之前,决定是继续合成长链信息还是放弃并释放短 RNA 片段。
长六到七个碱基时的隐匿停顿
先前的生化和单分子研究提示 RNA 聚合酶常在非常早期出现停顿,即新生 RNA 链仅延长到六或七个碱基时。但这些停顿极其短暂,难以直接观测,因此缺乏高分辨率结构。在这项研究中,作者使用冷冻电镜冻结并可视化了结核分枝杆菌起始机械的多种状态。他们设计了能在 RNA 长度为六或七单位时捕获复合体的 DNA–RNA 支架,并解析出三种主要状态的结构:两个“常规”起始复合体和一个独特的停顿起始复合体。
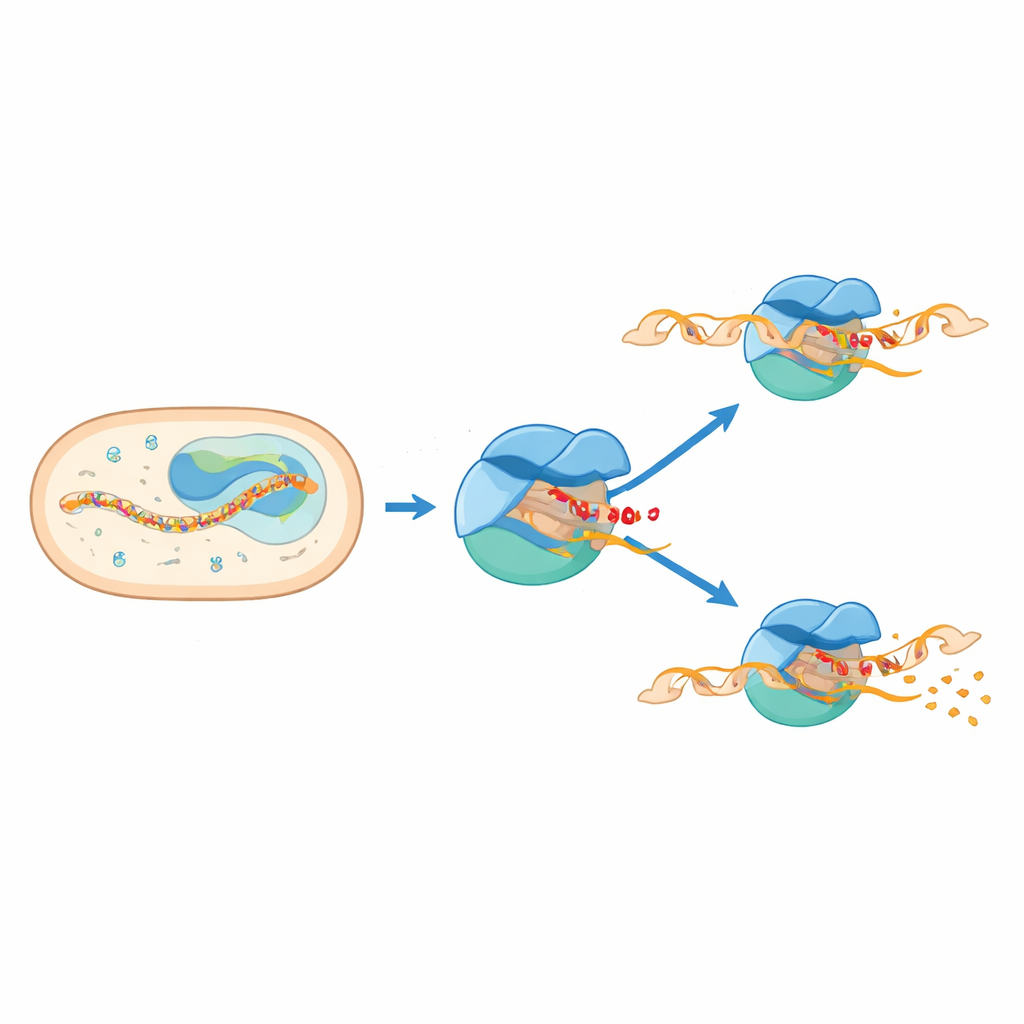
当机器的两部分发生碰撞
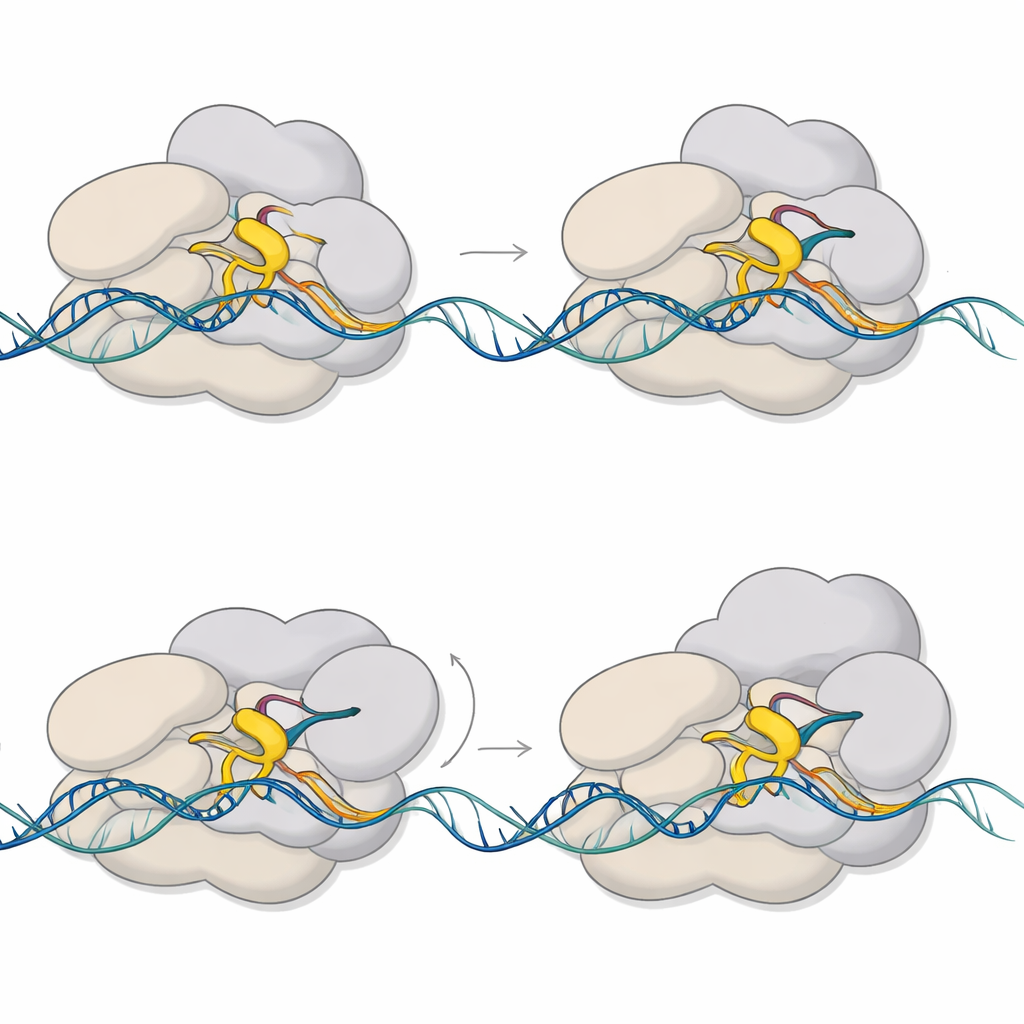
这些结构显示,停顿产生于机器的两部分试图占据同一空间。σE 的一段灵活片段,称为 3.2 区,突入生长的 RNA 必须通过的通道。当 RNA 延长到六或七个单位时,前端会与这个突出环发生碰撞。该碰撞迫使 RNA 聚合酶内的一个大型模块发生旋转,并使一个关键结构元件——桥螺旋发生畸变。与此同时,活性位点上游的 DNA 被向内拉入并部分解旋,形成“压缩”并弯曲的气泡。这些耦合运动将复合体锁定为一个停顿的、半推进状态,储存了机械应力。
变形的辅助因子稳定气泡
辅助因子 CarD 的作用比先前认为的更加多功能。在非停顿的起始复合体中,CarD 插入到气泡边缘一条 DNA 链的次槽中,帮助保持气泡打开,以便 RNA 聚合酶开始合成。在停顿复合体中,CarD 转位去拥抱相对的非模板链,与 σE 一起更紧密地夹住被压缩的气泡。生化实验显示,CarD 提高了 σE 依赖的转录并影响在六到七单位阶段积累的 RNA 数量。这些发现表明,CarD 既稳定初始的打开状态,也帮助停顿复合体避免过早塌陷。
失败与承诺之间的检查点
通过比较在部分预打开 DNA 上获得的高分辨率结构与在完全配对 DNA 上组装的低分辨率结构,作者表明相同的基本停顿构象也出现在更自然的条件下。他们提出,新生 RNA 与 σ3.2 环之间的碰撞在六到七个 RNA 单位处产生了一个能量积累的检查点。从这一待命状态,复合体可以沿两条主要路径之一前进:释放短 RNA 并重置(中止尝试),或利用储存的应力突破启动子区域并进入稳定的、长期的 RNA 产生。CarD 的重新定位以及 σ 因子对上游 DNA 握持的放松似乎引导着这一决定。
这对结核病为何重要
对非专业读者而言,核心信息是结核杆菌并非像开关灯那样简单地开启基因。相反,它在一个微小的 RNA 长度处犹豫,利用短暂的机械停顿作为在中止与承诺完全启动基因之间的决策点。这项工作以原子细节捕捉了该停顿,展示了一个小的移动环、一个旋转的核心和重塑的 DNA 气泡如何共同创造一个可控的检查点。由于 σE 和 CarD 对结核分枝杆菌应对应激至关重要,这些见解最终可能帮助研究者设计阻断该早期步骤的药物,从而削弱细菌的适应和生存能力。
引用: Zheng, L., Xu, K. Structural basis of pausing during transcription initiation in mycobacterium tuberculosis. Nat Commun 17, 2197 (2026). https://doi.org/10.1038/s41467-026-69104-w
关键词: 转录起始, RNA 聚合酶停顿, 结核分枝杆菌, σ 因子, 冷冻电子显微镜