Clear Sky Science · zh
急性腹膜炎诱导的脂肪 CD127+ ILC1 表达 PD-L1 并减轻小鼠炎症
为什么腹部脂肪能帮助对抗致命感染
当细菌从破裂的肠道泄入腹腔时,机体可能陷入一种称为败血症的危及生命的状态。本研究揭示了这一斗争中一个意想不到的盟友:潜伏在腹部脂肪中的一类特殊免疫细胞,它们在早期感染时迁入并充当抑制失控炎症的内在刹车。了解这些细胞的工作方式,可能为在不完全抑制免疫系统的前提下平息危险感染提供新的治疗思路。
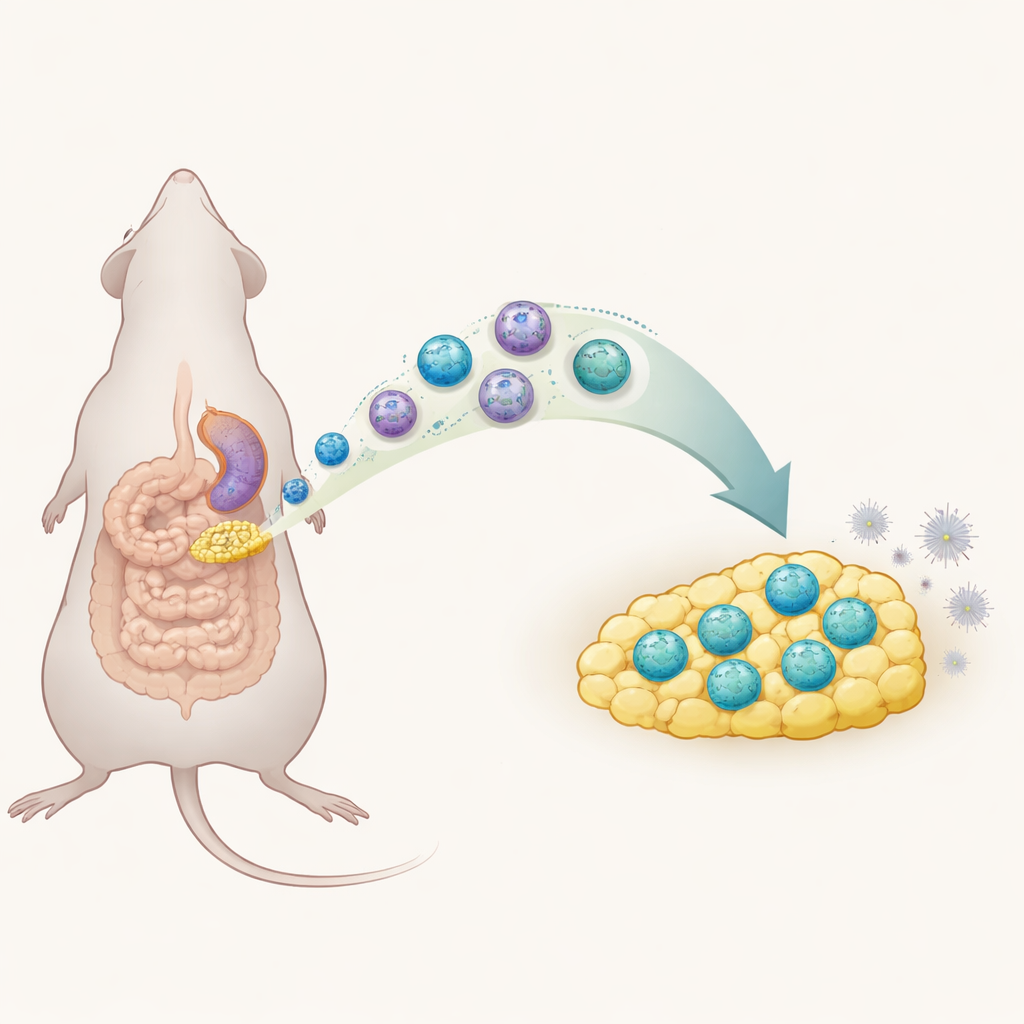
腹腔的危险泄漏
腹膜炎是指腹腔内膜发生炎症,最常见的原因是细菌从穿孔的肠道溢出。如果这场早期炎症风暴得不到控制,患者可能发展为败血症;尽管现代医疗已进步,败血症仍约每五名患者致死一人。医生可以通过手术和抗生素来处理感染,但几乎没有工具可以引导机体自身的免疫反应避免有害的过度激活。覆盖肠道的那层脂肪,被称为肠系膜脂肪组织,已知会涌向肠道损伤部位,这提示它在早期免疫反应中发挥着主动作用。
腹部脂肪中的隐秘守护者
近年来,科学家发现了“固有淋巴细胞”,这类快速反应的免疫哨兵分布于多种组织。其亚型之一——1组 ILC(ILC1)通常有助于发起强烈的炎性反应。在这项小鼠研究中,研究者使用了标准的外科腹膜炎模型来探究这些细胞在肠系膜脂肪中的行为。他们发现损伤后六小时,该脂肪组织出现炎性信号和 ILC1 的激增,而其他相关细胞类型几乎没有变化。这个时间点与动物病情高峰相吻合,提示 ILC1 与腹腔早期炎症阶段密切相关。
迁移并改变性质的细胞
深入分析时,研究团队运用先进的单细胞分型将 ILC1 群体分为亚群。在正常情况下,大多数腹部脂肪中的 ILC1 表面缺乏一种称为 CD127 的分子。然而在急性腹膜炎期间,出现并扩增了一群新的 CD127 阳性 ILC1。这些新来者产生的强效炎性信号干扰素‑γ(IFN‑γ)比其 CD127 阴性同类更少,显示出不寻常的克制性。科学家还表明,这些细胞并非只是局部分裂扩增:相反,来自脾脏的 ILC1 通过血流迁移到肠系膜脂肪,部分由化学“归巢”信号 CXCL10 及其受体 CXCR3 指引。到达脂肪后,它们改变了表面标志,获得 CD127 并采纳了这种更安静、更具调节性的表型。
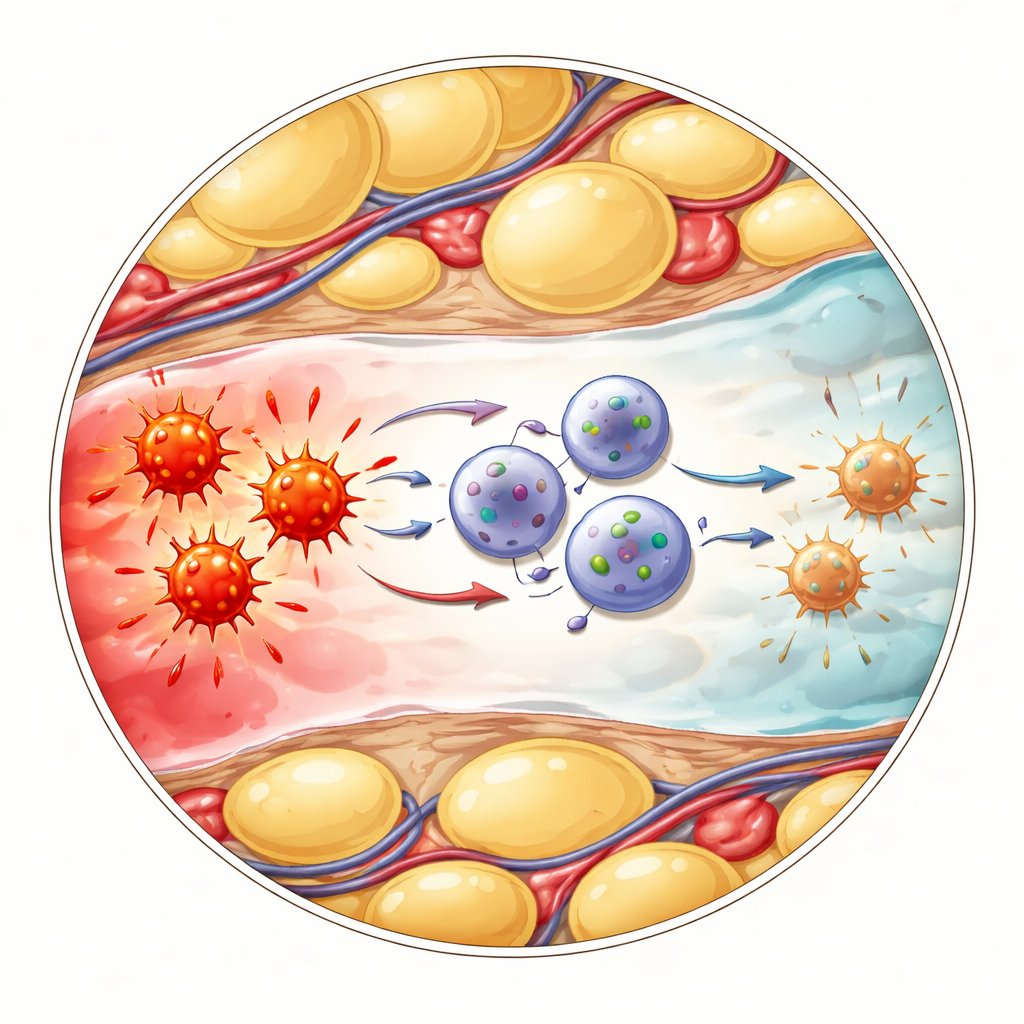
镇静细胞如何与燃烧的细胞对话
下一个问题是这些改变后的 ILC1 如何实际冷却炎症。研究者关注另一类免疫细胞——γδ T 细胞,它们对危险反应迅速,并能释放大量警报分子肿瘤坏死因子(TNF)。单细胞分析表明,CD127 阳性的 ILC1 与 γδ T 细胞通过一条已知的“制动”通路相互作用,该通路涉及表面蛋白 PD‑L1 与 PD‑1。在发炎的腹部脂肪中,新到达的 ILC1 强烈上调 PD‑L1,而附近的 γδ T 细胞则表现出高水平的 PD‑1。当团队用抗体阻断 PD‑1 时,γδ T 细胞分泌更多 TNF,证明这种接触通常会抑制其炎性输出。同样,基因工程小鼠若缺乏 ILC1 病情更重、炎性标志物更高且 γδ T 细胞产生更多 TNF——这些效应可以通过直接阻断 TNF 得到缓解。
对未来治疗的意义
综合这些发现,作者提出了一条“脾脏‑至‑腹部脂肪”轴:在细菌刚泄入腹腔后不久,ILC1 离开脾脏,归巢至肠系膜脂肪,并在那里转变为富含 CD127 和 PD‑L1 的细胞,这些细胞抑制 γδ T 细胞产生 TNF。与其助长炎火,这些特化的 ILC1 更像局部和平守护者,防止炎症过度扩散,并可能帮助阻止腹膜炎进展为致命的败血症。从长远看,增强或模拟这一腹部脂肪中调节回路的药物,可能为治疗严重感染提供一种新途径——调整免疫反应,使其既足够强大以对抗病原体,又不过度强大而危及患者。
引用: Nagata, R., Akama, Y., Goncalves, P. et al. Acute peritonitis-induced adipose CD127+ ILC1s express PD-L1 and ameliorate inflammation in mice. Nat Commun 17, 2391 (2026). https://doi.org/10.1038/s41467-026-69100-0
关键词: 腹膜炎, 固有淋巴细胞, 肠系膜脂肪组织, 免疫调节, 败血症