Clear Sky Science · zh
将核受体重新用于配体响应性液态凝聚体形成与基因调控
把激素变成按需的细胞开关
我们的细胞持续监听诸如激素和维生素之类的信号并将其转化为行动,例如开启或关闭基因。该研究展示了科学家如何利用这种天然“语言”构建合成“开关”,这些开关对真实的体内信号作出响应,甚至在细胞内形成微小的液滴以大幅增强基因活性。受激素控制的此类开关未来可能用于开发更智能的基因治疗、精准生物传感器或与患者自身生理紧密耦合的“活性药物”。
利用细胞自身的信号识别器
激素和相关分子由一类称为核受体的蛋白读取,这些蛋白通常驻留在细胞中并在甲状腺激素、维生素D、雌激素和皮质醇等信号作用下控制基因。每个受体都有一个结合其特定激素的口袋,以及在激素存在时与辅助蛋白(称为共同激活因子)结合的表面。研究人员没有设计完全人造的部件,而是重复使用这些天然受体和一小段人源共同激活因子蛋白(短的TIF2肽)作为模块化构件。这样的选择使他们的合成开关使用与机体相同的生化语言,更容易接入已存在的信号通路。
构建化学的开/关开关
研究团队首先证明激素结合可以按需将两个工程化蛋白片段拉到一起。他们将若干核受体的配体结合域融合到分裂报告酶的一半上,将TIF2肽融合到另一半。在人细胞中,加入匹配的激素会促使两半重聚,恢复报告酶的发光;而去除或阻断激素则会打破连接。通过将受体与其激活性药物(激动剂)和阻断性药物(拮抗剂)配对,他们建立了可由一种化合物打开、由另一种关闭的双输入开关,有时可在数分钟内重复切换。他们还用这种策略将酶定向移动到细胞内特定位置,按需改变局部化学环境。
通过倍增接触控制基因
为将这些开关转化为基因控制器,研究者将它们连接到基于CRISPR的DNA结合平台。一个“失活”的Cas9蛋白被引导到选定的DNA位点,而核受体携带强效的基因激活结构域。当加入激素时,受体会与附着在dCas9上的TIF2片段结合,将激活子带到目标基因。单个TIF2片段仅产生适度效应,但串联多个拷贝会形成多价的着陆平台,能够同时招募大量受体。这显著增强了基因激活——可达基础水平的数百倍——且响应在与体内相似的激素浓度范围内保持敏感。拮抗剂药物可以明显降低这种活性,显示出可逆且精确的控制。
创造可加速表达的液滴
随着TIF2拷贝数的增加,团队注意到性能出现陡峭阈值,这提示蛋白可能在凝聚成液滴。许多天然基因调控因子形成类似液体的“凝聚体”,将转录所需的机器浓缩在一起。研究者有意设计了用卷曲-线圈肽将多个TIF2基序捆绑在一起的支架,以鼓励在激素存在时多个受体聚集到同一位置。在活细胞中,这会产生明亮的球形液滴,表现出液体特性:会融合、在光漂白后恢复,并能被破坏弱蛋白相互作用的化学物质溶解。重要的是,只有在合适的多价和激素条件下才会出现液滴,且拮抗剂能够使其消失,证明液滴形成具有化学可调性。
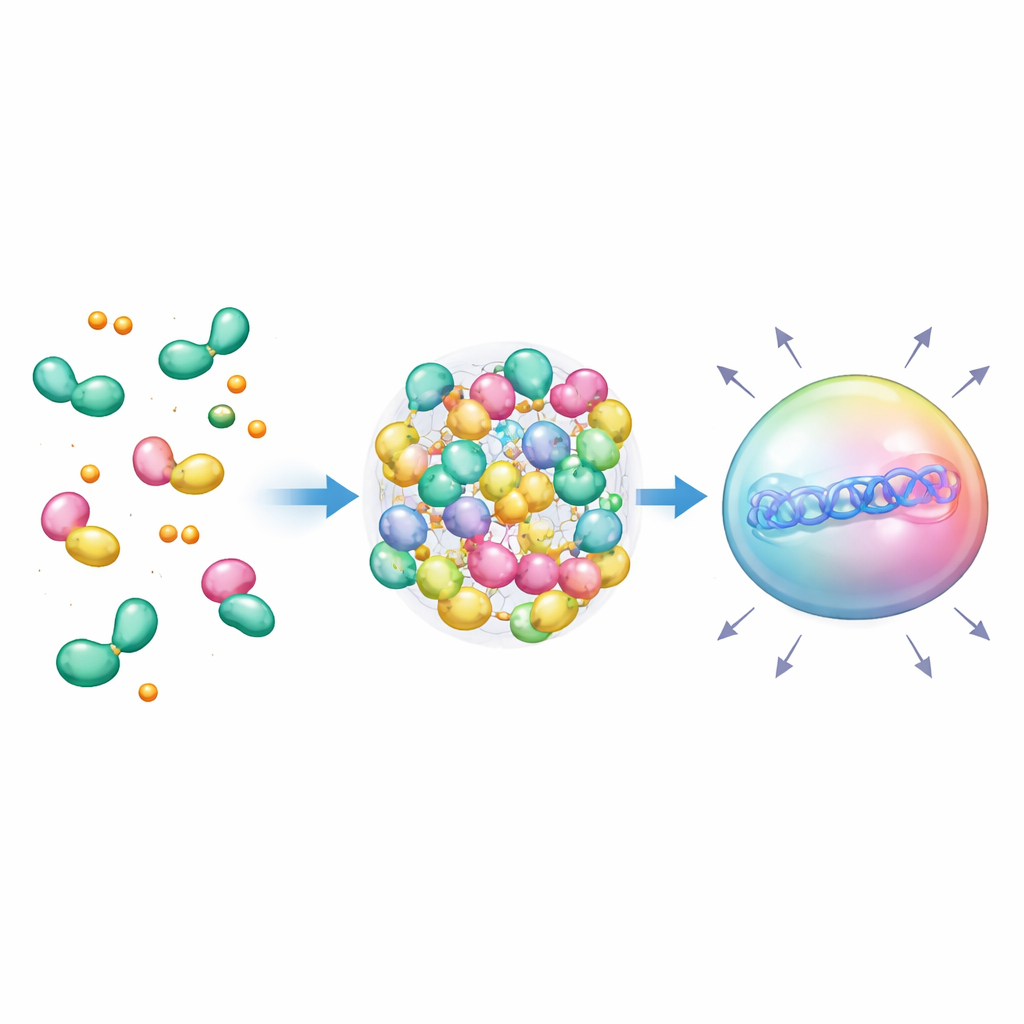
从设计液滴到未来疗法
通过将这些受激素控制的液滴与靶向DNA的CRISPR工具融合,作者创建了直接位于特定基因上方并能大幅放大其活性的核内凝聚体——即便靶点只有单个位点。由于这些组件源自人体并对皮质醇和雌激素等熟悉信号有响应,这些系统最终可能被接入到能自动根据患者激素水平做出反应的治疗电路中。尽管需要谨慎测试以避免干扰体内自身受体,该工作阐明了一个强有力的概念:重复使用天然的激素识别器和液态凝聚体,作为可编程开关来感知内部化学状态并驱动定制的基因响应。
引用: Rihtar, E., Fink, T., Ivanovski, F. et al. Repurposing nuclear receptors for ligand-responsive liquid condensate formation and gene regulation. Nat Commun 17, 2218 (2026). https://doi.org/10.1038/s41467-026-69099-4
关键词: 合成生物学, 核受体, 激素信号, 基因调控, 相分离