Clear Sky Science · zh
结肠空间单细胞蛋白组学与小鼠模型将线粒体功能障碍与克罗恩病中二聚体IgA分泌性浆细胞缺乏联系起来
为什么肠道抗体在克罗恩病中很重要
克罗恩病最为人知的是肠道炎症的剧烈复发和疼痛,但在症状爆发之前很久,免疫系统如何保护肠道可能已经发生了细微变化。本研究提出了一个简单却重要的问题:处于缓解期的克罗恩病患者,是否仍然产生能够将肠道微生物和平地控制在一旁的那类正确抗体?通过结合病人样本、高分辨率组织分型、代谢分析和小鼠模型,作者揭示了肠道抗体防线中的一个隐性弱点,该弱点与细胞能量产生有关。
不够充分的保护涂层
我们的肠道依赖一种特殊的抗体,称为分泌型IgA,它被释放到覆盖肠道的黏液中。IgA,尤其是其叫作二聚体IgA的“双体”形式,会包裹细菌和其他微生物,帮助将它们保持在表面而不是深入组织中。在这项工作中,研究者检查了来自处于缓解期的克罗恩病患者与非炎症对照者的结肠活检、血液和粪便。在结肠组织内,克罗恩患者实际上具有更多的B细胞和产抗体细胞,以及更高水平的与IgA相关的基因和蛋白。然而,当团队测量粪便中的IgA时,发现的情况与直觉相反:肠腔内的分泌型IgA显著减少。
半路滞留:未充分成熟的产抗体细胞
分泌IgA的细胞——浆细胞——通常从活跃的短寿命前体经过分明阶段成熟为能大量分泌二聚体IgA的长寿能手。利用空间单细胞蛋白组学(在完整组织内对单个细胞的多种蛋白进行定位绘制),作者能够区分结肠中未成熟与完全成熟的浆细胞亚群。在克罗恩患者中,早期浆母细胞和未成熟浆细胞扩增,而最成熟的浆细胞减少。生化分析证实,克罗恩结肠中二聚体与单体IgA的比率较低,且每个产抗体细胞平均分泌的二聚体IgA更少。当团队从结肠中分离出已发生类别转换的记忆B细胞并在培养中促使其成为浆细胞时,来自克罗恩患者的细胞无法上调关键成熟标志物且产生的总IgA和二聚体IgA较少,尽管IgG的产生总体上保持正常。这提示存在一个特异于IgA分泌浆细胞成熟程序的内在阻滞。
能量工厂承受压力
为了解驱动这一阻滞的原因,研究者转向细胞代谢。他们发现克罗恩组织中的浆细胞表达更高水平的CD38,这是一种位于细胞表面的酶,会消耗NAD+,而NAD+是线粒体能量产生的核心燃料。参与线粒体氧化磷酸化——细胞将营养物质转换为ATP的主要方式——的基因在克罗恩患者的结肠组织中普遍下调,血浆代谢物模式也与从高效线粒体呼吸转向其他代谢途径一致。在离体实验中,来源于克罗恩患者的浆细胞摄取很少葡萄糖、释放较少乳酸,并显示线粒体能量相关基因表达降低,表明其代谢处于“静止”或衰弱状态。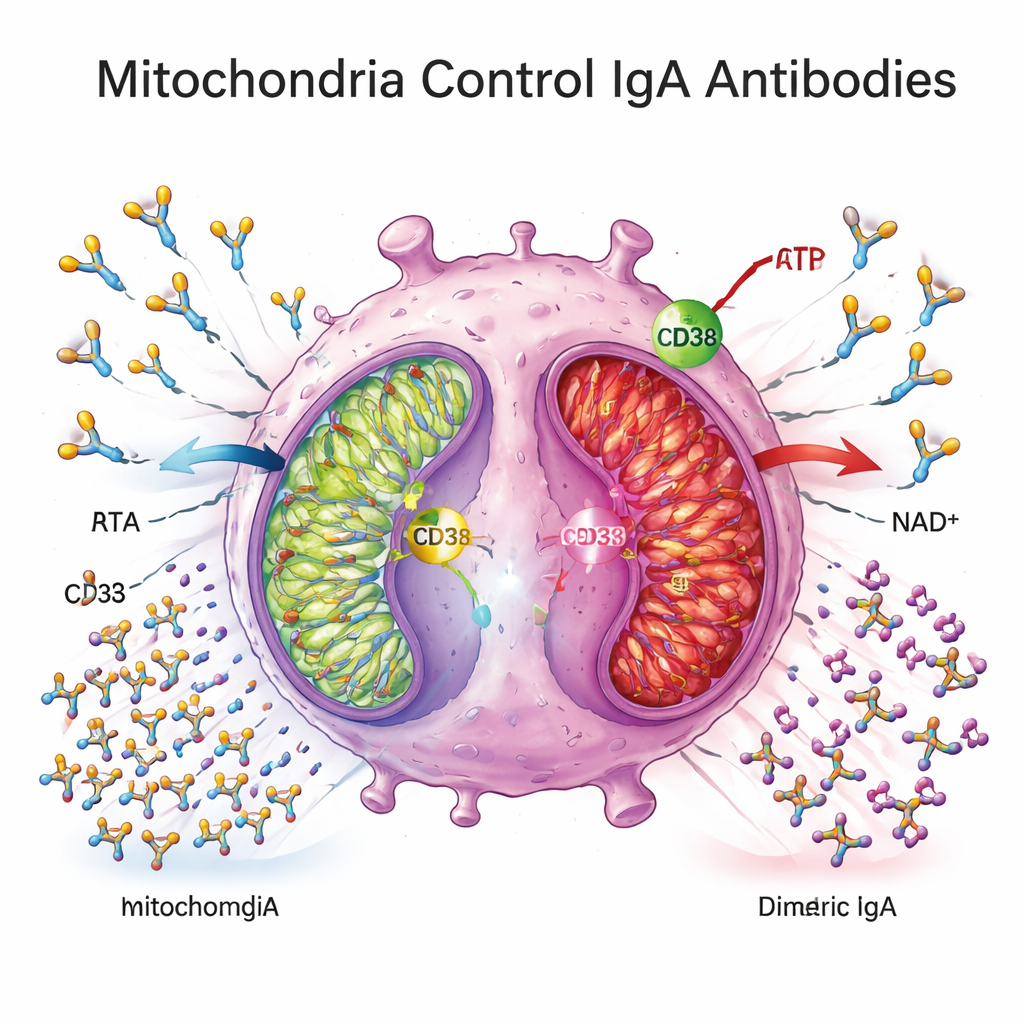
来自小鼠模型和饮食的线索
小鼠模型提供了进一步支持。携带会损害产生ATP的酶复合体V的特定线粒体突变的小鼠,在肠相关淋巴组织中具有更少的成熟浆细胞、结肠中浆细胞标志物表达降低,以及结肠组织中单体和二聚体IgA水平均降低。相反,健康小鼠喂食一种无葡萄糖、高蛋白的饮食(该饮食能增强结肠的线粒体活性)则产生更多的IgA分泌细胞并且粪便IgA升高。这些互补实验将线粒体功能直接与浆细胞成熟及维持肠道强健IgA屏障的能力联系起来。
对克罗恩病患者意味着什么
综合来看,这项研究勾画出这样一幅图景:即使在临床缓解期间,克罗恩病也与结肠中B系细胞未成熟群体过多以及能量需求高的、完全成熟的分泌二聚体IgA的浆细胞短缺相关。肠道表面看似平静,但其抗体屏障更薄、效能更弱。通过将这一缺陷与线粒体功能障碍联系起来——这可能部分由升高的CD38活性驱动——这项工作表明,旨在恢复细胞能量代谢或微调CD38信号的治疗,可能有助于重建黏膜IgA屏障。对于患者而言,这提示未来的治疗不仅可能在炎症出现时加以抑制,还可能通过强化肠道一线抗体防御来预防复发的发生。
引用: Raschdorf, A., de Almeida, L.N., Solbach, P. et al. Colonic spatial single-cell proteomics and murine models link mitochondrial dysfunction to dimeric IgA-secreting plasma cell deficiency in Crohn’s disease. Nat Commun 17, 1590 (2026). https://doi.org/10.1038/s41467-026-69069-w
关键词: 克罗恩病, 肠道抗体, IgA, 线粒体, 肠道免疫