Clear Sky Science · zh
紫杉醇驱动 TREM2+ 巨噬细胞扩增,导致其疗效逊于白蛋白结合型紫杉醇(Nab‑paclitaxel)
本研究为何重要
许多乳腺癌患者接受一种称为紫杉类的化疗药物,最常见的是紫杉醇或其更现代的配方——与微小白蛋白颗粒结合的白蛋白结合型紫杉醇(nab‑paclitaxel)。临床上早已怀疑新版药物常更为有效,但原因尚不清楚。本研究结合患者资料与动物实验,揭示标准紫杉醇可能通过重塑机体免疫细胞无意中助长癌细胞向肺转移,并指出了可能阻断这一有害副作用的策略。
两种相近药物,却有不同结局
研究者首先比较了现实世界中紫杉醇与白蛋白结合型紫杉醇在数千名乳腺癌患者中的表现。通过汇总来自17项包含6,486名患者的临床研究,他们发现 nab‑paclitaxel 在术前使肿瘤缩小和在乳房及近旁淋巴结中完全缓解的比率更高。这一优势在既往治疗失败后使用的患者中尤为明显。然而,两种药物的给药剂量相近,且设计初衷都是以类似机制攻击分裂的癌细胞,这提示二者之间的差异并非仅源自对肿瘤的直接杀伤。
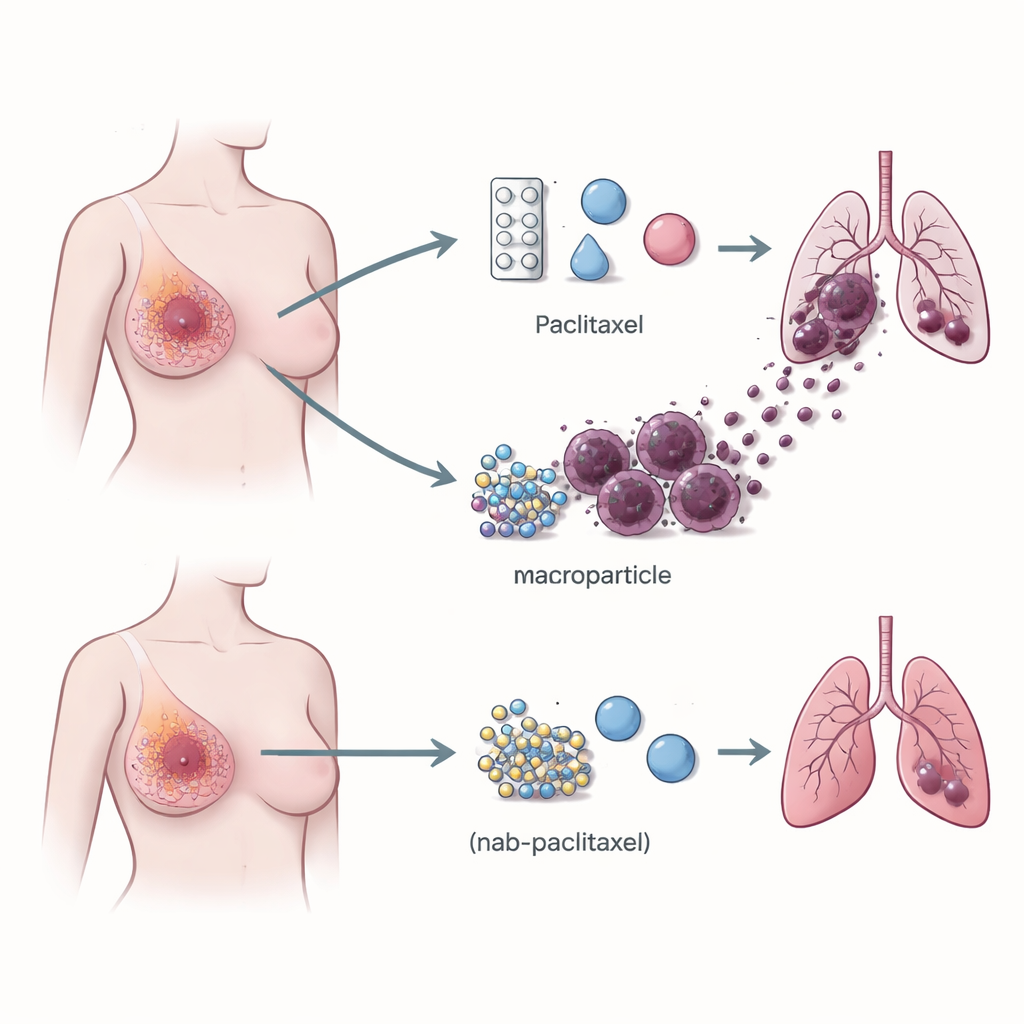
帮助癌细胞“旅行”的免疫细胞
注意力转向肿瘤的免疫环境——即可以抗癌、但常常反而助长癌症增长的白细胞混合群。研究团队使用单细胞 RNA 测序技术(对数千个细胞的基因活性逐一读取),比较了接受紫杉醇与 nab‑paclitaxel 处理的肿瘤样本。他们发现接受紫杉醇治疗的肿瘤中携带一种名为 TREM2 受体的巨噬细胞明显增多。这类 TREM2 阳性巨噬细胞在肿瘤边缘富集,并且在随后发生肺转移的患者中远多于病情未扩散的患者。该模式在更大规模的患者群体和小鼠模型中均得到验证,建立了该巨噬细胞类型与转移风险之间的强关联。
肿瘤缩小却助长转移的情形
在带有乳腺肿瘤的小鼠中,紫杉醇达到了其预期效果:减缓或缩小原发肿瘤。但与此同时,它增加了肺部癌性沉积的数量,并在肿瘤与血液中促进了 TREM2 阳性巨噬细胞的扩增。相比之下,nab‑paclitaxel 在同样有效缩小原发肿瘤的同时,并未促发肺转移或扩增这些巨噬细胞。当小鼠中 TREM2 基因被敲除,或用反义寡核苷酸(能沉默特定基因的短 DNA 片段)下调 TREM2 时,紫杉醇仍能缩小原发肿瘤,但其促进肺转移的能力大为减弱。这表明携带 TREM2 的巨噬细胞并非旁观者;它们是紫杉醇驱动转移的必要合作者。
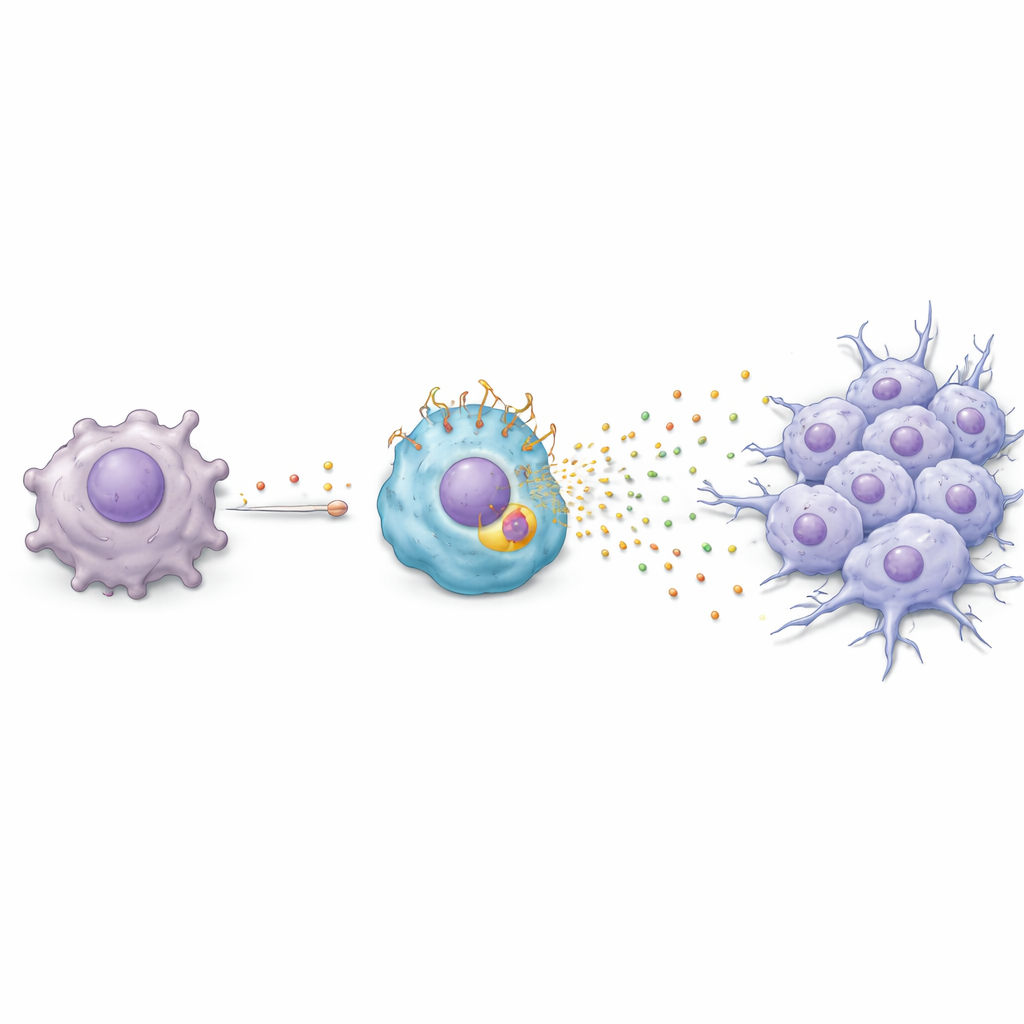
从肿瘤到免疫细胞的化学连锁反应
团队进一步探究紫杉醇如何促使巨噬细胞转变为这种有害的 TREM2 富集状态。他们发现了一条连锁反应:紫杉醇促使癌细胞激活一种应激反应基因 ATF3,ATF3 进而提升生长因子 FGF2 的产生。癌细胞将 FGF2 释放到周围环境,作用于邻近的巨噬细胞。在巨噬细胞中,FGF2 激活另一调控因子 EGR1,从而提高 TREM2 水平。一旦 TREM2 升高,巨噬细胞开始分泌一组蛋白质——包括 Serpin E1、HGF、CCL3 和 CXCL2——这些因子推动癌细胞进入更具移动性和侵袭性的上皮‑间质转化(epithelial‑mesenchymal transition)状态。在体外培养和小鼠体内,这种化学串话使肿瘤细胞更容易迁移和侵袭,这是转移过程中的关键步骤。
把双刃剑变成更安全的工具
从通俗角度来看,关键讯息是:紫杉醇像一把双刃剑——在攻击肿瘤的同时,也指挥某些免疫细胞帮助癌症转移到远处器官。而 nab‑paclitaxel 似乎避免触发这一特定的免疫失控。令人鼓舞的是,阻断 TREM2——或阻断 FGF2–EGR1–TREM2 信号链的部分环节——可以在动物模型中将紫杉醇的肿瘤缩小效应与其促进转移的风险分离开来。如果类似策略在人体中证明既安全又有效,临床医生可能得以继续使用这一熟悉且广泛可及的化疗药物,同时抑制其促转移的倾向,从而改善患者的长期结局。
引用: Xing, Y., Zhong, R., Li, Q. et al. Paclitaxel drives TREM2+ macrophage expansion underlying its inferior therapeutic efficacy compared to Nab-paclitaxel. Nat Commun 17, 2272 (2026). https://doi.org/10.1038/s41467-026-69060-5
关键词: 乳腺癌, 紫杉醇, 肿瘤微环境, 巨噬细胞, 转移