Clear Sky Science · zh
体内双重 RNA-测序揭示细胞外病原体破坏上皮屏障的关键效应因子
某些病原如何悄然越过我们的细胞围栏
我们的器官表面由紧密排列的细胞构成,像墙一样将血液、微生物和毒素限制在适当位置。然而某些病原仍能从这些细胞之间潜入并在体内扩散。本研究生动揭示了致钩端螺旋体病(一种全球性严重疾病)细菌如何悄无声息地到达肝脏和肾脏等器官,并利用一种涉及细胞内钙的巧妙手段撬开这些保护性屏障。
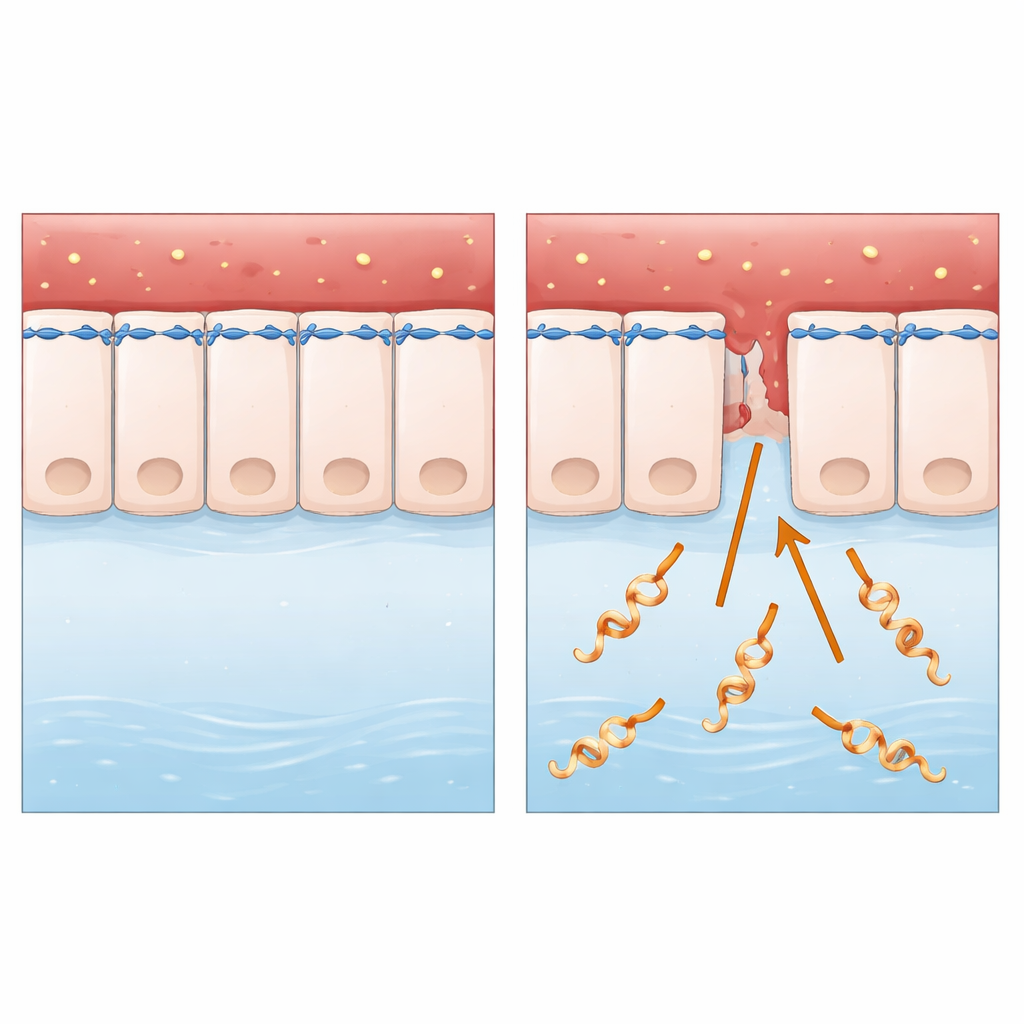
动物与人体组织的隐匿入侵者
研究聚焦于Leptospira interrogans,一种螺旋形细菌,主要通过被污染的水或土壤从动物传播到人。它通过皮肤细小破损或黏膜进入后,经血流传播,可引发严重疾病,包括肝肾衰竭和内出血。与许多被广泛研究的微生物不同,Leptospira为细胞外生存,且缺乏科学家通常寻找的一些经典“分子武器”。这使其成为一个理想的案例,用以探问一个基本问题:表面上看似简单的自由生存细菌如何如此高效地穿过完整的细胞层?
同时观测宿主与病原基因的动态对话
为了在活体动物中捕捉感染过程,研究团队在仓鼠(一种急性钩端螺旋体病模型)中使用了双重 RNA 测序。该方法可以同时读取宿主和病原体中被开启或关闭的基因。科学家感染仓鼠,并在感染后一天和三天采集肝脏与肾脏组织。早期尽管细菌数量很高,动物细胞的基因活性几乎未见变化,表明Leptospira最初可能潜入了免疫系统的视线之外。然而到第三天,两器官均表现出强烈反应,尤以肝脏为甚:与炎症、细胞间连接及细胞内支架相关的基因都发生显著改变,指向组织屏障的主动重塑。
从外部撬开细胞“拉链”
细胞层由紧密连接和黏附连接封闭,这些连接将相邻细胞连在一起并固定到一圈肌动蛋白-肌球蛋白(actin–myosin)上,正是这对蛋白在肌肉收缩中发挥作用。感染Leptospira的人类上皮细胞显微镜观察显示细胞形态改变、细胞间出现缝隙,关键连接蛋白变弱或错位。重要的是,细胞并未死亡,意味着屏障是被逐步拆解而非直接破坏。研究者也观察到细胞内折叠蛋白的压力迹象,但阻断这种应激并不能恢复连接,表明另有他因。
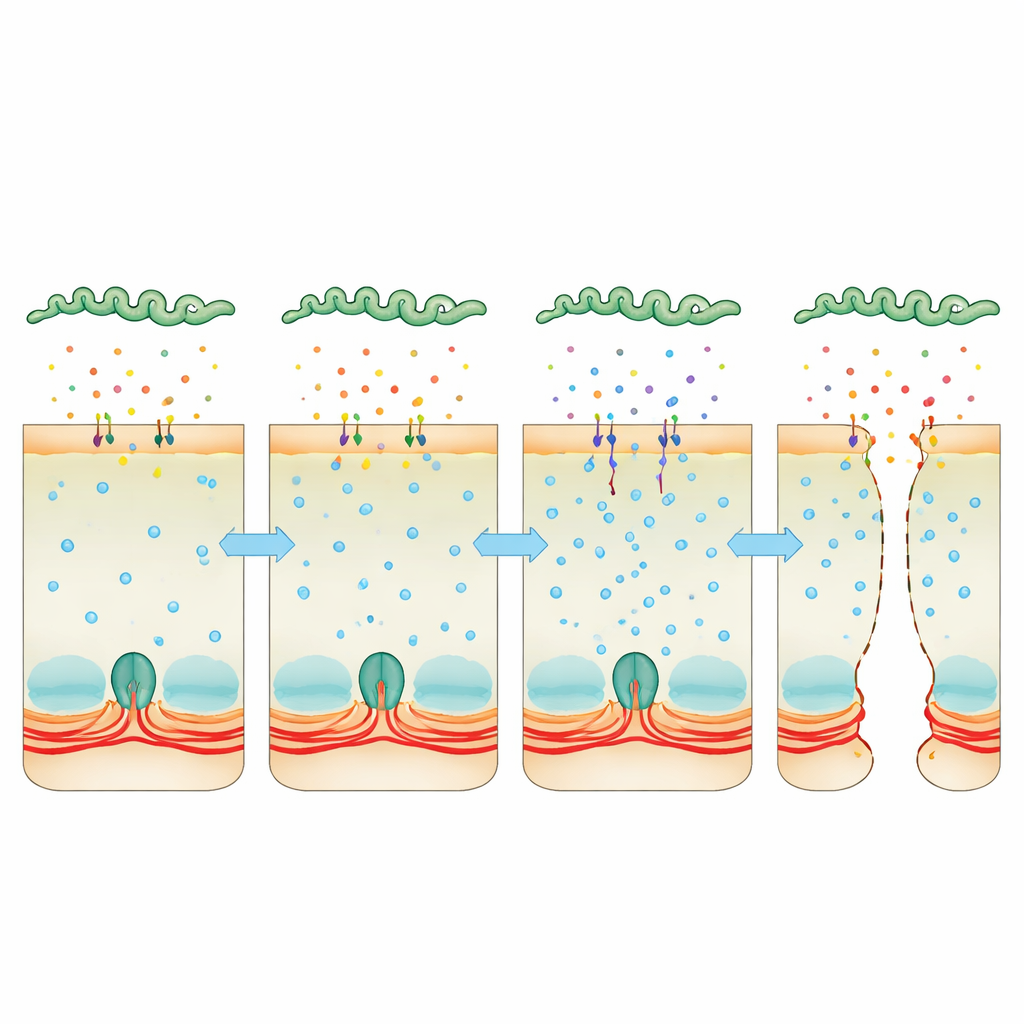
将钙作为隐蔽的撬棍劫持
注意力转向钙——一种普遍存在于细胞内的信号分子,可收紧或放松肌动蛋白-肌球蛋白环。被感染的细胞中钙积累增多,这与肌球蛋白轻链激酶(myosin light chain kinase)活性升高有关,该酶使收缩环对连接产生牵拉。团队使用能清除钙的化合物,或抑制钙调蛋白或该激酶的药物时,细胞层更能保持完整,细菌穿过的难度增加。与此同时,对细菌 RNA 的深度测序显示,在宿主体内,Leptospira强烈上调两种类似毒素的“毒力修饰(Virulence‑Modifying)”蛋白的产生。这些蛋白被分泌到细胞外,能附着并进入宿主细胞。当细菌缺失其中一种或两种蛋白时,它们穿透细胞层或造成致命疾病的能力明显下降,且其分泌的培养上清不再有效地提升钙水平或拆解连接。
对疾病与未来防护的意义
综合来看,结果描绘了一个清晰的图景。Leptospira几乎不被察觉地进入机体后,开始分泌类似毒素的毒力修饰蛋白。这些蛋白结合上皮细胞并扰乱细胞内钙平衡,进而激活一条牵拉细胞间“拉链”的收缩通路。随着紧密连接和黏附连接松弛,显微级的缝隙出现,允许细菌穿过细胞间隙、定植器官并诱发严重疾病。通过明确这一由钙驱动的机制及其背后的细菌蛋白,研究为新策略铺路——例如阻断这些蛋白或其信号通路——以强化我们的细胞围栏,限制钩端螺旋体病及可能利用类似策略的其他感染的扩散。
引用: Giraud-Gatineau, A., Haustant, G., Monot, M. et al. In vivo dual RNA-Seq uncovers key effectors of epithelial barrier disruption by an extracellular pathogen. Nat Commun 17, 2274 (2026). https://doi.org/10.1038/s41467-026-69033-8
关键词: 钩端螺旋体病, 上皮屏障, 钙信号, 细菌毒素, 宿主–病原体相互作用