Clear Sky Science · zh
核心-壳层脂质纳米粒的可设计内部结构促进高效的mRNA内体释放
这种新递送技巧为什么重要
从 COVID-19 疫苗到实验性癌症疗法,许多最令人振奋的新药都是由信使 RNA(mRNA)构建的。但有一个顽固的问题:这些脆弱的链进入细胞后,大多数都会被困在称为内体的小囊中并被破坏。这项研究引入了一种对携带 mRNA 的微小脂质泡(即脂质纳米粒)进行巧妙重新设计的方法。通过围绕固体金核重组其内部结构,研究者显著提高了有多少 mRNA 能够逃逸至细胞的工作空间,从而实际合成有用蛋白质。
给微小信使更合理的体式
目前的 mRNA 疫苗和疗法大多依赖由多种脂质组成的柔软、团块状颗粒包裹 mRNA。理论上,这些颗粒中的“可离子化”脂质在内体的酸性环境下应带正电并撕裂内体膜以释放 mRNA。但实际上,mRNA 的负电荷会抵消大部分这种作用,因此只有约 2% 的传递 mRNA 能到达细胞的蛋白合成机械。作者提出了一个简单但强有力的问题:与其仅改变脂质的化学性质,不如重新设计颗粒的内部结构,控制 mRNA 与脂质彼此相对的位置,效果如何?
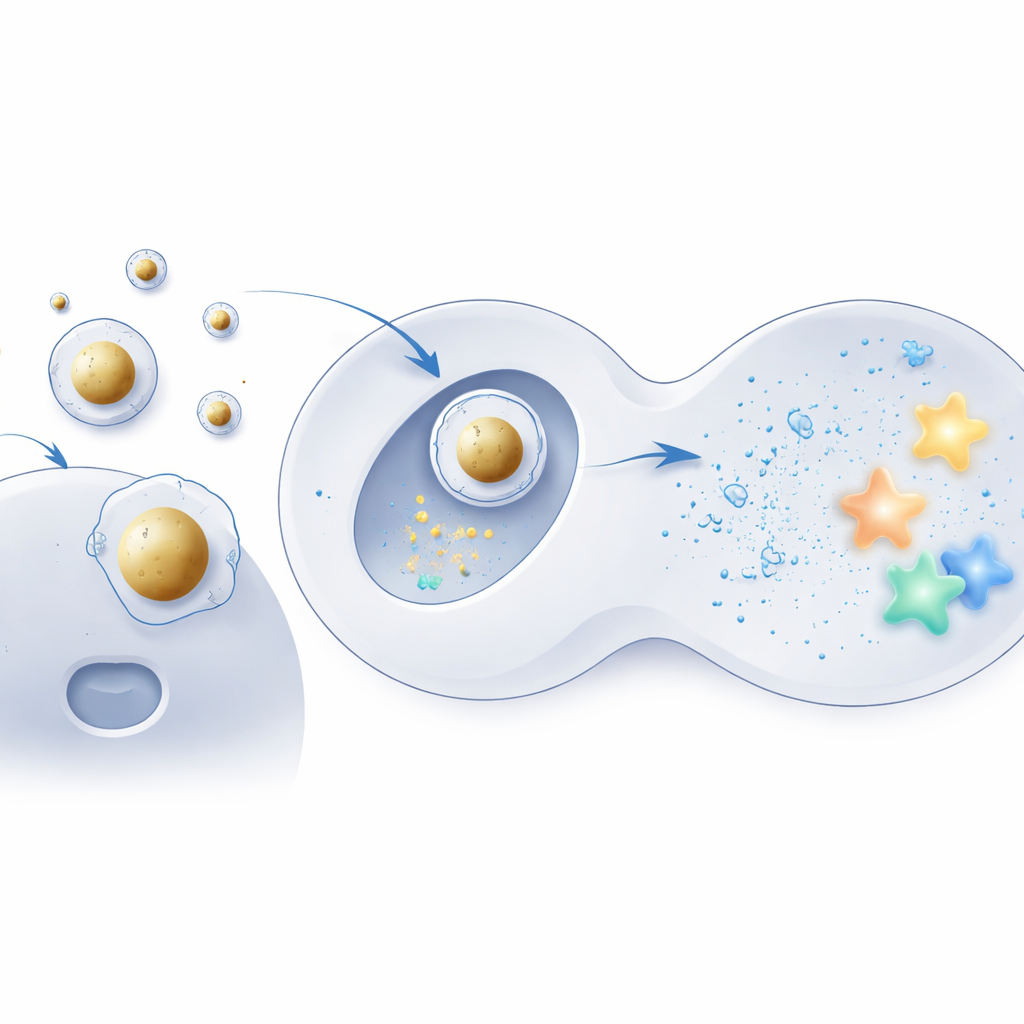
构建以金为中心的递送壳
为了检验这一想法,团队使用微小金球作为刚性核心,并用常规配方中使用的可离子化脂质对其进行包覆。带负电的 mRNA 首先被浓缩于这些核心上,随后将组装体用熟悉的助剂脂质和稳定分子混合物包裹,形成有序的核-壳结构。电子显微镜和计算机模拟显示这些“Au‑LNPs”高度均一、热力学稳定,并能在类体液环境中保持形态。更重要的是,它们的总体脂质成分与标准颗粒相同,将变化限定为内部结构而非成分,从而把关键改进归因于结构重排。
重新排列的内部如何提升逃逸
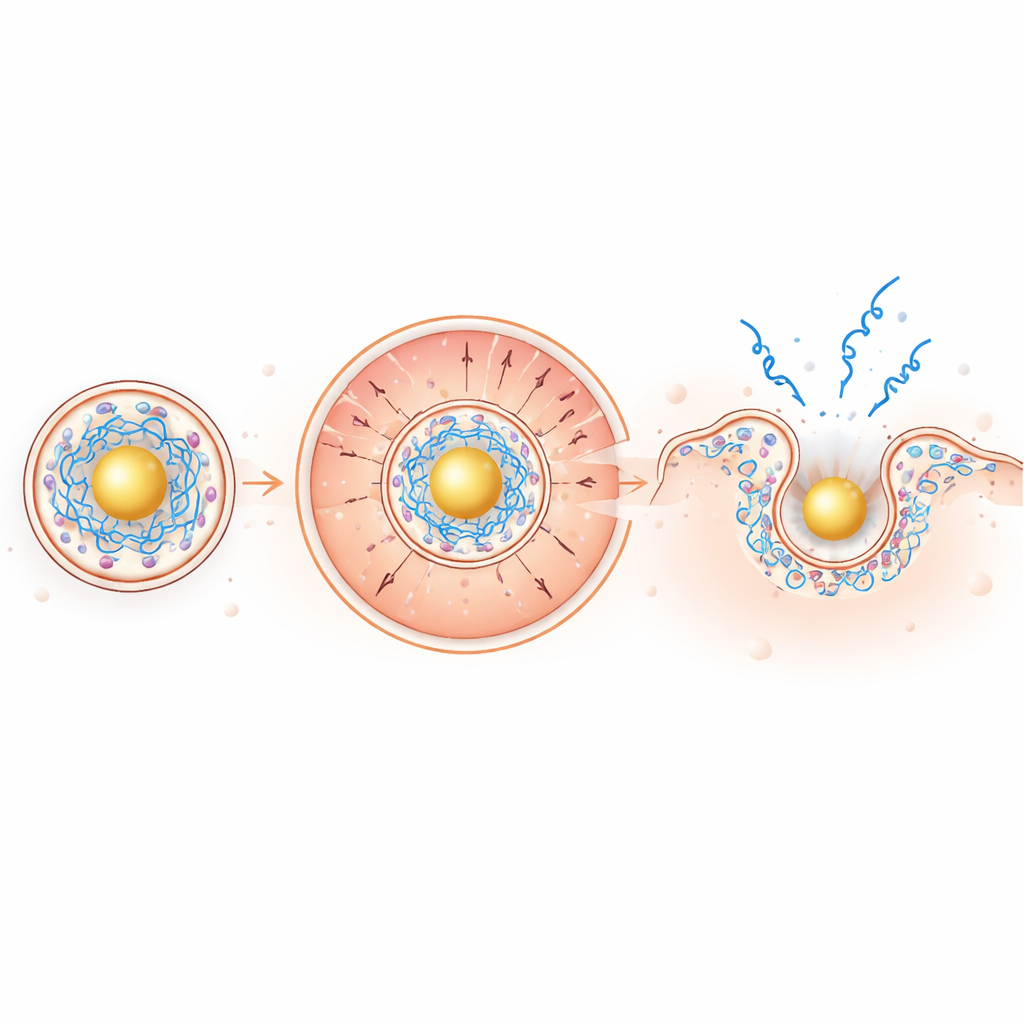
在微酸性的内体环境中,以金为核心的结构变得强烈带正电,将带负电的 mRNA 拉向内部,同时将带正电的可离子化脂质推向外侧靠近内体膜。由电荷驱动的这种分离将破膜脂质准确集中到所需位置。在模型膜测试和红细胞实验中,新型颗粒在低 pH 下更能有效刺穿膜,而在中性 pH 下保持低活性,这是一项理想的安全特性。在活细胞中,对荧光标记 mRNA 的成像显示,与传统颗粒相比,内体逃逸约增加一倍,且 mRNA 在细胞质中的传播距离惊人地约增加了 100 倍。
从培养皿到小鼠:更强的信号与更佳的保护
这些物理优势转化为实际的生物学收益。在多种细胞类型中,金核颗粒驱动的报告蛋白产量远高于标准配方,尤其在低剂量下更为明显。在小鼠中,肌肉或静脉注射后,它们将 mRNA 指导的蛋白产量提高了约五到七倍,同时并未改变颗粒在体内的分布偏好。在用于传递 SARS‑CoV‑2 刺突蛋白 mRNA 疫苗时,重新设计的颗粒在首针后大致使抗体水平翻倍,并在加强针后进一步提高,同时产生更强的病毒中和抗体。在具有挑战性的三阴性乳腺癌模型中,载于新型颗粒的 mRNA 癌症疫苗更有效地缩小肿瘤、降低肿瘤活性信号,并显著延长了生存期。
安全性与通向未来药物的路径
尽管核心使用了金属,但这些颗粒在小鼠中表现出良好的耐受性。体重、炎症指标和组织检查未见重大毒性,器官内的金含量在两天内回落至接近基线。作者强调,金更多地作为概念验证的骨架:相同的内部设计原则可以应用于其他安全或生物降解材料。对非专业读者来说,核心信息是我们如何在微小载体内包装 mRNA,可能和我们用什么来包装一样重要。通过赋予脂质纳米粒更有序的内部布局,这项工作提供了一种克服 mRNA 递送长期瓶颈的新途径——为传染病、癌症及其他领域带来更高效的疫苗和疗法的可能性。
引用: Li, T., Zhang, J., Guo, J. et al. Engineered internal architecture of core-shell lipid nanoparticles promotes efficient mRNA endosomal release. Nat Commun 17, 2187 (2026). https://doi.org/10.1038/s41467-026-69017-8
关键词: mRNA 递送, 脂质纳米粒, 内体逃逸, 纳米医学, RNA 疫苗