Clear Sky Science · zh
FGF13 在败血性肺损伤炎症状态中作为 ERK/有氧糖酵解轴的调节因子
这项研究对重症感染患者的重要性
败血症是感染导致的危及生命的并发症,能够在数小时内使肺功能衰竭,使患者依赖呼吸机并面临高死亡风险。本研究探讨了细胞内一种鲜为人知的蛋白——FGF13,并揭示了它如何推动失控的炎症和能量过度消耗,这些过程在败血症期间严重损害肺组织。通过追踪这一隐蔽的控制回路,研究指出了可能抑制肺部炎症风暴的新药物靶点,同时不至于全面抑制机体的免疫反应。
在败血性肺损伤中的隐秘参与者
研究人员首先比对了败血性小鼠与人类患者的肺组织与非败血性对照组织,检查了一类被称为成纤维细胞生长因子的分子家族,这些因子有助于维持肺组织健康。在这些因子中,FGF13 显著突出:败血性患者和动物的肺中其水平明显降低。当团队追踪 FGF13 的位置时,发现它主要存在于两类关键细胞中:形成血管内膜的内皮细胞和感知并放大炎症反应的巨噬细胞。在败血性肺组织中,FGF13 阳性的内皮细胞和巨噬细胞大幅减少,暗示该分子变化可能与严重的肺损伤相关。
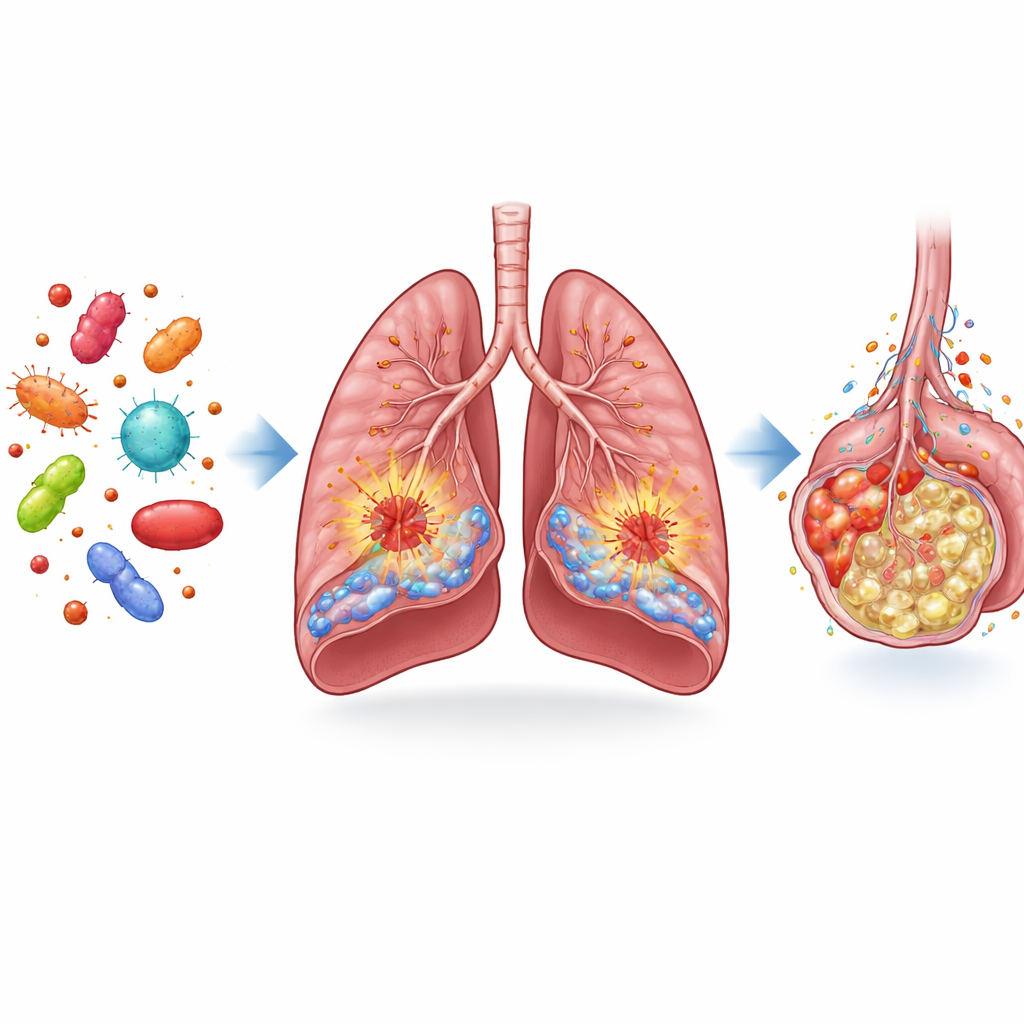
FGF13 如何把肺部防御细胞变成促损害的推手
为测试 FGF13 的实际功能,科研团队在小鼠中用遗传学工具有选择性地删除或过表达该蛋白。当仅在内皮细胞中缺失 FGF13 时,败血性小鼠表现出更少的肺漏出和水肿、侵入性免疫细胞减少以及更好的存活率。相反,当内皮细胞被改造为过度产生 FGF13 时,肺水肿、出血和炎性细胞积聚加重。在巨噬细胞中也观察到类似结果:缺乏巨噬细胞内 FGF13 的小鼠炎症反应较弱、肺损伤较轻,而被迫过表达 FGF13 的巨噬细胞释放更多促炎分子并加剧损害。在细胞培养中,降低 FGF13 使血管细胞和巨噬细胞的黏附性、炎症水平和对邻近细胞的毒性均下降。
发炎细胞切换到嗜糖模式
发炎细胞(类似肿瘤细胞)常改变其能量策略:不再依赖氧化缓慢燃烧燃料,而是快速通过名为有氧糖酵解的途径分解葡萄糖,产生乳酸。作者发现 FGF13 强力推动这一转变。在缺失内皮细胞或巨噬细胞内 FGF13 的败血性小鼠中,血乳酸水平较低。在体外实验中,降低 FGF13 的细胞在炎症刺激后摄取的葡萄糖和产生的乳酸都减少,而过表达 FGF13 的细胞则表现出增强的糖酵解。当研究者用药物抑制糖酵解时,过量 FGF13 促炎的效应大部分被削弱,将该分子的有害作用直接联系到它所促进的嗜糖代谢程序。
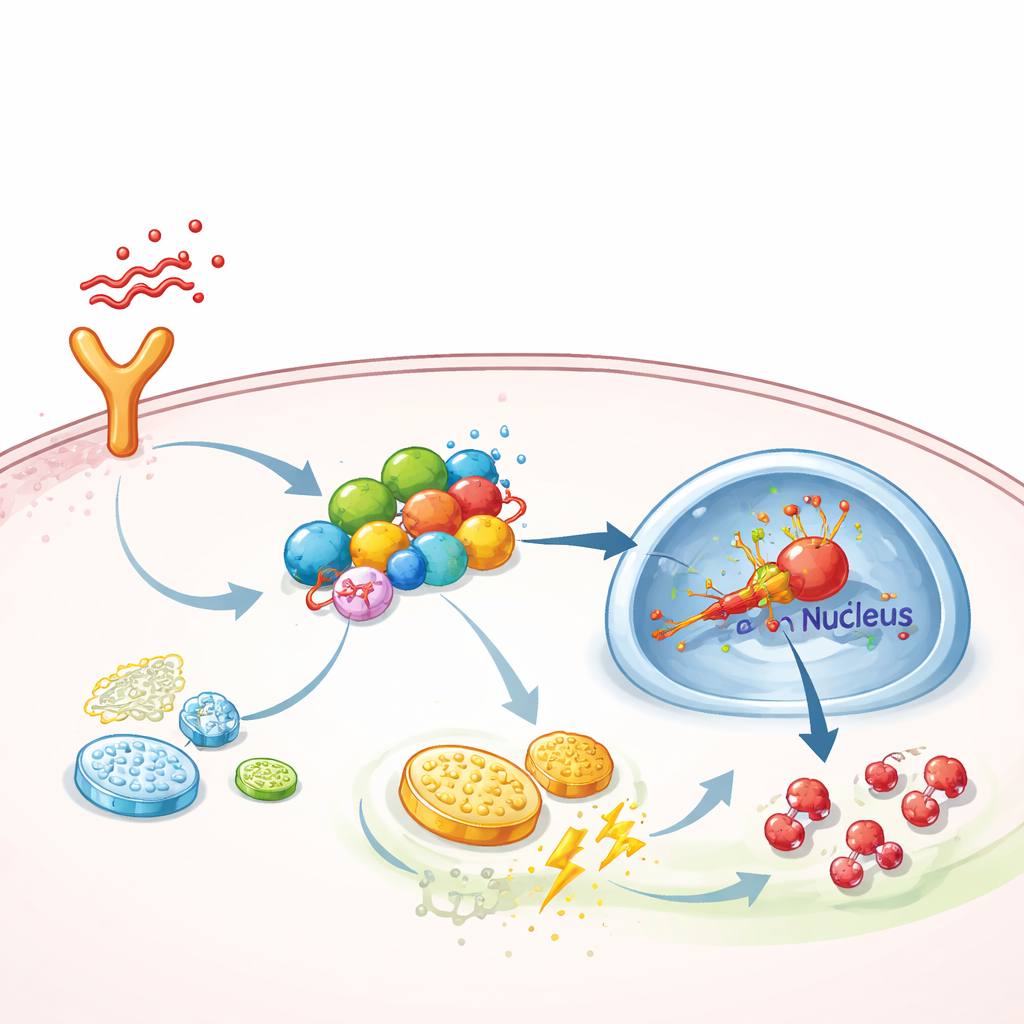
增强炎症信号的分子脚手架
进一步探究时,团队询问 FGF13 如何将细胞推向这种高效代谢状态。他们发现 FGF13 能够物理结合多种信号蛋白,这些蛋白构成了一条从细胞表面受体到细胞核的信号链——具体为 TAK1–MEK–ERK 通路,该通路已知可激活名为 HIF-1α 的缺氧应答主调控因子。FGF13 像一个脚手架,将这些组分聚拢在一起,使信号传递更高效。当 FGF13 水平降低时,ERK 和 HIF-1α 的激活下降,糖酵解减弱;反之,FGF13 增多则使该通路过度活化。在小鼠中过表达 HIF-1α 抹去了删除 FGF13 所带来的保护效应,而选择性 ERK 抑制剂 SCH772984 则中和了 FGF13 过表达所致的损害并改善了败血性动物的肺部状况。
对未来败血症治疗的启示
对非专业读者而言,关键结论是:败血性肺损伤并非纯粹随机的组织破坏,而是由血管内皮细胞和巨噬细胞内一个特定分子回路驱动。FGF13 位于该回路的核心,帮助组装一个信号枢纽,使细胞进入嗜糖且高度促炎的状态。尽管败血症期间 FGF13 水平下降——可能是更广泛应激反应的一部分——本研究表明残存的蛋白仍能显著促成损害。通过阻断 FGF13 的信号伙伴或其促进的糖酵解转变,或许可以在不削弱机体抗感染能力的前提下,减少肺部水肿、渗漏和炎症。因而该研究将 FGF13 及 ERK–HIF‑1α–糖酵解轴突出了作为开发更精确、更安全的败血症相关肺功能衰竭治疗方案的有前景靶点。
引用: Zhu, J., Wang, J., Jiang, C. et al. FGF 13 functions as a regulator of the ERK/aerobic glycolysis axis in the inflammatory state during septic lung injury. Nat Commun 17, 2383 (2026). https://doi.org/10.1038/s41467-026-69014-x
关键词: 败血性肺损伤, FGF13, 内皮炎症, 有氧糖酵解, ERK 信号