Clear Sky Science · zh
联合靶向与表观遗传学疗法通过稳定GATA6依赖的MHCI表达增强胰腺导管腺癌的抗肿瘤免疫
这项研究对胰腺癌的重要性
胰腺导管腺癌是最致命的癌症之一,很大程度上因为它能躲避免疫系统并对多数药物耐受。该研究揭示了一种由基因GATA6驱动的肿瘤细胞状态,使胰腺癌细胞更易被免疫系统识别并受攻击。作者还展示了如何通过组合两类药物维持这一脆弱状态,从而在实验模型中增强杀伤性T细胞对肿瘤的攻击能力。
一种更易被免疫系统识别的肿瘤细胞状态
并非所有胰腺癌细胞行为相同。有些细胞保持更有序的上皮样身份,而另一些则向更具迁移性、侵袭性的间充质样状态转变。转录因子GATA6有助于维持上皮身份,并与患者更好的预后相关。在大规模患者队列中,GATA6水平高的肿瘤比GATA6缺失或极低的肿瘤含有更多免疫细胞,包括CD8“杀伤”T细胞。利用对人体肿瘤样本的先进空间成像,研究者发现GATA6阳性的癌细胞更常位于CD8 T细胞旁,并显示更高水平的MHCI,这种分子像一面旗帜,向T细胞展示细胞内的内容。这些观察提示GATA6标记了一类天然更易被免疫系统识别的肿瘤细胞群体。 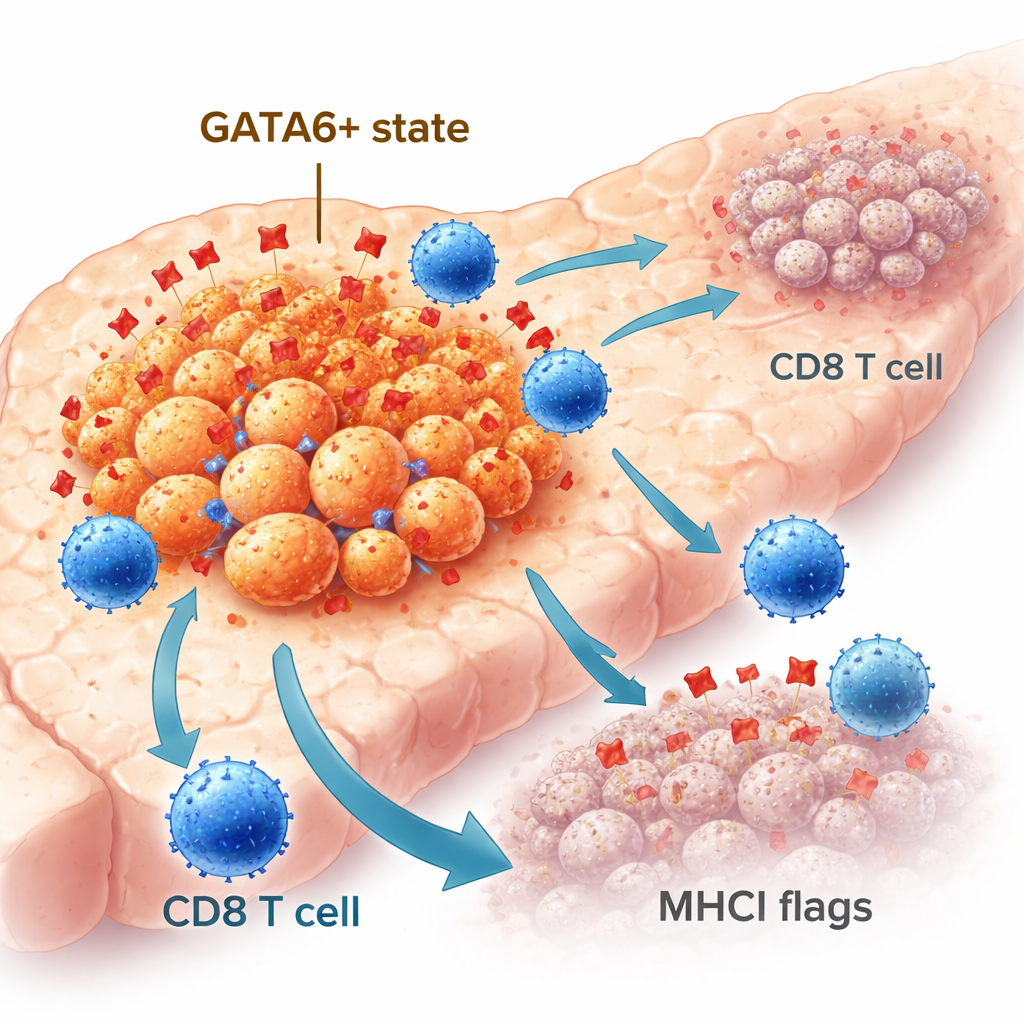
能提高肿瘤可见性的靶向疗法——但有代价
团队接着探讨靶向药物能否进一步增强这种可见性。他们聚焦于MEK抑制剂,这类药物阻断在胰腺癌中常见的生长信号通路。在小鼠胰腺癌细胞系、移植于小鼠的肿瘤以及患者来源的异种移植肿瘤中,MEK抑制使GATA6高表达的肿瘤细胞表面MHCI增加,使其成为T细胞更好的靶点。在小鼠体内对GATA6高的肿瘤用MEK抑制剂处理后,肿瘤生长减慢、MHCI上调,携带细胞毒分子的CD8 T细胞更多地浸润到肿瘤中。直接阻断GATA6(如基因敲除或快速降解该蛋白)则消除了MEK抑制剂诱导的MHCI上升及相应的肿瘤控制,证明GATA6对这一有益效应是必需的。
肿瘤如何适应:滑向更难被杀死的状态
然而,情况并不简单。长期使用MEK抑制剂促使许多肿瘤细胞从GATA6阳性的上皮状态转向更具间充质特征、GATA6低表达的耐药状态。在小鼠模型和患者来源的异种移植中,MEK抑制剂处理后肿瘤最终显示出GATA6阳性细胞减少、上皮-间充质转化的标志增加,以及总体疗效不持久。尽管单个GATA6阳性细胞仍会对药物做出MHCI上调的反应,但该细胞群体规模缩小限制了整体肿瘤抗原呈递的改善,这有助于解释为何单用MEK抑制剂在胰腺癌临床试验中效果令人失望。
把肿瘤“钉”在脆弱状态的表观遗传药物
为对抗这种适应性逃逸,研究者转向组蛋白脱乙酰酶抑制剂(HDAC抑制剂),一类已知能影响细胞身份和免疫可见性的表观遗传药物。在细胞培养和小鼠模型中,将MEK抑制剂与I类HDAC抑制剂(如domatinostat)联合使用,恢复了因MEK抑制而被抑制的GATA6表达,逆转了上皮-间充质转化的迹象,并进一步提高了肿瘤细胞表面的MHCI水平。重要的是,这种联合治疗在原位小鼠肿瘤和一种高度模拟人类胰腺癌的基因工程小鼠模型中,加强了CD8 T细胞的浸润与活化,并促使更多肿瘤细胞死亡。耗尽CD8 T细胞会消除大部分获益,确认该组合疗法主要通过增强杀伤性T细胞发挥作用。
朝着对付顽固癌症的更聪明组合疗法迈进
综合这些发现,研究提出了一种策略:联用靶向的MEK抑制和表观遗传的HDAC抑制以稳定一种由GATA6驱动、富含MHCI且更易被免疫系统识别的肿瘤细胞状态。通过既增加GATA6阳性细胞的数量又增强它们的MHCI“旗帜”,该组合促进更深的CD8 T细胞浸润、更强的细胞毒活性,并在侵袭性小鼠模型中延长生存。尽管HDAC抑制剂可能带来显著副作用且该工作仍处于临床前阶段,这项研究为未来将通路靶向药物与审慎选择的表观遗传修饰剂配对,以增强机体自身免疫防御对胰腺肿瘤的脆弱性,指明了方向。 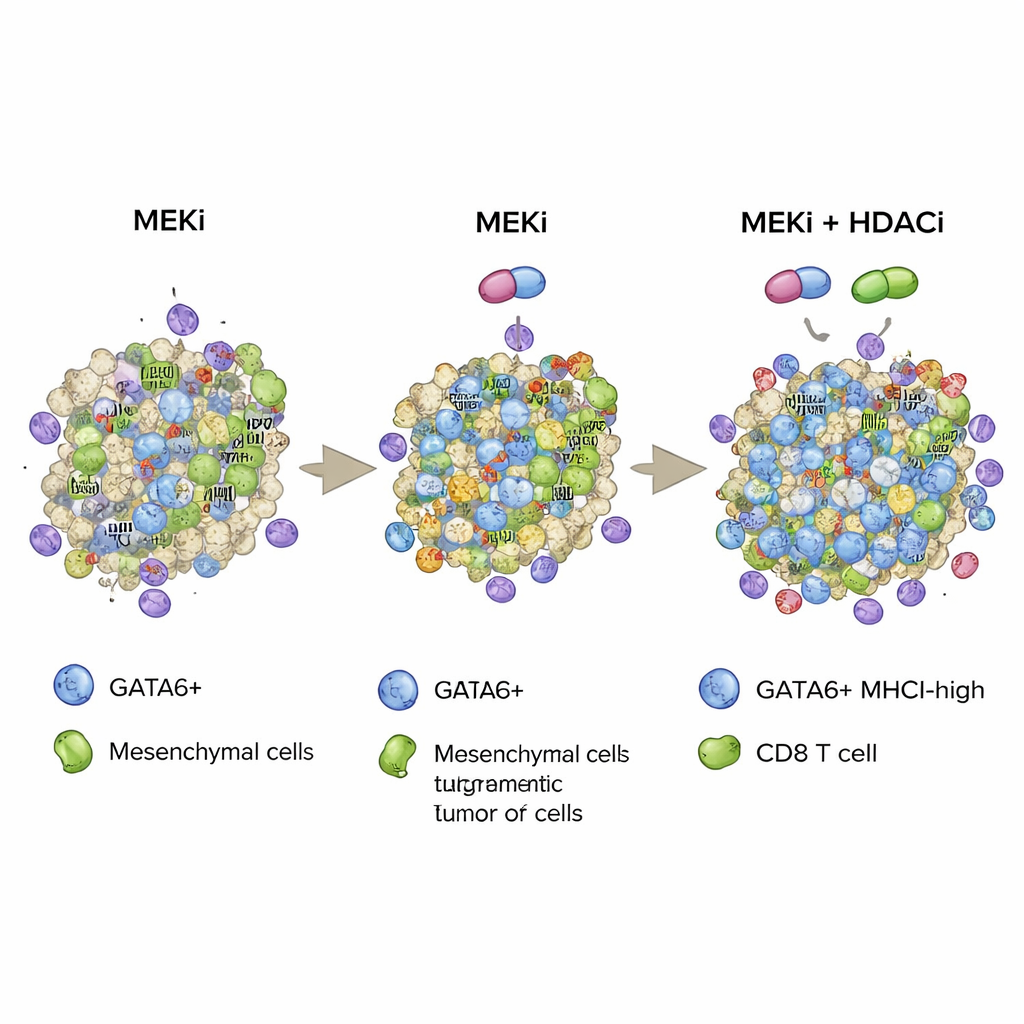
引用: Peng, J., Yang, J., Antonopoulou, G. et al. Combined targeted and epigenetic-based therapy enhances antitumor immunity by stabilizing GATA6-dependent MHCI expression in pancreatic ductal adenocarcinoma. Nat Commun 17, 1476 (2026). https://doi.org/10.1038/s41467-026-69013-y
关键词: 胰腺癌, 肿瘤免疫, GATA6, MEK抑制剂, HDAC抑制剂